- Accueil
- Volume 77 (2024)
- Inventaire préliminaire des relations entre pucerons myrmécophiles et fourmis des parcelles agricoles en périphérie de la ville d’Antananarivo (Madagascar)
Visualisation(s): 1263 (30 ULiège)
Téléchargement(s): 41 (0 ULiège)
Inventaire préliminaire des relations entre pucerons myrmécophiles et fourmis des parcelles agricoles en périphérie de la ville d’Antananarivo (Madagascar)

Document(s) associé(s)
Version PDF originaleRésumé
Cette étude avait pour objectif de fournir un inventaire préliminaire des interactions entre différentes espèces de fourmis et de pucerons myrmécophiles en périphérie d’Antananarivo. Nous avons identifié cinq espèces de pucerons exotiques, tels que Aphis fabae Scopoli 1763, Aphis citricidus (Kirkaldy 1907), Rhopalosiphum maidis (Fitch 1856), Aphis spiraecola Patch 1914 et Macrosiphum euphorbiae (Thomas 1878), sur un total de quatre espèces de plantes hôtes en interaction avec quatre espèces de fourmis mutualistes : Monomorium madecassum Forel 1892, Nylanderia gracilis (Forel 1892), Camponotus liandia Rakotonirina & Fisher 2018, Camponotus maculatus (Fabricius 1782). Dans cet article nous détaillons quelles espèces ont été en interaction. Enfin, nous discutons d’éventuelles raisons qui pourraient expliquer ces observations, comme le régime alimentaire de pucerons et nous proposons quelques pistes pour de futures recherches.
Abstract
This study aimed to provide a preliminary inventory of interactions between different ant species and myrmecophilous aphids on the outskirts of Antananarivo. We identified five exotic aphid species, such as Aphis fabae Scopoli 1763, Aphis citricidus (Kirkaldy 1907), Rhopalosiphum maidis (Fitch 1856), Aphis spiraecola Patch 1914 et Macrosiphum euphorbiae (Thomas 1878), on a total of four host plant species interacting with four mutualistic ant species: Monomorium madecassum Forel 1892, Nylanderia gracilis (Forel 1892), Camponotus liandia Rakotonirina & Fisher 2018, Camponotus maculatus (Fabricius 1782). In this article, we detail the species that interacted. Finally, we discuss possible reasons that could explain these observations, such as the aphids' diet, and propose some avenues for future research.
Reçu le 6 novembre 2023, accepté le 2 février 2024.
Cet article est distribué suivant les termes et les conditions de la licence CC-BY (http://creativecommons.org/licenses/by/4.0/deed.fr)
1Introduction
2Depuis des années, les relations entre plantes-pucerons et fourmis font l’objet de nombreuses études, que ce soit par des éthologues, des biologistes ou bien des agronomes (Depa, 2010; Stadler & Dixon, 2005). En effet, ces relations multi-trophiques peuvent à la fois avoir un grand impact sur l’agriculture et sur notre compréhension des interactions symbiotiques (Dedryver et al., 2010). Les pucerons (Hemiptera : Aphidoidea), se nourrissent de la sève élaborée des plantes à l’aide de leurs pièces buccales modifiées en rostre piqueur-suceur et vont donc les affaiblir en puisant leurs ressources (Dedryver et al., 2010). Ce mode d’alimentation est la source de transmission de nombreux pathogènes (e.g., bactéries, virus et champignons) et place donc les pucerons parmi les grands ravageurs de cultures à travers le monde (Bowling et al., 2016; Ng & Perry, 2004; Stavrinides et al., 2009). La sève du phloème étant riche en sucres et pauvres en acides aminés, les pucerons doivent en absorber de grandes quantités afin de subvenir à leurs besoins les amenant à devoir évacuer l’excédent de liquide sucré (M. K. Fischer & Shingleton, 2001). Cette excrétion, qui sort en petites gouttelettes de leur anus, porte le nom de miellat (Douglas, 2006). Ce miellat, contient des trisaccharides comme le mélézitose qui est fortement appétant pour les fourmis (Hymenoptera : Formicidae) (Detrain et al., 2010). Certaines espèces de pucerons considérées comme myrmécophiles vont offrir du miellat aux fourmis en échange de leur protection (Kaszyca-Taszakowska et al., 2022) contre des prédateurs, des parasitoïdes et certains pathogènes (El-Ziady & Kennedy, 1956; Rice & Eubanks, 2013). Au-delà de cette fonction défensive, les fourmis peuvent avoir un impact non négligeable sur les populations aphidiennes. En effet, lorsqu’une colonie de pucerons devient trop importante, les fourmis peuvent réguler la croissance de la colonie aphidienne (Endo & Itino, 2013). De plus, les fourmis peuvent exercer de la prédation sur les pucerons lorsque ceux-ci ne produisent pas assez de miellat pour se nourrir ou bien pour nourrir les larves de fourmis (Sakata, 1994). Les relations entre les fourmis et les pucerons myrmécophiles sont donc complexes et le type d’interaction entre ces organismes peut être déterminé par différents paramètres : la présence de certaines bactéries dans le miellat, la disponibilité en protéines par rapport aux hydrates de carbones, l’espèce de puceron et la qualité du miellat produit par ce dernier (Endo & Itino, 2012, 2013; C. Y. Fischer et al., 2015, 2017; Sakata, 1994).
3Bien que Madagascar soit connue pour être un berceau de la biodiversité, les données sur les relations entre fourmis et pucerons y sont presque inexistantes. Concernant les pucerons, il existe essentiellement des données à propos d’Aphis gossypii Glover. 1877 de Pentalonia nigronervosa Coquerel. 1859 d’Eriosoma lanigerum (Hausmann 1802) et du genre Paulianaphis (De Clerck et al., 2014, 2015; Frappa, 1937; Ghosh, 1982; Kuklinski & Borgemeister, 2002; Paulian 1950). Pour ce qui est des fourmis l’inventaire taxonomique est beaucoup plus détaillé. En 2019 the California Academy of Sciences dénombrait 62 genres de fourmis à Madagascar (Fisher & Peeters, 2019). Nous avons voulu faire un inventaire préliminaire des pucerons et des fourmis en associations dans les parcelles agricoles en périphérie d’Antananarivo afin d’identifier quelles espèces de pucerons et de fourmis entretiennent des interactions.
MATERIEL ET METHODES
Lieux d’étude
4Pour notre étude, cinq sites ont été échantillonnés pour un total de onze parcelles dans la périphérie d’Antananarivo, Madagascar (Figure 1). Les échantillonnages ont été réalisés sur la période 16 avril au 15 juin 2023. Pour qu’une parcelle agricole ou un jardin soit sélectionné comme zone d’étude, celle-ci devait contenir au moins trois plantes d’une même espèce (Phaseolus vulgaris L. 1753; Citrus limon (L.) Burm. f. 1768; Solanum nigrum L. 1753; Zea mays L. 1753 ) sur lesquelles se trouvaient des pucerons fréquentés par des fourmis. Quatre espèces de plantes agricoles (haricot, citronnier, morelle noire et le maïs) ont été sélectionnées afin de faire un constat préliminaire sur la présence de pucerons sur différentes plantes couramment consommées dans la région sur une parcelle d’au moins un are. Deux autres points importants ont été considérés pour orienter les choix de zones d’études dont : l’accessibilité du site et l’acceptation du paysan pour la collecte des spécimens.
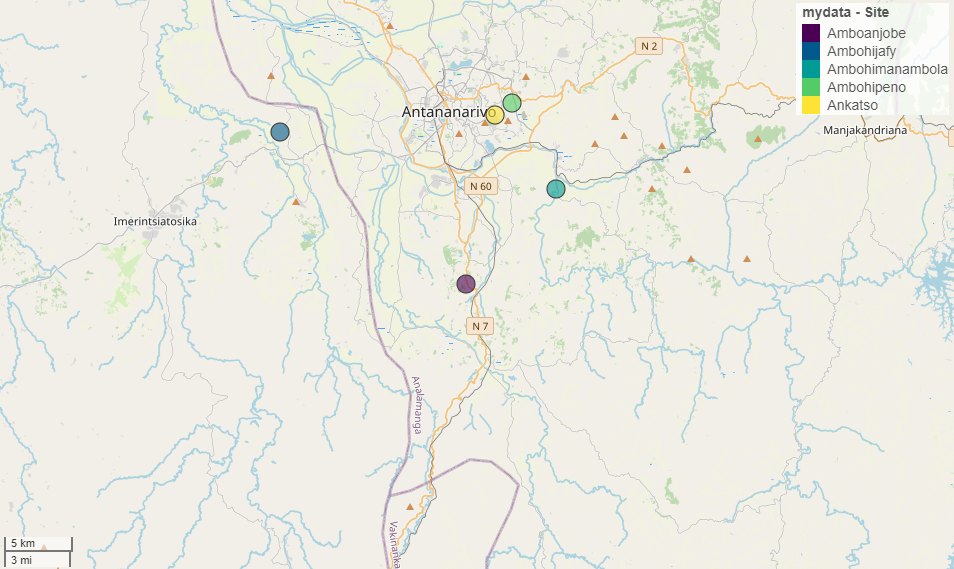
Figure 1 : Sites d’échantillonnages en périphérie d’Antananarivo (Madagascar).
5Récolte des pucerons et des fourmis
6Les insectes étudiés ont été prélevés à l’aide d’un aspirateur à insecte confectionné à la main, à l’aide des doigts ou d’une brindille lorsque la situation l’exigeait. La totalité des fourmis se trouvant sur une même plante hôte ont été mises dans un même tube Eppendorf de 2 ml contenant de l’éthanol à 70% et une quinzaine de pucerons d’une même plante hôte ont aussi été regroupés dans un même tube Eppendorf. Les échantillons ont été étiquetés et conservés à une température ambiante d’environ 20°C jusqu’au retour en Belgique.
7Identification des pucerons et des fourmis
8Les fourmis ont été identifiées morphologiquement par le centre de recherche California Academy of Sciences de Tananarive grâce à des clés d’identifications spécifiques à chaque genre et en comparaison à des exemples provenant de boites de collections. Les pucerons ont quant à eux été identifié moléculairement via le séquençage du gène mitochondrial codant pour la Cytochrome Oxydase I (COI).
9Techniques d’identification moléculaire
10L’ADN des insectes a été extrait en utilisant le kit QIAamp PowerFecal Pro DNA (Référence : 51804 ; QIAGEN, Hilden Allemagne), en suivant les consignes du fabricant. L’ADN a été élué dans 50 μl de tampon C6 du kit et 2 μl d’ADN par échantillon ont ensuite été dosés à l’aide du NanoDrop One (Isogen Life Science, Utrecht Pays-Bas).
11Le gène d’ADN mitochondrial codant pour la cytochrome oxydase I (COI) a été amplifié à l’aide des primers LCO (5'- GGTCAACAAATCATAAAGATATTGG -3') et HCO (5'- TAAACTTCAGGGTGACCAAAAAATCA -3') (Folmer et al., 1994; Wilson et al., 2022). Pour chaque échantillon, un mix de 40 μl a été réalisé et a ensuite été complété avec 10 μl d’ADN par échantillon. Le détail de chaque mix PCR est présenté dans le tableau 1 :
Tableau 1 : Composition d’un mix PCR utilisé pour amplifier le gène codant pour la COI.
|
Produit |
Quantité |
|
Eau déminéralisée stérilisée |
10 μl |
|
Q5 High-Fidelity 2X Master Mix, (New England Biolabs Inc, Massachusetts, États-Unis) |
25 μl |
|
Forward (LCO) |
2,5 μl |
|
Reverse (HCO) |
2,5 μl |
|
ADN |
10 μl |
|
Total |
50 μl |
12Le programme utilisé avec le thermocycleur iCycler (BioRad, Californie, Etats-Unis), est le suivant. La Polymérase haute-fidélité est activée, suivie d'une dénaturation de l'ADN à 98°C pendant 30 secondes, avant le commencement des cycles. Chacun des 35 cycles a comporté une dénaturation de l’ADN à 98°C pendant 10 secondes, un appareillement des amorces à 55°C pendant 30 secondes, une élongation des brins à 72°C pendant 30 secondes. Une phase d’élongation finale à 72°C pendant 2 minutes a suivi les cycles puis la température a été portée à 4°C jusqu’à ce que les échantillons soient récupérés.
13Ensuite le kit NucleoSpin Gel and PCR Clean‑up (Thermo Fisher Scientific, Massachusetts, USA) a été utilisé en suivant les consignes du fabricant afin de purifier les amplicons avant de les envoyer au séquençage de Sanger (Eurofins Genomics Germany GmbH, Munich, Allemagne)
14Identification moléculaire des pucerons
15Une fois les fichiers des séquences Forward et Reverse récupérés, les séquences où l’ADN n’était pas dégradé ont été sélectionnées à la main. Le logiciel SerialCloner 2.6.1 (Serial Basics) a permis de réaliser un alignement local des deux séquences d’ADN correspondant à chaque échantillon. Le site internet « NCBI BLAST » (Johnson et al., 2008) a ensuite été utilisé afin de comparer les séquences à la base de données du site. Un BLAST (Basic Local Alignment Search Tool) a été effectué avec les autres arthropodes de la librairie du site internet. Seul les espèces possédant 100% d’identité de leur COI ont été sélectionnées.
RESULTATS
16Espèces récoltées
17Durant la période d’échantillonnage les pucerons et les fourmis ont été récoltés sur cinq sites en périphérie d’Antananarivo avec un total de 5 espèces différentes de pucerons myrmécophiles : Aphis fabae Scopoli 1763; Aphis citricidus (Kirkaldy 1907); Rhopalosiphum maidis (Fitch 1856); Aphis spiraecola Patch 1914; Macrosiphum euphorbiae (Thomas 1878). Pour ce qui est des fourmis mutualistes, un total de 4 espèces ont été récoltées: Monomorium madecassum Forel 1892; Nylanderia gracilis (Forel 1892); Camponotus liandia Rakotonirina & Fisher 2018; Camponotus maculatus (Fabricius 1782).
18Le puceron A. fabae a été retrouvé sur le citron et le haricot ; A. citricidus sur le citron ; A. spiraecola sur le citron ; R. maidis sur le maïs ; M. euphorbiae sur la morelle noire (Tableau 2).
Tableau 2 : Répartition et abondance relative des espèces de pucerons sur les différentes espèces de plantes hôtes.

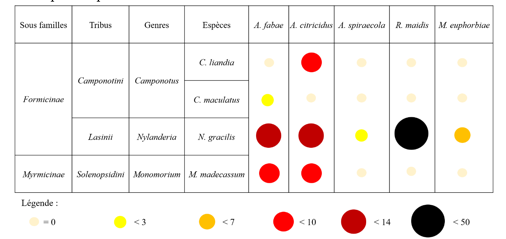
19La fourmi C. liandia a été retrouvée avec A. citricidus ; C. maculatus avec A.fabae ; N. gracilis avec A. citricidus, A. fabae, A. spiraecola, R. maidis et M. euphorbiae ; M. madecassum avec A. fabae et A. citricidus (Tableau 3).
Tableau 3 : Abondance relative des espèces de fourmis en fonction de l’espèce de pucerons associées.
DISCUSSION
20Les fourmis et les pucerons entretiennent une relation mutualiste qui favorise le développement et la survie de ces derniers. Mieux connaître ces associations nous permet d’un côté, d’en apprendre davantage sur la biologie de ces espèces et à la fois d’identifier la présence de ravageurs de cultures. Au stade actuel, aucune de ces espèces de puceron inventoriées n’est endémique. Ce sont toutes des espèces exotiques et certaines sont inféodés aux cultures maraichères (Renaud 1950, Reckhaus 1997). Pour ce qui est des fourmis deux espèces sont endémiques de l’île, N. gracilis et C. liandia.
21Notre inventaire préliminaire des associations entre pucerons et fourmis en périphérie d’Antananarivo a permis d’identifier cinq espèces de pucerons en association avec différentes espèces de fourmis. Bien que nous ayons eu recours à l’identification moléculaire pour les pucerons, nous avons supposé comme étant de la même espèce tous les pucerons se trouvant sur la même espèce de plante hôte. Malgré tout il subsistera toujours un doute sur une potentielle cohabitation de plusieurs espèces de pucerons (Inbar & Wool, 1995). Ce doute pourrait quant à lui être amoindri par une connaissance maitrisée des parasitoïdes, des prédateurs et de la biologie générale des pucerons. Cela pourrait permettre de relever certains indices spécifiques à certaines espèces. Parmi les cinq espèces de pucerons, quatre d’entre elles sont polyphages (A. fabae, A. spiraecola, R. maidis, M. euphorbiae) et une de ces espèces a un régime oligophage (A. citricidus) (Guidolin & Cônsoli, 2020; Kuo et al., 2006; Papadimitriou et al., 2019; Raboudi et al., 2005; Wilkinson & Douglas, 2003). Nous avons constaté que les espèces de pucerons de notre étude les plus fréquentés par différentes espèces de fourmis sont respectivement le puceron oligophage A. citricidus (C. liandia, N. gracilis, M. madecassum) et le puceron polyphage A. fabae (C. maculatus, N. gracilis, M. madecassum). Il est à noter que l’espèce A. citricidus n’est pas recensé dans l’ouvrage de Paulian (1950), (Reckhaus 1997). A notre connaissance, il n’y a pas de données montrant que le régime oligophage ou polyphage d’un puceron augmente son attrait pour différentes espèces de fourmis. Il serait dès lors intéressant d’investiguer si les pucerons oligophages ou polyphages d’un endroit donné interagissent avec davantage d’espèces de fourmis. Il est important de prendre en compte que l’espèce de puceron et de plante hôte influencent la composition du miellat, au niveau du type de sucre et de leur concentration (Hendrix et al., 1992; Hogervorst et al., 2007). Ces facteurs peuvent donc être à l’origine du fait que nous ayons retrouvé plus d’espèces de fourmis associées aux pucerons A. citricidus et A. fabae. Pour ce qui est des quatre espèces de fourmis que nous avons identifiées en association avec des pucerons dans notre étude, la fourmi N. gracilis est celle qui interagit avec le plus grand nombre d’espèces de pucerons (A. citricidus, A. fabae, A. spiraecola, R. maidis, M. euphorbiae). Cela pourrait s’expliquer par le fait que les fourmis du genre Nylanderia sont connues pour fourrager activement et se faire très présentes par rapport aux autres espèces de leur milieu (Lapolla et al., 2011). Le faible nombre d’espèces que nous avons récolté s’explique probablement car notre échantillonnage n’a pas été exhaustif du fait que nous nous sommes cantonnés à quatre espèces de plantes hôtes. Il serait dès lors intéressant d’étendre l’échantillonnage que ce soit au niveau de sa zone géographique et du nombre d’espèces de plantes hôtes. La présente étude démontre le caractère envahissant de ces espèces de pucerons. Des mesures préventives comme le monitoring devrait être planifiés afin d’éviter l’extension de leur aire de distribution et l’usage excessif de pesticide. La nécessité d’une mise en place d’un suivi écologique de ces espèces envahissantes comme ce fut le cas avec les fourmis exotiques soulevés par Rakotonirina (2010) et par Ravelomanana et al (2022) mérite d’être prise au sérieux par les autorités scientifiques du pays.
CONCLUSION
22Ce travail a permis d’identifier différentes espèces de fourmis et de pucerons qui entretiennent des relations dans des jardins et cultures en périphérie de la capitale malgache. En plus d’apporter des connaissances sur la biologie de ces différents insectes ce travail permet d’identifier quelles zones encourent un risque face aux pucerons.
Remerciements
Merci à l’ARES (Académie de recherche et d'enseignement supérieur) d’avoir financé le voyage de fin d’étude qui a permis de réaliser cette recherche. Nous tenons à remercier aussi le Ministère de l’Environnement et du Développement Durable pour le Permis de recherche 151/23/MEDD/SG/DGGE/DAPRNE/SCBE.Re. Merci à l’insectarium et au le laboratoire d’entomologie-culture, élevage et santé de l’Université d’Antananarivo pour leur implication et leur soutien logistique durant cette étude. Merci à Emilie Bera pour son encadrement et son aide concernant la partie moléculaire.
Bibliographie
Bowling R.D., Brewer M.J., Kerns D.L., Gordy J., Seiter N., Elliott N.E., Buntin G.D., Way M.O., Royer T.A., Biles S. & Maxson E., 2016. Sugarcane aphid (Hemiptera: Aphididae): A new pest on sorghum in North America. Journal of Integrated Pest Management. 7(1), 12. doi:10.1093/jipm/pmw011.
California Academy of Science, October-10-2023. Antweb. https://www.antweb.org/bioregion.do?name=Malagasy, (dernière consulation le 10/10/2023).
De Clerck C., Fujiwara A., Joncour P., Léonard S., Félix M.-L., Francis F., Jijakli M.H., Tsuchida T. & Massart S., 2015. A metagenomic approach from aphid’s hemolymph sheds light on the potential roles of co-existing endosymbionts. Microbiome. 3(1), 63. doi:10.1186/s40168-015-0130-5.
De Clerck C., Tsuchida T., Massart S., Lepoivre P., Francis F. & Jijakli M.H., 2014. Combination of genomic and proteomic approaches to characterize the symbiotic population of the banana aphid (Hemiptera: Aphididae). Environmental Entomology. 43(1), 29–36. doi:10.1603/EN13107.
Dedryver C.-A., Le Ralec A. & Fabre F., 2010. The conflicting relationships between aphids and men: a review of aphid damage and control strategies. Comptes Rendus Biologies. 333(6–7), 539–553. doi:10.1016/j.crvi.2010.03.009.
Depa, Ł. (2010). Possibility of overwintering of Aphis sambuci Linnaeus, 1758 /Hemiptera, Aphididae/ on secondary host in the climatic conditions of Poland. Aphids and Other Hemipterous Insects. 16, 21‑25.
Detrain C., Verheggen F.J., Diez L., Wathelet B. & Haubruge E., 2010. Aphid–ant mutualism: how honeydew sugars influence the behaviour of ant scouts. Physiological Entomology. 35(2), 168–174. doi:10.1111/j.1365-3032.2010.00730.x.
Douglas A.E., 2006. Phloem-sap feeding by animals: problems and solutions. Journal of Experimental Botany. 57(4), 747–754. doi:10.1093/jxb/erj067.
El-Ziady S. & Kennedy J.S., 1956. Beneficial effects of the common garden ant, Lasius niger L., on the black bean aphid, Aphis fabae Scopoli. Proceedings of the Royal Entomological Society of London. Series A, General Entomology. 31(4–6), 61–65. doi:10.1111/j.1365-3032.1956.tb00208.x.
Endo S. & Itino T., 2012. The aphid-tending ant Lasius fuji exhibits reduced aggression toward aphids marked with ant cuticular hydrocarbons. Population Ecology. 54(3), 405–410. doi:10.1007/s10144-012-0314-9.
Endo S. & Itino T., 2013. Myrmecophilous aphids produce cuticular hydrocarbons that resemble those of their tending ants. Population Ecology. 55(1), 27–34. doi:10.1007/s10144-012-0355-0.
Fischer C.Y., Detrain C., Thonart P., Haubruge E., Francis F., Verheggen F.J. & Lognay G.C., 2017. Bacteria may contribute to distant species recognition in ant-aphid mutualistic relationships. Insect Science. 24(2), 278–284. doi:10.1111/1744-7917.12302.
Fischer, C. Y., Lognay, G. C., Detrain, C., Heil, M., Grigorescu, A., Sabri, A., Thonart, P., Haubruge, E., & Verheggen, F. J. (2015). Bacteria may enhance species association in an ant–aphid mutualistic relationship. Chemoecology. 25(5), 223‑232. DOI: 10.1007/s00049-015-0188-3
Fischer M.K. & Shingleton A.W., 2001. Host plant and ants influence the honeydew sugar composition of aphids. Functional Ecology. 15(4), 544–550. doi:10.1046/j.0269-8463.2001.00550.x.
Fisher B.L. & Peeters C., 2019. Ants of Madagascar: A Guide to the 62 Genera, Guides sur la diversité biologique de Madagascar, Antananarivo: Association Vahatra in Antananarivo, 262pp.
Folmer O., Black M., Wr H., Lutz R. & Vrijenhoek R., 1994. DNA primers for amplification of mitochondrial Cytochrome C oxidase subunit I from diverse metazoan invertebrates. Molecular Marine Biology and Biotechnology. 3, 294–9.
Frappa C., 1937. Les principaux insectes nuisibles aux cultures de Madagascar. Journal d’Agriculture Traditionnelle et de Botanique Appliquée. 17(191), 513–516. doi:10.3406/jatba.1937.5764.
Ghosh A.K., 1982. Cervaphidini (Homoptera : Aphidoidea) of the world. Oriental Insects. 16(1), 77–98. doi:10.1080/00305316.1982.10434331.
Guidolin A.S. & Cônsoli F.L., 2020. Influence of host plant on oligophagous and polyphagous aphids, and on their obligate symbiont titers. Biologia. 75(1), 71–81. doi:10.2478/s11756-019-00274-3.
Hendrix D.L., Wei Y. & Leggett J.E., 1992. Homopteran honeydew sugar composition is determined by both the insect and plant species. Comparative Biochemistry and Physiology Part B: Comparative Biochemistry. 101(1), 23–27. doi:10.1016/0305-0491(92)90153-I.
Hogervorst P.A.M., Wäckers F.L. & Romeis J., 2007. Effects of honeydew sugar composition on the longevity of Aphidius ervi. Entomologia Experimentalis et Applicata. 122(3), 223–232. doi:10.1111/j.1570-7458.2006.00505.x.
Inbar M. & Wool D., 1995. Phloem-feeding specialists sharing a host tree: Resource partitioning minimizes interference competition among galling aphid species. Oikos. 73(1), 109–119. doi:10.2307/3545732.
Johnson M., Zaretskaya I., Raytselis Y., Merezhuk Y., McGinnis S. & Madden T.L., 2008. NCBI BLAST: a better web interface. Nucleic Acids Research. 36(Web Server), W5–W9. doi:10.1093/nar/gkn201.
Kaszyca-Taszakowska N., Kanturski M. & Depa Ł., 2022. Comparative studies of perianal structures in myrmecophilous aphids (Hemiptera, Aphididae). Insects. 13(12), 1160. doi:10.3390/insects13121160.
Kuklinski F. & Borgemeister C., 2002. Cotton pests and their natural enemies in Madagascar. Journal of Applied Entomology. 126(2–3), 55–65. doi:10.1046/j.1439-0418.2002.00622.x.
Kuo M.H., Chiu M.C. & Perng J.J., 2006. Temperature effects on life history traits of the corn leaf aphid, Rhopalosiphum maidis (Homoptera: Aphididae) on corn in Taiwan. Applied Entomology and Zoology. 41(1), 171–177. doi:10.1303/aez.2006.171.
Lapolla J.S., Brady S.G. & Shattuck S.O., 2011. Monograph of Nylanderia (Hymenoptera: Formicidae) of the World: An introduction to the systematics and biology of the genus. Zootaxa. 3110(1), 1–9. doi:10.11646/zootaxa.3110.1.1.
Ng J.C.K. & Perry K.L., 2004. Transmission of plant viruses by aphid vectors. Molecular Plant Pathology. 5(5), 505–511. doi:10.1111/j.1364-3703.2004.00240.x.
Papadimitriou D.M., Petrakis E.A., Arvaniti K.A., Kimbaris A.C., Polissiou M.G. & Perdikis D.Ch., 2019. Comparative bioactivity of essential oils from two Mentha pulegium (Lamiaceae) chemotypes against Aphis gossypii, Aphis spiraecola, Tetranychus urticae and the generalist predator Nesidiocoris tenuis. Phytoparasitica. 47(5), 683–692. doi:10.1007/s12600-019-00770-x.
Paulian R., 1950. Insectes utiles et nuisibles de la région de Tananarive, Institut de recherche scientifique, 142pp.
Raboudi F., Chavigny P., Marrakchi M., Makni H., Makni M. & Vanlerberghe-Masutti F., 2005. Characterization of polymorphic microsatellite loci in the aphid species Macrosiphum euphorbiae (Hemiptera: Aphididae). Molecular Ecology Notes. 5(3), 490–492. doi:10.1111/j.1471-8286.2005.00966.x.
Rakotonirina J.C., 2010. Survey of leaf litter ant species and assessment of invasive ants in the mining sites at Ambatovy, Madagascar. Malagasy Nature. 3, 77–91.
Ravelomanana, A., Razafimanantsoa Z. T. A., Razafinjatovo M. N., Rakotonirina I. J. & Raharisoa E., 2022. "Sustainable use of the endemic wild silkworm, Borocera cajani, in the Tapia woodland of Madagascar." African Conservation Telegraph. 17(4), 1-6
Reckhaus, P.,1997. Maladies et ravageurs des cultures maraîchères à Madagascar. Weikersheim.
Rice K.B. & Eubanks M.D., 2013. No enemies needed: Cotton aphids (Hemiptera: Aphididae) directly benefit from red imported fire ant (Hymenoptera: Formicidae) tending. The Florida Entomologist. 96(3), 929–932. doi:10.1653/024.096.0329.
Sakata H., 1994. How an ant decides to prey on or to attend aphids. Population Ecology. 36(1), 45–51. doi:10.1007/BF02515084.
Stadler B. & Dixon A.F.G., 2005. Ecology and evolution of aphid-ant interactions. Annual Review of Ecology, Evolution, and Systematics. 36(1), 345–372. doi:10.1146/annurev.ecolsys.36.091704.175531.
Stavrinides J., McCloskey J.K. & Ochman H., 2009. Pea aphid as both host and vector for the phytopathogenic bacterium Pseudomonas syringae. Applied and Environmental Microbiology. 75(7), 2230–2235. doi:10.1128/AEM.02860-08.
Wilkinson T.L. & Douglas A.E., 2003. Phloem amino acids and the host plant range of the polyphagous aphid, Aphis fabae. Entomologia Experimentalis et Applicata. 106(2), 103–113. doi:10.1046/j.1570-7458.2003.00014.x.
Wilson C.R., Cooke-McEwen C., Gilligan T.M. & Tembrock L.R., 2022. Detection of Centistes sp. (Hymenoptera, Braconidae) from intercepted Diabrotica undecimpunctata (Coleoptera, Chrysomelidae) using CO1 DNA barcodes and larval morphology. Journal of Hymenoptera Research. 91, 69–81. doi:10.3897/jhr.91.84139.
(40 Réf.)