- Accueil
- volume 9 (2005)
- Essais de prolifération et d’enracinement de matériel issu de rajeunissement par bouturage d’oliviers adultes (Olea europaea L.) et de germination in vitro : effets de cytokinine et d’auxines
Visualisation(s): 4944 (37 ULiège)
Téléchargement(s): 283 (1 ULiège)
Essais de prolifération et d’enracinement de matériel issu de rajeunissement par bouturage d’oliviers adultes (Olea europaea L.) et de germination in vitro : effets de cytokinine et d’auxines

Notes de la rédaction
Reçu le 1er décembre 2004, accepté le 2 juin 2005
Résumé
Les essais de micropropagation ont concerné le matériel juvénile et adulte de l’olivier ‘Picholine marocaine’. La zéatine, additionnée au milieu de prolifération, a été testée à 0, 1, 5, 10 et 20 mg/l. L’induction racinaire a lieu en présence des auxines AIB, ANA et AIA, comparées aux concentrations 0, 0,5, 1, 2 et 4 mg/l. Une interaction significative (P<0,001) a été notée entre le type d’explant et la concentration de cytokinine d’une part et le type et la concentration d’auxine d’autre part. La concentration de 5 mg/l de zéatine a permis d’obtenir les meilleurs débourrement et développement des pousses. Néanmoins, et pour des raisons économiques, cette cytokinine peut être utilisée convenablement à 1 mg/l. Un enracinement de 100 % des microboutures a été obtenu en présence de 1 mg/l d’ANA qui s’est distingué des autres auxines testées. Aucun enracinement n’a été observé dans le cas du matériel adulte. Des travaux sont en cours pour améliorer la réactivité de ce matériel récalcitrant.
Abstract
Proliferation and rooting of juvenile and adult olive explants (Olea europaea L.): effects of cytokinin and auxins. The micropropagation trials conducted concerned juvenile and adult material from the ‘Moroccan Picholine’ olive cultivar. Zeatin, added to the proliferation medium, was tested at 0, 1, 5, 10 et 20 mg/l. Root induction was performed on media contaning IAA, IBA or NAA tested at 0, 0.5, 1, 2 et 4 mg/l. A significant (P<0.001) interaction exists between the explant type and the cytokinine concentration on one hand and the type and concentration of auxin on the other hand. The highest bud sprouting and shoot development were obtained on medium supplemented with 5 mg/l zeatin. For economical reasons, satisfying results can be obtained with only 1 mg/l. Rooting of microcuttings reached 100% when NAA, which proved to be the best auxin for root induction, was used at 1 mg/l. No rooting was observed in the case of adult plant material. Further investigations are being undertaken to improve the reactivity of this recalcitrant type of material.
Table des matières
1. Introduction
1L’olivier a suscité un intérêt particulier ces dernières années non seulement au niveau de la Méditerranée, principale région oléicole à l’échelle mondiale, mais aussi au niveau d’autres continents, notamment américain. Ce regain d’intérêt est dû, en plus de l’intérêt socio-économique et environnemental de cette espèce, aux qualités sanitaires et nutritionnelles particulières de l’huile d’olive. Le développement de cette culture est tributaire de la mise au point de techniques de production en masse de plants de qualité, permettant la diffusion des clones sélectionnés et des génotypes performants nouvellement obtenus.
2Les progrès réalisés en matière de micropropagation de l’olivier, bien que modestes comparativement à d’autres espèces fruitières, sont prometteurs. Plusieurs cultivars ont ainsi été multipliés in vitro (Leva et al., 2004). Les travaux concernant la Picholine marocaine, représentant près de 98 % des plantations oléicoles au Maroc et destinée à la production d’olives de table et de l’huile d’olive, restent cependant très limités (Walali, Abousalim, 1993 ; Brhadda et al., 2003). Dans cette dernière étude, nous avons identifié un milieu de culture approprié pour le microbouturage de ce cultivar. La synthèse des travaux réalisés chez d’autres cultivars d’olivier montre que d’autres facteurs influencent la morphogenèse des microboutures mises en culture in vitro (Rugini, 1984 ; Rugini, Lavee, 1992 ; Bati et al., 1999).
3Dans le présent travail, les effets de la concentration de zéatine et du type et de la concentration d’auxine ont été étudiés, respectivement, en phase de prolifération et d’enracinement. Ont été comparés les explants issus de matériel adulte et juvénile de la Picholine marocaine.
2. Matériel et méthodes
2.1. Matériel végétal utilisé et méthodes de désinfestation
4Le matériel végétal utilisé provient de la Picholine Marocaine, cultivar à double fin. Les types d’explants comparés proviennent respectivement de plants issus de germination in vitro et de plants obtenus par bouturage semi-ligneux à partir de pieds-mères sélectionnés et âgés de 30 ans. Les pousses de l’année ont été prélevées sur les plants élevés jusqu’à l’âge de quatre ans, en pots, sous serre.
5La germination in vitro des embryons zygotiques, préalablement prétraités à basse température, a lieu dans un milieu MS modifié selon le protocole précédemment décrit (Brhadda et al., 2000). Dans le cas des plants adultes, les pieds-mères ont été prétraités avec un fongicide plusieurs jours avant le prélèvement des pousses. Ces dernières ont ensuite été essuyées avec du coton imbibé de Tween 20 et lavées, pendant quelques minutes, sous l’eau courante. Les microboutures prélevées ont été trempées pendant trois minutes dans une solution de chlorure de mercure à 677 mg/l contenant quelques gouttes de Tween 20, avant d’être rincées abondamment à l’eau distillée stérile.
2.2. Milieux et conditions de culture
6Les microboutures ayant survécu à l’établissement ont été transférées dans le milieu de base OM (Rugini, 1984) additionné de 30 g/l de saccharose. Cette composition minérale a donné de meilleurs résultats comparativement à d’autres formulations que nous avions préalablement comparées (Brhadda et al., 2003). La zéatine, additionnée en phase de prolifération, a été testée à 0, 1, 5, 10 et 20 mg/l.
7L’induction racinaire a lieu dans un milieu additionné ou non d’auxine. Les auxines comparées sont l’AIB (acide indole-3-butyrique), l’ANA (acide a-naphtalène acétique) et l’AIA (acide indole-3-acétique). Ces régulateurs de croissance ont été testés aux concentrations de 0, 0,5, 1, 2 et 4 mg/l. Les explants ont ensuite été transférés dans un milieu frais dépourvu d’auxines pour favoriser le développement racinaire.
8Les milieux de culture ont été solidifiés par l’agar (7 g/l) et autoclavés, après ajustement du pH à 5,8, pendant 20 minutes à 121 °C. La prolifération et le développement racinaire ont été réalisés à la lumière, sous une photopériode de 16 h, alors que l’incubation des pousses en phase d’induction racinaire a lieu à l’obscurité. La température a été maintenue à 25 ± 2 °C.
2.3. Analyses statistiques
9Un dispositif complètement aléatoire a été adopté. Le test de Newman et Keuls, au seuil de 5 %, a été utilisé pour le classement des moyennes. Les pourcentages 0 et 100 ont subi respectivement la transformation (1/4n) et (1-1/4n), n étant le nombre d’explants mis en culture, et les pourcentages ont subi la transformation arc sin√P avant de procéder à l’analyse de la variance (ANOVA).
3. Résultats et discussion
3.1. Débourrement et développement des pousses
10Une interaction significative (P<0,001) a été notée entre le type d’explant et sa réactivité à la concentration en zéatine utilisée dans le milieu de multiplication. Pour le matériel juvénile, les concentrations de 5 et 10 mg/l ont toutes les deux permis d’obtenir 100 % de débourrement. Une réactivité élevée (91,6 %) des pousses mises en culture a aussi été observée en présence de 1 mg/l de zéatine. Des résultats inférieurs ont été obtenus dans le cas du matériel adulte avec un optimum de débourrement (63 %) atteint dans le milieu contenant 5 mg/l de zéatine. Le débourrement a été très faible en l’absence de cytokinines aussi bien dans le cas du matériel juvénile que dans le cas du matériel adulte (Figure 1).
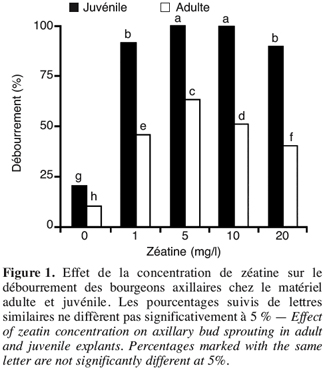
11Le développement des nouvelles pousses a généralement suivi une tendance similaire à celle du débourrement. Les meilleurs résultats ont été obtenus avec 5 mg/l de zéatine pour le matériel juvénile (100 %) et adulte (65 %) (Figure 2). Il est à noter que les explants adultes ont manifesté une callogenèse importante au niveau de leur partie basale.
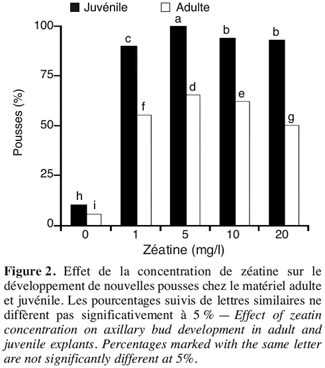
12La cytokinine la plus appropriée pour la micropropagation de l’olivier est la zéatine (Rugini, 1986 ; Mencuccini, 1995 ; Rokba et al., 2000). Dans le cas de la Picholine marocaine, la concentration de 5 mg/l permet de garantir la meilleure réactivité des bourgeons et des pousses du matériel aussi bien pour le matériel juvénile qu’adulte. Les résultats obtenus nous permettent cependant de recommander l’utilisation de la concentration de 1 mg/l et ce pour des raisons économiques. Pour réduire les coûts de production, Leva et al. (2004) ont eux recommandé l’ajout de 2 mg/l de zéatine au milieu de culture, concentration qui a permis d’obtenir des coefficients de multiplication similaires ou supérieurs à ceux observés en présence de la concentration de 4 mg/l citée traditionnellement dans la littérature.
3.2. Enracinement in vitro des microboutures
13Une interaction significative (P<0,001) a été notée entre le type d’explant et sa réactivité au type et à sa concentration d’auxine dans le milieu d’induction racinaire. Le matériel adulte n’a pas développé de racines, quelles que soient l’auxine et la concentration utilisée. Dans le cas du matériel juvénile, l’ANA s’est nettement distinguée des autres auxines testées et l’induction la plus élevée de racines a lieu en présence de 1 mg/l (100 %) et 2 mg/l (94,4 %) (Figure 3). Il est à noter qu’une formation de cals a été observée à la base des microboutures, mais à des degrés différents selon le type et la concentration d’auxine, l’effet étant significatif (P<0,001). L’induction la plus importante de cals caractérise surtout les milieux contenant l’AIA suivi par l’AIB et les concentrations de 4 et 2 mg/l d’auxine (Figure 4).
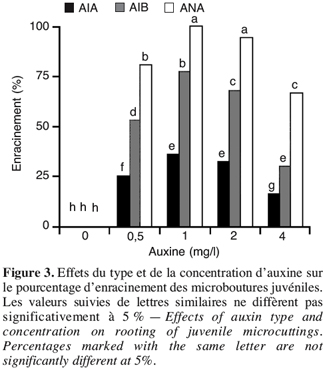
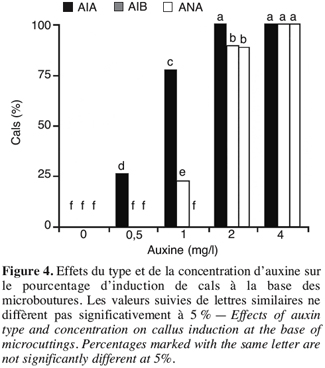
14Rugini (1984) a également rapporté que l’ANA à 1 mg/l est le plus efficace pour l’enracinement (>80 %) des microboutures issues de souquets, de rameaux fructifères ou de pousses non productives des cultivars Frantoio, Moraiolo et Dolce Agogia, tandis que les résultats obtenus avec l’AIB et l’AIA n’étaient pas satisfaisants. Jacoboni (1989) a également rapporté que l’olivier différencie mieux les racines avec l’ANA qu’avec d’autres auxines.
15L’absence d’enracinement dans le cas des explants issus de matériel adulte âgé de 30 ans confirme nos résultats antérieurs obtenus chez l’olivier (Walali, Abousalim, 1993). La difficulté d’enracinement in vitro du matériel adulte est commune à d’autres espèces ligneuses, fruitières et forestières. Le rajeunissement du matériel par divers moyens a été suggéré par plusieurs auteurs en vue d’améliorer sa réactivité in vitro (Howard et al., 1989 ; Franclet, 1979 ; Fouret et al., 1985).
16Les essais menés sur la Picholine marocaine permettent de conclure ce qui suit :
17– pour des raisons économiques, la zéatine à 1 mg/l peut convenablement être utilisée en phase de prolifération des pousses ;
18– l’ANA à 1 mg/l permet de garantir le meilleur enracinement des explants juvéniles ;
19– un rajeunissement et/ou une modification de la composition du milieu de culture s’imposent pour favoriser l’induction racinaire chez le matériel adulte. Des travaux sont en cours pour améliorer la réactivité de ce matériel récalcitrant.
Bibliographie
Brhadda N., Walali LD., Abousalim A., Benali D. (2000). Effet de la température et de l’endosperme sur la dormance et la germination des embryons d’olivier (Olea europaea L.) variété Picholine marocaine. Agronomie 20, p. 643–653.
Brhadda N., Abousalim A., Walali LD. (2003). Effets du milieu de culture et de la lumière sur l’embryogenèse somatique de l’olivier (Olea europaea L.) cv. Picholine marocaine. Fruits 58 (3), p. 167–174.
Bati C., Fodale A., Mulé R., Trombino T. (1999). Trials to increase in vitro rooting of Olea europaea L. cuttings. Acta Hortic. 474, p. 91–94.
Fouret A., Arnaud Y., Larrieu C. (1985). Rajeunissement in vitro de Sequoia sempervirens : effet du nombre et de la fréquence des subcultures, recherche de critères précoces de juvénilité. Ann. Rech. Sylv. 1984, p. 111–137.
Franclet A. (1979). Rajeunissement des arbres adultes en vue de leur propagation végétative. AFOCEL Etud. Rech. 12, p. 3–8.
Howard BH., Jones OP., Vasek J. (1989). Long-term improvement in the rooting of plum cuttings following rejuvenation. J. Hort. Sci. 64 (2), p. 147–156.
Jacoboni A. (1989). Culture in vitro. Olivae 25, p. 31–34.
Leva AR., Petruccelli R., Polsinelli L. (2004). La multiplication végétative in vitro de l’olivier : du laboratoire à la production. Olivae 101, p. 18–26.
Mencuccini M., Micheli M., Standardi A. (1995). Micropropagazione dell’olivo : effetto di alcune citochinine sulla proliferazione. Italus Hortus 4 (6), p. 33–37.
Rokba ZA., Loxou VK., Lionakis SM. (2000). Regeneration of olive (Olea europaea L.) in vitro. COST 843, WG1: Developmental biology of regeneration. 1st meeting, 12–15 oct., Geisenheim, p. 25–26.
Rugini E. (1984). In vitro propagation of some olive (Olea europaea sativa L.) cultivars with different root ability, and medium development using analytical data from developing shoots and embryos. Sci. Hortic. 24, p. 123–134.
Rugini E. (1986). Olive (Olea europaea L.). In Bajajj YPS. (ed). Biotechnology in agriculture and forestry, Vol.1 : Trees. Berlin Heidelberg: Springer-Verlag, p. 253–267.
Rugini E., Lavee S. (1992). Olive. In Hammershlag FA., Litz RE. (eds). Biotechnology of perennial fruit crops, CAB international, p. 371–382.
Walali LD., Abousalim A. (1993). Olive tree propagation. In Tantaoui - El Araki A. (ed.). Proceedings of the first CNCPRST-CSIS seminar on oleaginous plants. October 19-21, Rabat, Morocco, p. 63–67.






