- Accueil
- Volume 14 (2010)
- numéro 2
- Étude des salives de pucerons : un préalable au développement de nouveaux bio-insecticides
Visualisation(s): 5550 (68 ULiège)
Téléchargement(s): 316 (5 ULiège)
Étude des salives de pucerons : un préalable au développement de nouveaux bio-insecticides

Notes de la rédaction
Reçu le 4 juin 2009, accepté le 17 septembre 2009
Résumé
Les pucerons, insectes ravageurs majeurs des forêts, des cultures céréalières, légumières, maraichères, fruitières et ornementales, sont combattus essentiellement avec des insecticides de synthèse. En raison de l'effet nocif de ces derniers sur l'environnement et du développement de populations de pucerons résistants, il est primordial d'adopter des alternatives de lutte. La salive des insectes joue un rôle crucial dans leur alimentation. Elle contient une grande variété de composés dont la spécificité d'action permet de disséquer certains mécanismes physiologiques qui régissent les interactions entre l'insecte et son hôte. Certains composés induisent les défenses de leur hôte et sont considérés comme des outils prometteurs dans la lutte contre les insectes ravageurs. Une des stratégies envisageables repose sur la recherche et la valorisation de substances présentes dans la salive des pucerons. Cette approche a surtout été développée chez les insectes hématophages. L'état des connaissances sur la salive des pucerons est exposé dans cet article en parallèle avec les informations disponibles sur la salive des insectes phytophages broyeurs et des insectes hématophages.
Abstract
Study of aphid saliva: a prerequisite to new bio-insecticides development. Aphids, major insect pests of forests, cereal, vegetable, fruit and ornamental crops, are controlled mainly by synthetic insecticides. However, due to the adverse effects of these ones on the environment and the development of resistant populations of aphids, it is essential to adopt alternative control. Aphid saliva plays a key role during insect feeding. It contains a wide variety of compounds whose specificity of action allows to dissect some physiological mechanisms that govern the interactions between the insect and its host. Some identified compounds were found to induce defences of their host and are therefore considered promising tools in the fight against insect pests. One of the possible strategies is based on research and recovery of substances found in aphid saliva. This approach has been developed especially in hematophagous insects such as mosquitoes. The current state of knowledge about aphid saliva is discussed in this article in parallel with saliva of chewing phytophagous and hematophagous insects.
Table des matières
1. Introduction
1La salive est un liquide biologique sécrété par les glandes salivaires (GS). Chez l'homme, elle est constituée d'eau à 98 % et contient également des électrolytes, du mucus, des composés antibactériens et diverses protéines enzymatiques (Dodds et al., 2005). Elle participe à l'humidification des muqueuses, prépare les aliments à la digestion, possède un rôle antiseptique et constitue une réelle interface avec l'environnement extérieur (Dodds et al., 2005). Depuis plusieurs années se sont développés des projets couplant les techniques de protéomique et de transcriptomique et visant à constituer un véritable catalogue des protéines salivaires humaines (Hu et al., 2006), le but étant d'identifier parmi celles-ci des biomarqueurs de maladies (Xie et al., 2005 ; Baldini et al., 2008). À ce titre, plusieurs protéines se sont révélées être impliquées dans le développement de cancers et de tumeurs, si bien que certains chercheurs avancent que des tests salivaires pourraient, dans le futur, remplacer la traditionnelle prise de sang (Denny et al., 2008 ; Xie et al., 2008).
2La salive des insectes est également au centre des préoccupations scientifiques. Cette matrice est impliquée dans divers processus comme la digestion, l'entretien des pièces buccales, l'équilibre hydrique et la transmission de pathogènes (Musser et al., 2005). Elle peut induire la répulsion des prédateurs des insectes qui la produisent, peut posséder une activité antimicrobienne et peut permettre de contourner les défenses de l'hôte (Musser, 2005).
3Certains insectes phytophages sont munis de pièces buccales piqueuses-suceuses comme les pucerons ou de pièces buccales broyeuses comme les chenilles de Lépidoptères. Ils sont fortement dommageables pour une multitude d'espèces végétales. Depuis 400 millions d'années de coévolution avec les plantes, les insectes ont développé divers mécanismes de résistance pour faire face aux défenses naturelles des plantes (Després et al., 2007). De plus, l'utilisation massive des insecticides a également conduit à la sélection de populations résistantes à ces substances (Davies et al., 2008). Comme la découverte et le développement de nouveaux insecticides chimiques sont désormais en nette diminution, il reste peu d'alternatives pour lutter contre ces insectes. Le constat est le même en ce qui concerne les insectes hématophages (comme les moustiques) dont les effets sont dramatiques sur la santé humaine (Li et al., 2007). Consciente de cette problématique, la communauté scientifique a adopté une stratégie de développement de moyens de lutte biologique. À ce titre, Harmel et al. (2008a) ont résumé ces différents moyens de lutte biologique contre les pucerons. Parmi ces moyens, l'étude de la salive des insectes se révèle être d'une importance capitale autant dans le domaine agronomique que médical avec la recherche et l'identification d'éliciteurs de défenses végétales chez les insectes phytophages et d'allergènes chez les insectes hématophages.
4L'étude de la salive des insectes et l'identification des composés qu'elle contient permettent de comprendre les interactions que ces organismes exercent avec leur hôte. À ce titre, cet article exposera dans un premier temps les avancées réalisées dans l'étude de la salive des insectes hématophages. La salive des insectes phytophages sera ensuite traitée en évoquant les cas des insectes munis de pièces buccales broyeuses et celui des pucerons, insectes qui, bien que phytophages, partagent de nombreux points communs avec les insectes hématophages, notamment au niveau de leur capacité à moduler les réponses de défenses de leur hôte.
2. Salive des insectes hématophages
5De par l'impact négatif que les insectes hématophages exercent sur les vertébrés et le manque de moyens de lutte réellement efficaces, de nombreuses études visent à identifier leurs protéines salivaires. La majorité de ces recherches se sont concentrées sur les moustiques qui constituent un modèle en entomologie médicale. Les femelles exercent des dommages directs par leurs piqûres mais également indirects en véhiculant de nombreux pathogènes transmissibles à l'homme comme le paludisme, parasitose due à un protozoaire du genre Plasmodium transmis par la piqûre de femelles d'Anopheles (Dinglasan et al., 2008). La salive est injectée à plusieurs reprises durant la pénétration des pièces buccales dans la peau de l'hôte jusqu'aux capillaires sanguins. Différents composants salivaires induisent une anesthésie locale et empêchent le sang de coaguler dans la trompe.
6La salive des moustiques contient un mélange de molécules qui inhibent et inactivent différentes composantes de la réponse hémostatique de l'hôte ainsi que les réactions inflammatoires produites par la piqûre pour faciliter l'ingestion de sang. Des composés anticoagulants et antiplaquettaires ainsi que des vasodilatateurs ont été identifiés dans les GS des moustiques. Ces composés accroissent le fitness des moustiques en augmentant la vitesse à laquelle le sang est trouvé et prélevé et en réduisant la probabilité d'être tué par leur hôte pendant qu'ils se nourrissent (Ribeiro et al., 2003). Certains composés affectent également la transmission de parasites par leurs vecteurs et devraient, à terme, servir de cibles pour des vaccins contre ces maladies (Dinglasan et al., 2008). Les GS des moustiques contiennent, entre autres, des enzymes associés à la digestion des sucres (avec les maltases, glucosidases et amylases) (Calvo et al., 2004), du lysozyme qui a un rôle de défense antibactérien (Paskewitz et al., 2008), des endonucléases qui réduisent la viscosité du sang créée par la libération d'acide désoxyribonucléique (ADN) de l'hôte au niveau du site de piqûre (Calvo et al., 2006), des aspyrases et d'autres protéines antiplaquettaires qui inhibent l'agrégation des plaquettes (Champagne et al., 1995 ; Yoshida et al., 2008). Certaines protéines salivaires de moustiques ont un effet négatif sur ce dernier comme, par exemple, les chitinases qui induisent l'élicitation de la réponse inflammatoire des éosinophiles, cellules sanguines ayant un rôle dans le système immunitaire, suivie de la production d'anticorps dans l'hôte (Owhashi et al., 2007).
7La plupart de ces composés salivaires ont été identifiés par des études visant à dresser le transcriptome et le protéome des GS de plusieurs espèces de moustiques adultes femelles. Il a ainsi été possible d'identifier de nouveaux transcrits associés à la nutrition des moustiques et de nouvelles séquences protéiques et peptidiques salivaires potentielles (Valenzuela et al., 2002 ; 2003). Disposer de banques de données contenant de telles séquences est un préalable à l'établissement de profils en protéines salivaires des moustiques, à l'étude de leurs caractéristiques et propriétés, à la vérification de leurs rôles et au développement de stratégies visant à les bloquer. Le rôle de certaines de ces protéines a été étudié en bloquant leur expression par la technique de l'acide ribonucléique interférence (ARNi), technique consistant à introduire un ARN simple ou double brin qui interfère avec un ARN messager spécifique conduisant à sa dégradation et à la diminution de sa traduction en protéine (Boisson et al., 2006).
3. Salive des insectes phytophages
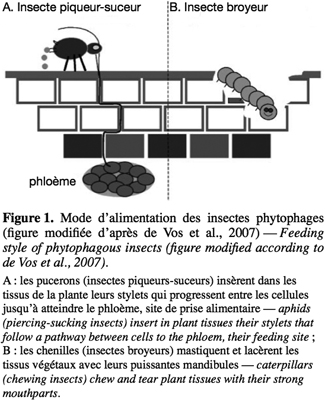
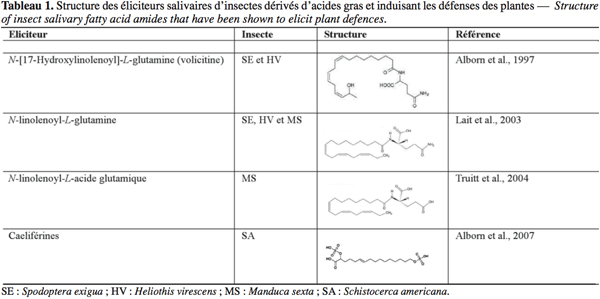
8Les mécanismes de défense de la plante sont enclenchés suite à la perception de deux types de stimuli : l'un est mécanique, il s'agit de la blessure mécanique provoquée par l'insecte phytophage, l'autre est chimique, il s'agit de l'éliciteur présent dans la salive de l'insecte (Walling, 2000). Quand l'insecte se nourrit au détriment d'une plante, il la blesse. L'étendue de cette blessure dépend du régime alimentaire de l'insecte, lui-même fonction du type de pièces buccales de l'insecte. Un insecte piqueur-suceur (comme un puceron), en insérant son stylet dans la feuille, endommage beaucoup moins les tissus du végétal qu'un insecte broyeur (Walling, 2000) (Figure 1). Les éliciteurs sont des composés chimiques capables d'induire des changements physiologiques chez l'organisme vivant visé, une plante dans notre cas (Zhao et al., 2005). De tels composés ont été identifiés dans les sécrétions orales (SO) de plusieurs espèces d'insectes broyeurs (Tableau 1).
3.1. Insectes broyeurs et éliciteurs
9Les éliciteurs identifiés chez les insectes broyeurs appartiennent à deux groupes : celui des dérivés d'acides gras avec les amides de l'acide linolénique – parmi lesquels figurent le N-[17-hydroxylinolenoyl]-L-glutamine (aussi appelé volicitine) (Alborn et al., 1997), le N-linolenoyl-L-glutamine (Lait et al., 2003) et d'autres dérivés de structure très proche – et les caeliférines (Alborn et al., 2007) et celui des composés protéiques avec deux enzymes lytiques – la β-glucosidase (Mattiaci et al., 1995) et la glucose oxydase (GOX) (Eichenseer et al., 1999) – et un peptide, l'inceptine (Schmelz et al., 2007).
10Parmi les amides de l'acide linolénique, la volicitine demeure l'éliciteur le plus étudié. Elle a été pour la première fois isolée des SO de chenilles de Spodoptera exigua (Hübner) (Alborn et al., 1997). Elle active, quand elle entre en contact avec des feuilles endommagées de maïs, la biosynthèse de novo de composés volatils organiques (COV) attractifs pour Cotesia marginiventris (Cresson), une guêpe qui parasite les chenilles phytophages. Ces COV servent ainsi de signal de défense pour les plants de maïs et agissent comme des synomones en ayant un rôle positif aussi bien pour l'espèce émettrice que l'espèce réceptrice (Alborn et al., 1997).
11Les plantes sont capables d'émettre des bouquets de COV spécifiques des chenilles phytophages qui les attaquent et attractifs pour les prédateurs et parasitoïdes de ces derniers (De Moreas et al., 1998 ; Mori et al., 2001). Ainsi, la volicitine et d'autres dérivés d'acides gras présentant une structure très proche de celle-ci ont été identifiés dans les SO d'autres espèces de chenilles de Lépidoptères (Tumlinson et al., 2005) (Tableau 1).
12Une question importante persiste : pourquoi un insecte phytophage produit-il un composé qui induit, chez sa plante hôte, des réponses de défense qui lui sont défavorables ? Spiteller et al. (2000) suggèrent que la volicitine serait produite par la microflore intestinale de l'insecte et fonctionnerait comme surfactant pour faciliter la digestion. Ainsi, la volicitine aurait un rôle dans le métabolisme de l'insecte et la plante l'aurait exploitée à ses propres fins (Gatehouse, 2002).
13Les caeliférines représentent la seule catégorie d'éliciteurs salivaires identifiés chez des insectes phytophages appartenant à un ordre autre que celui des Lépidoptères, à savoir celui des Orthoptères (Alborn et al., 2007) (Tableau 1).
14La β-glucosidase a été isolée des SO des chenilles de Pieris brassicae L. (Mattiaci et al., 1995). Des feuilles de choux blessées mécaniquement et traitées ensuite avec la salive de l'insecte libèrent un bouquet de COV attractifs (synomones) pour Cotesia glomerata L., un parasitoïde de P. brassicae. L'enzyme cliverait les liaisons entre les COV et les sucres, ce qui entrainerait la libération de COV libres.
15Eichenseer et al. (1999) ont identifié la GOX dans les SO de Helicoverpa zea Boddie. Musser et al. (2002) ont montré que des feuilles de tabac blessées mécaniquement et traitées avec de la GOX voyaient leur induction de nicotine significativement réduite en comparaison avec des plants de tabac blessés et traités avec une GOX inactive. Cette nicotine est considérée comme allomone : elle exerce un effet positif pour l'espèce émettrice et négatif pour l'espèce réceptrice. Des résultats similaires ont été obtenus en utilisant des chenilles dont les GS labiales ont été cautérisées (Musser et al., 2006). La GOX induit également une diminution de la transcription de gènes codant pour des enzymes à la base de la voie de biosynthèse des terpénoïdes (synomone) chez le tabac (Bede et al., 2006) et une diminution du contenu des feuilles de tomate en inhibiteurs de trypsine (allomone) (Musser et al., 2005).
16L'inceptine est un peptide retrouvé dans les SO de Spodoptera frugiperda J.E. Smith qui induit l'émission de COV attractifs pour les chenilles néonates de la même espèce par des plants de Vigna unguiculata (L.) Walp. (Schmelz et al., 2007 ; Carrol et al., 2008). Ces COV agissent comme des kairomones en induisant un effet négatif pour l'espèce émettrice et positif pour l'espèce réceptrice. La GOX et l'inceptine sont deux éliciteurs avec un rôle positif pour l'insecte qui les produit.
3.2. Particularités des pucerons
17Les pucerons sont des ravageurs fortement dommageables pour de nombreuses espèces végétales. Leurs stylets pénètrent l'épiderme de la plante et les cellules du parenchyme pour atteindre les tissus phloémiens et prélever le phloème dont les pucerons se nourrissent. Ils occasionnent des dégâts directs moins marqués que les insectes phytophages munis de pièces buccales broyeuses (Walling, 2000) (Figure 1). Par contre, ils sont responsables de dégâts indirects assez importants en véhiculant des virus phytopathogènes. Le contact entre le puceron et le végétal se fait essentiellement par l'intermédiaire de la salive de l'insecte. Étudier cette matrice permet de décortiquer les évènements qui séparent l'entrée du puceron dans la plante et la prise alimentaire phloémienne.
18Le puceron doit faire face aux propriétés du phloème et aux réactions qui s'y déroulent avec notamment des protéines qui coagulent dans les éléments de vaisseau et dans le stylet du puceron (Tjallingii, 2006). Il semble que la salive aqueuse de l'insecte joue un rôle important pour empêcher cette obstruction. Cette salivation, qui intervient avant toute ingestion de phloème, se ferait en quatre périodes (Figure 2). Durant la première, la salivation gélifiante (1) forme un manchon de salive autour des stylets du puceron entre les cellules des tissus végétaux pour limiter le contact direct du stylet avec l'apoplaste de la plante. Les trois autres périodes font intervenir une salivation aqueuse tout d'abord pendant les piqûres brèves intracellulaires (2), ensuite dans les vaisseaux du phloème (3) et enfin à partir de la sève déjà ingérée (4) (Tjallingii, 2006).

19À ce jour, aucun éliciteur n'a été identifié dans la salive des pucerons. Cependant, plusieurs indices montrent que ces ravageurs sont capables d'induire et de manipuler les défenses de leur hôte. Par exemple, des plants de pomme de terre infestés par des pucerons, des insectes broyeurs ou blessés mécaniquement libèrent des bouquets de COV différents et présentent des profils en oxylipines différents (Harmel et al., 2007 ; Gosset et al., 2009). Les pucerons minimisent la réponse à la blessure normalement induite par les insectes broyeurs (Thompson et al., 2006). Face aux pucerons, la plante induit l'expression de gènes inefficaces comme moyen de défense (les gènes régulés par le salicylate) et inactive l'expression de gènes efficaces comme moyen de défense (les gènes régulés par le jasmonate) (Zhu-Salzman et al., 2005). À l'opposé de cette manipulation des défenses végétales, les pucerons induisent des modifications dans la structure de la paroi cellulaire des plantes, ce qui a pour effet de renforcer les barrières dressées contre les insectes qui sondent les tissus végétaux (Voelckel et al., 2004 ; Qubbaj et al., 2005). Comme les dégâts mécaniques engendrés par les pucerons sont limités, leur salive joue un rôle prépondérant dans ces phénomènes.
20Les protéines de la salive des pucerons sont de deux types : structurelles et enzymatiques. Les protéines structurelles interviennent dans la phase de salivation gélifiante. Les enzymes salivaires sont soit des hydrolases (pectinases, cellulases et oligosaccharases), soit des enzymes d'oxydation et de réduction (phénol oxydase, glucose oxydase et peroxydases) (Tableau 2).
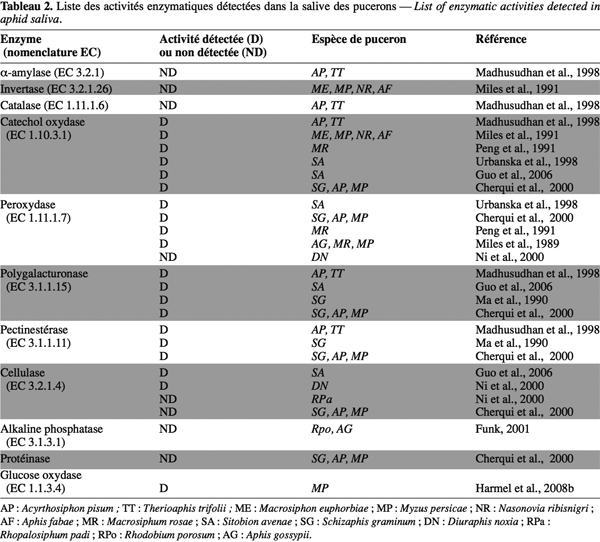
21Les phénoloxydases oxyderaient les polyphénols de la plante en quinones. La pénétration du stylet du puceron dans la plante cause l'accumulation de ces polyphénols et surtout de la catéchine, certainement comme réaction de défense de la plante. On ne sait cependant pas quel avantage tire le puceron de cette excrétion de phénoloxydase. Certains suggèrent une détoxication des phénols (Cherqui et al., 2000). Comme il semble qu'il n'y ait pas d'ingestion substantielle de fluides de la plante pendant la formation de salive gélifiante (salive dans laquelle on observe cette activité), cette explication est discutable (Cherqui et al., 2000). La peroxydase, une autre oxydoréductase, utilise le H2O2 (une des formes activées de l'oxygène) pour oxyder les phénols et d'autres dérivés aromatiques (Urbanska et al., 1998).
22Il a été suggéré que les pectinestérases et les polygalacturonases avaient une importance majeure lors de la pénétration du stylet entre les cellules en dissolvant la pectine de lamelle médiane. Par microscopie électronique en transmission, il a été montré que les stylets suivaient les parois secondaires des cellules en pénétrant entre les couches de cellulose et non via la lamelle. Les pectinases pourraient dégrader les substances pectiques entre les fibres de cellulose et hémicellulose mais le stylet semble aller plus vite que ce que permet l'activité. Les pectinases pourraient conduire à des fragments de pectines qui pourraient agir comme éliciteurs (Cherqui et al., 2000). Les pectines sont des polymères de polysaccharides acides. Plusieurs poly- et oligosaccharides (comme la chitine et le chitosan) et leurs fragments (comme les chitooligosaccharides) sont connus comme éliciteurs chez Phytophtora sojae Kaufmann & Gerd, Phytophthora megasperma Drechsler et Pyricularia oryzae Cavara (Zhao et al., 2005).
23Les enzymes salivaires des pucerons interviennent certainement dans la détoxication des défenses de la plante, leur rôle devant encore être précisé. Il est à noter que, jusqu'ici, nous n'avons parlé que d'enzymes identifiés par leur activité. Un lien hypothétique a été établi entre ces activités enzymatiques et leur effet sur la plante mais aucune étude n'a pu le confirmer. Vérifier l'effet d'un éliciteur salivaire potentiel d'un insecte broyeur se fait en appliquant ce composé sur une blessure mécanique occasionnée par l'expérimentateur à une plante. Comme l'insecte broyeur occasionne naturellement de telles blessures, aucun biais n'est introduit dans l'étude. Il n'en est pas de même pour étudier l'effet d'un composé salivaire de pucerons sur les défenses des plantes où l'effet d'une même blessure mécanique sur les défenses des plantes masquerait celui du puceron (Zhu-Salzman et al., 2005).
24À ce jour, seules deux études ont permis d'associer une fonction à une protéine salivaire de puceron. Will et al. (2007) ont montré que deux protéines salivaires du puceron Megoura viciae Buckton avaient la capacité d'empêcher in vitro l'occlusion des tubes criblés (TC) du tissu phloémien de plants de fève en modifiant la conformation des forisomes. Les forisomes sont des inclusions protéiques dont la conformation passe d'un état contracté (en-dessous d'un seuil de concentration en calcium) qui obstrue les TC à un état dispersé (au-dessus d'un seuil de concentration en calcium) qui n'obstrue pas les TC. Ces protéines salivaires possèdent des domaines de liaison au calcium. La deuxième expérience a montré que, une fois la traduction de la protéine salivaire C002 fortement diminuée par ARNi, le puceron Acyrthosiphon pisum Harris passait beaucoup moins de temps en contact avec le phloème et que sa durée de vie était réduite de 8 jours (Mutti et al., 2006 ; 2008).
25On en est à peine à comprendre comment le puceron manipule les défenses de la plante. C'est pourquoi les efforts actuels se concentrent sur la caractérisation de la salive des pucerons aux niveaux du transcriptome et du protéome. L'établissement d'une banque de marqueurs de séquences exprimées (préalable au séquençage et à l'annotation du génome) de GS du puceron A. pisum a conduit à l'identification de plusieurs transcripts. Parmi ceux-ci, il s'est révélé que la protéine C002 codée par le transcrit le plus abondant dans les GS d'A. pisum était nécessaire à la survie du puceron (Mutti et al., 2006 ; 2008). La constitution de telles banques de données est également à la base de l'identification des protéines salivaires des pucerons Myzus persicae Sulzer (Harmel et al., 2008b) et A. pisum (Carolan et al., 2009). Ces deux études ont permis d’identifier une enzyme de conversion de l'angiotensine (métalloprotéase M2), une métalloprotéase M1, un marqueur de sénescence 30 (régucalcine) et une glucose-méthanol-choline-oxydoréductase dans la salive de A. pisum (Carolan et al., 2009) et une glucose oxydase, une glucose déhydrogénase, une NADH déhydrogénase, une α-glucosidase et une α-amylase dans la salive de M. persicae (Harmel et al., 2008b).
4. Salives et insectes piqueurs : de nouveaux enjeux
26La majorité de nos connaissances sur les protéines salivaires d'insectes proviennent de moustiques. La constitution de banques d'ADNc de leurs GS a conduit à l'identification de protéines qui ont un rôle majeur pour l'insecte. Bien que les moustiques soient hématophages, ils présentent des similarités dans leur mode de nutrition avec les pucerons. Ces sérieux ectoparasites ont développé des stratégies leur permettant de traverser la peau de leur hôte et de prélever son sang. Les moustiques injectent dans leur hôte une salive qui permet de moduler les réponses immunitaires et de favoriser l'ingestion de sang grâce à des anticoagulants, des vasodilatateurs, des inhibiteurs d'agrégation des plaquettes (Valenzuela et al., 2002). La stratégie des pucerons, insectes également munis de pièces buccales de type piqueur-suceur en est proche. La comparaison ne s'arrête pas là : les dégâts directs provoqués par le moustique et le puceron sont limités (pertes de sang et de sève, respectivement), alors que leurs dégâts indirects (transmission de pathogènes) sont fortement dommageables pour leur hôte.
27Les travaux portant sur le protéome et le transcriptome des GS de plusieurs espèces de moustiques sont nombreux (Francischetti et al., 2002 ; Valenzuela et al., 2002 ; 2003 ; Ribeiro et al., 2004 ; 2007 ; Arcà et al., 2005 ; 2007 ; Calvo et al., 2008). Rechercher la fonction des protéines salivaires est primordial. Disposer de banques de données contenant des séquences entières de transcrits et de protéines est nécessaire pour associer une fonction à ces protéines, produire des protéines recombinantes d'intérêt, étudier leurs structures et propriétés, les inactiver par ARNi, vérifier leur rôle et développer des stratégies visant à les bloquer. De telles études chez le puceron n'ont été initiées qu'assez récemment. Le fossé qui existe entre les connaissances accumulées sur la salive des moustiques et celles des pucerons est encore important. Les études menées sur moustiques doivent servir de modèle à celles qui doivent être conduites sur pucerons. Ainsi, l'analyse du transcriptome des GS d'individus femelles d'une espèce de moustiques non hématophages a permis d'identifier des protéines de fonction au préalable inconnue comme étant uniquement associées à l'assimilation des sucres (Calvo et al., 2008). La même démarche doit être appliquée à l'étude de SO des pucerons. Parmi les diverses possibilités d'étude, des espèces présentant des comportements alimentaires nuancés doivent être investiguées afin de pouvoir associer des fonctions aux protéines identifiées. Une autre possibilité serait d'étudier le protéome salivaire d'une espèce de puceron en relation avec la plante sur laquelle il est élevé ou encore vérifier si les protéomes salivaires de pucerons asymbiotiques et symbiotiques sont identiques (Harmel et al., en préparation). Enfin, l'utilisation de la technique de l'ARNi permettra de vérifier le rôle des protéines préalablement identifiées pour autant qu'un phénotype visible soit associé à l'inhibition de l'expression de la protéine étudiée (Reeck, communication personnelle).
28Des études récentes portant sur le transcriptome et le protéome de la salive et des GS de pucerons ont permis de se rendre compte que la diversité des protéines salivaires et de leurs cibles était plus élevée que ce l'on ne pensait (Mutti et al., 2006 ; 2008 ; Will et al., 2007 ; Harmel et al., 2008b ; Carolan et al., 2009). La découverte et la compréhension des interactions biochimiques entre les constituants salivaires de l'insecte et les cibles de l'hôte sont donc d'un grand intérêt tant d'un point de vue fondamental qu'appliqué.
29La valorisation des résultats devra être envisagée en tenant compte du rôle bénéfique ou défavorable de l'éliciteur identifié envers la plante. Si le seul éliciteur présent dans la salive du puceron réduit les défenses végétales, il faudra l'inhiber pour lutter contre l'insecte. De la sorte, l'insecte ne parviendra pas à manipuler les défenses de la plante et à les détourner à son avantage. C'est pourquoi connaitre le rôle de l'éliciteur, ses effets sur la plante et les voies métaboliques qu'il induit est primordial. Si un éliciteur induisant positivement les défenses de la plante est identifié, deux approches complémentaires pourront être combinées : l'application d'une formulation de protéines élicitrices des défenses végétales sur les espèces cultivées et la production de variétés végétales transgéniques exprimant la protéine élicitrice de défense après transfert du gène d'intérêt. Dans ce cas, la plante traitée ou exprimant la protéine élicitrice développera les mécanismes de défense végétale et sera protégée préventivement des attaques de ravageurs dans le respect de l'environnement et en toute sécurité pour les organismes non cibles, dont l'homme.
30En outre, compte tenu du fait que certains composés salivaires induisent des défenses naturelles de leur hôte, le développement de bio-insecticides basés sur ce principe semble être une alternative séduisante aux méthodes de contrôle actuellement disponibles.
31Abréviations
32ADN : acide désoxyribonucléique
33ARNi : acide ribonucléique interférence
34COV : composé organique volatile
35GOX : glucose oxydase
36GS : glande salivaire
37SO : sécrétion orale
38Remerciements
39Nicolas Harmel est financé par une bourse des Fonds pour la formation à la Recherche dans l'Industrie et dans l'Agriculture (FRIA).
Bibliographie
Alborn H.T. et al., 1997. An elicitor of plants volatiles from beet armyworm oral secretion. Science, 276(5314), 945-949.
Alborn H.T. et al., 2007. Disulfooxy fatty acids from the American bird grasshopper Schistocerca americana, elicitors of plant volatiles. Proc. Natl Acad. Sci. USA, 104(32), 12976-12981.
Arcà B. et al., 2005. An updated catalogue of salivary gland transcripts in the adult female mosquito, Anopheles gambiae. J. Exp. Biol., 208(20), 3971-3986.
Arcà B. et al., 2007. An insight into the sialome of the adult female mosquito Aedes albopictus. Insect Biochem. Mol. Biol., 37(2), 107-127.
Baldini C. et al., 2008. Proteomic analysis of the saliva: a clue for understanding primary from secondary Sjögren's syndrome? Autoimmunity Rev., 38(1), 42-58.
Bede J.C., Musser R.O., Felton G.W. & Korth K.L., 2006. Caterpillar herbivory and salivary enzymes decrease transcript levels of Medicago truncatula genes encoding early enzymes in terpenoid biosynthesis. Plant Mol. Biol., 60(4), 519-531.
Boisson B. et al., 2006. Gene silencing in mosquito salivary glands by RNAi. FEBS Lett., 580(8), 1988-1992.
Calvo E. et al., 2004. The transcriptome of adult female Anopheles darlingi salivary glands. Insect. Mol. Biol., 13(1), 73-88.
Calvo E. & Ribeiro J.M., 2006. A novel secreted endonuclease from Culex quinquefasciatus salivary glands. J. Exp. Biol., 209(14), 2651-2659.
Calvo E., Pham V.M. & Ribeiro J.M.C., 2008. An insight into the sialotranscriptome of the non-blood feeding Toxorhynchites amboinensis mosquito. Insect Biochem. Mol. Biol., 38(5), 499-507.
Carolan J.C. et al., 2009. The secreted proteome of the pea aphid Acyrthosiphon pisum characterised by mass spectrometry. Proteomics, 9(9), 2457-2467.
Carrol M.J., Schmelz E.A. & Teal P.E.A., 2008. The attraction of Spodoptera frugiperda neonates to cowpea seedlings is mediated by volatiles induced by conspecific herbivory and the elicitor inceptin. J. Chem. Ecol., 34(3), 291-300.
Champagne D.E. et al., 1995. The salivary gland-specific apyrase of the mosquito Aedes aegypti is a member of the 5'-nucleotidase family. Proc. Natl Acad. Sci. USA, 92(3), 694-698.
Cherqui A. & Tjallingii W.F., 2000. Salivary proteins of aphids, a pilot study on identification, separation and immunolocalisation. J. Insect Physiol., 46(8), 1177-1186.
Davies T.G.E., Field L.M., Usherwood P.N.R. & Williamson M.S., 2008. DTT, pyrethrins, pyrethroids and insect sodium channels. IUBMB Life, 59(3), 151-162.
De Moreas C.M. et al., 1998. Herbivore-infested plants selectively attract parasitoids. Nature, 393, 570-573.
Denny P. et al., 2008. The proteomes of human parotid and submandibular/sublingual gland salivas collected as the ductal secretions. Proteome Res., 7(5), 1994-2006.
Després L., David J.P. & Gallet C., 2007. The evolutionary ecology of insect resistance to plant chemicals. Trends Ecol. Evol., 22(6), 298-307.
Dinglasan R.R. & Jacobs-Lorena M., 2008. Flipping the paradigm on malaria transmission-blocking vaccines. Trends Parasitol., 24(8), 364-370.
Dodds M.W.J., Johnson D.A. & Yeh C.K., 2005. Health benefits of saliva: a review. J. Dent., 33(3), 223-233.
Eichenseer H. et al., 1999. Salivary glucose oxidase: multifunctional roles for Helicoverpa zea? Arch. Insect Biochem. Physiol., 42(1), 99-109.
Francischetti I.M. et al., 2002. Towards a catalog for the transcripts and proteins (sialome) from the salivary gland of the malaria vector Anopheles gambiae. J. Exp. Biol., 205(16), 2429-2451.
Funk C.J., 2001. Alkaline phosphatase activity in whitefly salivary glands and saliva. Arch. Insect Biochem. Physiol., 46(4), 165-174.
Gatehouse J.A., 2002. Plant resistance towards insect herbivores: a dynamic interaction. New Phytol., 156(2), 145-169.
Gosset V. et al., 2009. Attacks by a piercing-sucking insect (Myzus persicae Sultzer) or a chewing insect (Leptinotarsa decemlineata Say) on potato plants (Solanum tuberosum L.) induce differential changes in volatile compound release and oxylipin synthesis. J. Exp. Bot., 60(4), 1231-1240.
Guo G.X., Liu Y., Yang J.J. & Ma X.Z., 2006. Identification, activity and function of several salivary enzymes secreted by Macrosiphum avenae. Acta Entomol. Sinica, 49(5), 768-774.
Harmel N. et al., 2007. Role of terpenes from aphid infested potato as indirect defence on Episyrphus balteatus behaviour. Insect Sci., 14(1), 57-63.
Harmel N., Francis F., Haubruge É. & Giordanengo P., 2008a. Physiologie des interactions entre pomme de terre et pucerons : vers une nouvelle stratégie de lutte basée sur les systèmes de défense de la plante. Cah. Agric., 17(14), 395-400.
Harmel N. et al., 2008b. Identification of aphid salivary proteins: a proteomic investigation of Myzus persicae. Insect Mol. Biol., 17(2), 165-174.
Hu S. et al., 2006. Human saliva proteome and transcriptome. J. Dent. Res., 85(12), 1129-1133.
Lait G.C., Alborn H.T., Teal P.E.A. & Tumlinson III J.H., 2003. Rapid biosynthesis of N-linolenoyl-l-glutamine, an elicitor of plant volatiles, by membrane-associated enzyme(s) in Manduca sexta. Proc. Natl Acad. Sci. USA, 100(12), 7027-7032.
Li X., Schuler M.A. & Berenbaum M.R., 2007. Molecular mechanisms of metabolic resistance to synthetic and natural xenobiotics. Annu. Rev. Entomol., 52, 231-253
Ma R., Reese J.C., Black W.C. IV & Bramel-Cox P., 1990. Detection of pectinesterase and polygalacturonase from salivary secretions of living greenbugs, Schizaphis graminum (Homoptera: Aphididae). J. Insect Physiol., 36(7), 507-512.
Madhusudhan V.V. & Miles P.W., 1998. Mobility of salivary components as a possible reason for differences in the responses of alfalfa to the spotted alfalfa aphid and pea aphid. Entomol. Exp. Appl., 86(1), 25-39.
Mattiacci L., Dicke M. & Posthumus M.A., 1995. β-glucosidase: an elicitor of herbivore-induced plant odor that attracts host-searching parasitic wasps. Proc. Natl Acad. Sci. USA, 92(6), 2036-2040.
Miles P.W. & Peng Z., 1989. Studies on the salivary physiology of plant bugs: detoxification of the phytochemicals by the salivary peroxidase of aphids. J. Insect Physiol., 35(11), 865-872.
Miles P.W. & Harrewijn P., 1991. Discharge by aphids of soluble secretions into dietary sources. Entomol. Exp. Appl., 59(2), 123-134.
Mori N., Alborn H.T., Teal P.E.A. & Tumlinson J.H., 2001. Enzymatic decomposition of elicitors of plant volatiles in Heliothis virescens and Helicoverpa zea. J. Insect Physiol., 47(7), 749-757.
Musser R.O., 2005. Insect saliva: an integrative approach. Arch. Insect Biochem. Physiol., 58(2), 53.
Musser R.O. et al., 2002. Herbivory: caterpillar saliva beats plant defences. Nature, 416(6881), 599-600.
Musser R.O. et al., 2005. Evidence that the caterpillar salivary enzyme glucose oxidase provides herbivore offense in Solanaceous plants. Arch. Insect Biochem. Physiol., 58(2), 128-137.
Musser R.O. et al., 2006. Ablation of caterpillar labial salivary glands: technique for determining the role of saliva in insect-plant interactions. J. Chem. Ecol., 32(5), 981-992.
Mutti N.S., Park Y., Reese J.C. & Reeck G.R., 2006. RNAi knockdown of a salivary transcript leading to lethality in the pea aphid, Acyrthosiphon pisum. J. Insect Sci., 6, 38.
Mutti N.S. et al., 2008. A protein from the salivary glands of the pea aphid, Acyrthosiphon pisum, is essential in feeding on a host plant. Proc. Natl Acad. Sci. USA, 105(29), 9965-9969.
Ni X.Z. et al., 2000. Hydrolase and oxido-reductase activities in Diuraphis noxia and Rhopalosiphum padi (Hemiptera: Aphididae). Ann. Entomol. Soc. Am., 93(3), 595-601.
Owhashi M. et al., 2007. Identification of an eosinophil chemotactic factor from anopheline mosquitoes as a chitinase family protein. Parasitol. Res., 102(3), 357-363.
Paskewitz S.M., Li B. & Kajla M.K., 2008. Cloning and molecular characterization of two invertebrate-type lysozymes from Anopheles gambiae. Insect Mol. Biol., 17(3), 217-225.
Peng Z. & Miles P.W., 1991. Oxidases in the gut of an aphid, Macrosiphum rosae (L.) and their relation to dietary phenolics. J. Insect Physiol., 37(10), 779-787.
Qubbaj T., Reineke A. & Zebitz C.P.W., 2005. Molecular interactions between rosy apple aphids, Dysaphis plantaginea, and resistant and susceptible cultivars of its primary host Malus domestica. Entomol. Exp. Appl., 115(1), 145-152.
Ribeiro J.M.C. & Francischetti I.M.B., 2003. Role of arthropod saliva in blood feeding: sialome and post-sialome perspectives. Annu. Rev. Entomol., 48, 73-88.
Ribeiro J.M.C. et al., 2004. An insight into the salivary transcriptome and proteome of the adult female mosquito Culex pipiens quiquefasciatus. Insect Biochem. Mol. Biol., 34(6), 543-563.
Ribeiro J.M.C. et al., 2007. An annotated catalogue of salivary gland transcripts in the adult female mosquito, Aedes aegypti. BMC Genomics, 8(6).
Schmelz E.A. et al., 2007. Cowpea chloroplastic ATP synthase is the source of multiple plant defence elicitors during insect herbivory. Plant Physiol., 144(2), 793-805.
Spiteller D., Dettner K. & Boland W., 2000. Gut bacteria may be involved in interactions between plants, herbivores and their predators: microbial biosynthesis of N-acylglutamine surfactants as elicitors of plant volatiles. Biol. Chem., 381(8), 755-762.
Thompson G.A. & Goggin F.L., 2006. Transcriptomics and functional genomics of plant defence induction by phloem-feeding insects. J. Exp. Bot., 57(4), 755-766.
Tjallingii W.F., 2006. Salivary secretions by aphids interacting with proteins of phloem wound responses. J. Exp. Bot., 57(4), 739-745.
Tumlinson J.H. & Lait C.G., 2005. Biosynthesis of fatty acid amide elicitors of plant volatiles by insect herbivores. Arch. Insect Biochem. Physiol., 58(2), 54-68.
Urbanska A., Tjallingii W.F., Dixon A.F.G. & Leszczynski B., 1998. Phenol oxidising enzymes in the grain aphid's saliva. Entomol. Exp. Appl., 86(2), 197-203.
Valenzuela J.G. et al., 2002. Towards a description of the sialome of the adult female mosquito Aedes aegypti. Insect Biochem. Mol. Biol., 32(9), 1101-1122.
Valenzuela J.G. et al., 2003. Exploring the salivary gland transcriptome and proteome of the Anopheles stephensi mosquito. Insect Biochem. Mol. Biol., 33(7), 717-732.
Voelckel C., Weisser W.W. & Baldwin I.T., 2004. An analysis of plant-aphid interactions by different microarray hybridization strategies. Mol. Ecol., 13(10), 3187-3195.
Walling L.L., 2000. The myriad plant responses to herbivores. J. Plant Growth Regul., 9(19), 195-216.
Will T., Tjallingii W.F., Thönnessen A. & van Bel A.J.E, 2007. Molecular sabotage of plant defense by aphid saliva. Proc. Natl Acad. Sci. USA, 104(25), 10536-10541.
Xie H. et al., 2005. A catalogue of human saliva proteins identified by free flow electrophoresis-based peptide separation and tandem mass spectrometry. Mol. Cell. Proteomics, 4(11), 1826-1830.
Xie H. et al., 2008. Proteomics analysis of cells in whole saliva from oral cancer patients via value-added three-dimensional peptide fractionation and tandem mass spectrometry. Mol. Cell. Proteomics, 7(3), 486-498.
Yoshida S. et al., 2008. Inhibition of collagen-induced platelet aggregation by anopheline antiplatelet protein, a saliva protein from a malaria vector mosquito. Blood, 111(4), 2007-2014.
Zhao J., Davis L.C. & Verpoorte R., 2005. Elicitor signal transduction leading to production of plant secondary metabolites. Biotechnol. Adv., 23(4), 283-333.
Zhu-Salzman K., Bi J.L. & Liu T.X., 2005. Molecular strategies of plant defense and insect counter-defense. Insect Sci., 12(1), 3-15.
Pour citer cet article
A propos de : Nicolas Harmel
Univ. Liège - Gembloux Agro-Bio Tech. Unité d'Entomologie fonctionnelle et évolutive. Passage des Déportés, 2. B-5030 Gembloux (Belgique). E-mail : harmelnico@gmail.com
A propos de : Éric Haubruge
Univ. Liège - Gembloux Agro-Bio Tech. Unité d'Entomologie fonctionnelle et évolutive. Passage des Déportés, 2. B-5030 Gembloux (Belgique).
A propos de : Frédéric Francis
Univ. Liège - Gembloux Agro-Bio Tech. Unité d'Entomologie fonctionnelle et évolutive. Passage des Déportés, 2. B-5030 Gembloux (Belgique).






