- Accueil
- Volume 14 (2010)
- numéro 3
- Essais de culture de quelques champignons lignicoles comestibles de la région de Kinshasa (R.D. Congo) sur divers substrats lignocellulosiques
Visualisation(s): 11428 (85 ULiège)
Téléchargement(s): 481 (7 ULiège)
Essais de culture de quelques champignons lignicoles comestibles de la région de Kinshasa (R.D. Congo) sur divers substrats lignocellulosiques

Notes de la rédaction
Reçu le 29 juillet 2009, accepté le 5 janvier 2010
Résumé
Neuf souches de champignons lignicoles comestibles isolées sur milieu gélosé et testées sur substrats de semis à base de grains de maïs et de sciure de bois et sur substrats de fructification à base de sciure de bois et de tiges de Cyperus papyrus, ont donné des résultats encourageants. Le rendement moyen en sporophores le plus élevé, près de 22 % en poids frais, a été obtenu avec une souche locale de Pleurotus flabellatus sur tiges de C. papyrus. Un rendement moyen de 19 % a été enregistré avec Lentinus squarrosulus sur un substrat à base de sciure de bois. Il s'agit des premières données méthodologiques publiées sur la culture de souches locales de champignons comestibles pour l'Afrique centrale.
Abstract
Cultivation tests for some edible lignicolous mushrooms in the Kinshasa region (D.R. Congo) on different lignocellulosic substrates. Nine strains of edible lignicolous mushrooms isolated on agar medium and tested on spawn substrates of corn grains and sawdust, and on fruiting substrates of sawdust and stems of Cyperus papyrus, gave satisfactory results. The highest average yield in sporophores, of 22% fresh weight, was obtained with a local strain of Pleurotus flabellatus on C. papyrus stems. An average yield of 19% was recorded with Lentinus squarrosulus on sawdust substrates. This constitutes the first publication of methodological data on the cultivation of local strains of edible mushrooms for central Africa.
Table des matières
1. Introduction
1En Afrique centrale, les champignons constituent des produits forestiers non ligneux d'une importance capitale, tant du point de vue nutritionnel qu'économique (Ndoye et al., 2007). Néanmoins, la saisonnalité dans l'apparition des sporophores est un facteur limitant pour leur disponibilité, souvent aléatoire et concentrée sur quelques semaines par an, principalement en saison des pluies. Dès lors, la mise en culture des champignons se révèle être une activité rentable pour les paysans africains. En période de sècheresse, elle permet en effet de fournir des produits frais tout en transformant des déchets agricoles en protéines alimentaires de haute qualité.
2Bien que plus de 300 espèces de champignons comestibles aient été recensées en Afrique tropicale (Zoberi, 1978 ; Rammeloo et al., 1993 ; Boa, 2006), très peu ont pu faire l'objet d'une mise en culture. En effet, beaucoup d'espèces de champignons africains se développent exclusivement en association spécifique avec des végétaux en formant des ectomycorrhizes, alors que d'autres sont inféodées à des termites. Ces espèces forment des relations symbiotiques actuellement encore non reproductibles en laboratoire, rendant ainsi impossible leur mise en culture (Cailleux, 1963 ; Chang et al., 1978 ; 1982 ; Oei, 1993 ; 2003). Notre choix s'est donc orienté vers des espèces saprotrophes lignicoles (Heim et al., 1965 ; Quimio, 1982 ; Quimio et al., 1982 ; Vilela et al., 1982 ; Oei, 2005 ; De Kesel et al., 2008 ; Eyi Ndong et al., 2008), le plus généralement cultivables sur des déchets d'origine agricole ou agro-industrielle largement disponibles en Afrique. À l'instar de quelques chercheurs qui ont pu domestiquer des souches locales (De Kesel et al., 2002 ; 2008; Eyi Ndong et al., 2008), nous avons délibérément opté pour ce type de matériel, contrairement à la plupart des essais de culture initiés en Afrique tropicale depuis plus de 20 ans et qui concernaient généralement des souches importées, souvent couteuses et inadaptées au climat équatorial.
3Le protocole de mise en culture présenté s'inspire des techniques préconisées par Oei (1993, 2003) mises en oeuvre durant plus de dix années à partir de souches locales de champignons lignicoles comestibles. Il permet de valoriser différents déchets lignocellulosiques et présente l'avantage de pouvoir être transposé en milieu paysan sans gros investissement financier.
4À l'exception de la publication des résultats d'essais concluants de production de sclérotes de Lentinus tuber-regium (Fr.) Fr. [= Pleurotus tuber-regium (Rumph. ex Fr.) Singer] (Dibaluka et al., 1992) et d'un essai limité aux cultures mycéliennes (Mosibono et al., 1991), cet article constitue la première note méthodologique relative à la production de champignons comestibles à partir de souches locales en Afrique centrale.
2. Matériel et méthodes
5Une étape préliminaire a consisté à inventorier, auprès des populations locales, les espèces lignicoles comestibles les plus appréciées. Le choix des espèces à cultiver s'est basé sur les résultats d'une enquête ethnomycologique menée sur le site du « Lac de Ma Vallée » (S 04°25'5,24'' E 15°20'0,16'' ; altitude 450 m) non loin de Kinshasa (Dibaluka, 2005). Les spécimens de référence récoltés lors de notre travail ont été déposés à l'Herbier du Jardin botanique national de Belgique (BR).
6Les étapes de la culture des champignons mises en œuvre dans le cadre de notre étude sont détaillées ci-après.
2.1. Préparation de milieux gélosés et obtention de la culture pure (starter)
7L'isolement est réalisé sur milieu gélosé PDA (filtrat de cuisson dans 1 l d'eau déminéralisée de 200 g patate douce + 20 g agar-agar + 20 g dextrose, porté à 1 l) ou SDA (filtrat de cuisson dans 1 l d'eau déminéralisée de 18 g son de riz + 18 g agar-agar + 18 g dextrose, porté à 1 l). Le milieu est chauffé pendant environ 15 min jusqu'à dissolution des ingrédients et obtention d'un mélange homogène qui est réparti dans les tubes à essai. Ces derniers sont bouchés avec un tampon d'ouate coiffé d'un morceau de papier aluminium avant d'être stérilisés (120 °C, 15-20 min, pression 1 atm). Après stérilisation, les tubes sont placés en position inclinée afin de maximiser la surface de contact du milieu de culture après refroidissement. La sporulation est obtenue en plaçant dans le goulot du tube à essai contenant le milieu de culture, un morceau de chapeau du champignon fixé à un ruban Parafilm, face hyméniale dirigée vers le milieu de culture. Après 12 h, le morceau de chapeau est enlevé et le tube à essai est rebouché en conditions aseptiques au-dessus de la flamme d'une lampe à alcool. Le tube inoculé est placé dans un incubateur Millipore (32 °C, 48 h) afin d'accélérer la germination des spores, puis incubé (~ 25 °C, 10 j). La culture pure ou starter est ensuite conservée au frigidaire (4° C).
2.2. Culture de semis
8La culture de semis consiste à favoriser le développement du mycélium sur un substrat adéquat et stérile. Le produit obtenu à l'issue de cette opération est appelé « blanc-mère » ou « blanc de semis » et sera utilisé ultérieurement pour ensemencer (larder) le substrat de fructification.
9Préparation du substrat de semis. Deux types de substrats de semis ont été préparés :
10– grains de maïs : trempage (24 h), cuisson (25 min), égouttage et essorage au soleil, ajustement du pH à 7 avec de la chaux éteinte (~ 1 %), répartition du milieu (~ 300 g) dans des bocaux hermétiquement fermés par un tampon d'ouate et un couvercle vissé, stérilisation (120 °C, 1 h, 1 atm),
11– sciure de bois : tamisage (600 g), trempage dans l'eau de cuisson de grains de céréales (1 l) enrichie avec du son de blé (200 g) et du saccharose (10 g), ajustement du pH à 7 avec de la chaux éteinte (~ 10 g), mélange du milieu dans des sachets en plastique thermorésistants ou des bocaux, aération du milieu à l'aide d'une baguette métallique, stérilisation (120 °C, 1 h, 1 atm).
12Inoculation et incubation. L'inoculation du substrat de semis avec du mycélium de la culture pure sur milieu gélosé est réalisée dans des conditions de stricte asepsie, de préférence dans une boite d'inoculation où le matériel de prélèvement et de transfert de l'inoculum est stérilisé grâce à la flamme d'une lampe à alcool. L'incubation des grains de maïs (27°-29 °C, 15 jours) et de la sciure de bois (30 jours) est réalisée à l'obscurité, dans une armoire fermée.
2.3. Culture de fructification
13Préparation du substrat de production. Deux substrats de culture ont été utilisés dans des sacs en plastique :
14– sciure de bois de Milicia excelsa (Welw.) C.C.Berg (Moraceae) (‘kambala'), Entandrophragma spp. (Meliaceae) (‘lifaki'), Oxystigma oxyphyllum (Harms) J.Léonard (Leguminosae) (‘tola rouge') et Terminalia superba Engl. & Diels. (Combretaceae) (‘limba') en mélange, additionnée de différents ingrédients (Tableau 1). La sciure fraiche est mise à tremper puis à fermenter sous bâche pendant deux semaines à un mois, en veillant à la mélanger une fois par semaine. Le remplissage et l'ajout des ingrédients sont réalisés, à la demande, dans des sacs en plastique thermorésistants et doublés (19 x 28 cm et 24 x 38 cm recevant respectivement 500 g et 1 000 g de substrat) puis stérilisés (120 °C, 1 h 30, 1 atm),

15– tiges de Cyperus papyrus L. (Cyperaceae) coupées en morceaux de 20 cm, trempées (24 h), essorées (1 h) puis liées en bottes (~ 12 cm d) avec du fil de nylon. Les bottes sont immergées dans de l'eau bouillante enrichie de 1 % sucre, 1 % chaux éteinte et 10 % son de blé, puis égouttées. Les sachets en plastique thermorésistants doublés sont remplis puis stérilisés (120 °C, 1 h 30, 1 atm).
16Lardage du substrat de production. L'ensemencement ou « lardage » est réalisé en conditions aseptiques dans une boite d'inoculation, à raison de 3 % de blanc de semis par rapport à la masse de substrat. Les sachets sont ensuite fermés hermétiquement à l'aide de bouchons en mousse et d'un anneau en PVC (3 cm de hauteur, 2,5 à 3 cm de diamètre).
17Incubation des cultures. L'incubation a lieu dans une armoire à l'obscurité totale (28 °C, 3-4 semaines). Une uniformisation des conditions d'incubation est assurée par un déplacement aléatoire des sachets de culture à l'intérieur de l'armoire une à deux fois par semaine. L'incubation est maintenue jusqu'à envahissement total du substrat de production par le mycélium et apparition des premiers primordia.
18Induction de la fructification. Les sachets sont déplacés dans des abris-serres dont les murs sont confectionnés à l'aide de nattes et dans lesquels règnent une lumière tamisée, une humidité élevée et des températures modérées (23°-28 °C en journée). Il y a lieu d'éviter le rayonnement solaire direct tout en permettant une bonne circulation de l'air, notamment par le maintien d'un espace d'aération entre les murs et le toit. Le contrôle de l'humidité relative et de la température est réalisé à l'aide d'un hygromètre et d'un thermomètre. L'arrosage du sol, jonché de morceaux de briques, à raison de 2 à 3 fois par jour, permet de garder un taux d'humidité élevé dans l'abri. Un contrôle des moisissures est assuré en pulvérisant le milieu à l'aide de chaux éteinte en solution dans de l'eau. La destruction systématique par le feu des sachets présentant des larves d'insectes permet d'éviter une infestation massive de la champignonnière.
3. Résultats et discussion
3.1. Inventaire
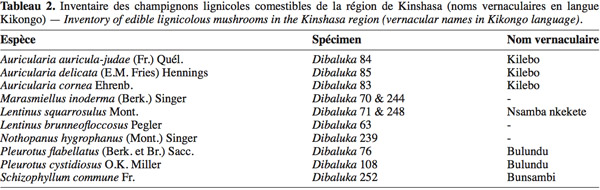
19Dix espèces de champignons lignicoles comestibles ont été inventoriées dans la région de Kinshasa (Tableau 2). Elles appartiennent toutes au cortège classique des espèces saprotrophes, abondantes dans le sous-bois de la forêt dense d'Afrique centrale.
3.2. Mise en culture
20Production de la culture mère. À l'exception des Auricularia, toutes les souches mises en culture à partir de spores ont poussé endéans 48 h après inoculation sur PDA. L'utilisation du SDA permet de ramener la durée d'incubation des spores d'auriculaires à des valeurs proches des autres espèces.
21D'après nos essais préliminaires, le milieu SDA améliorerait également la vitesse de croissance mycélienne par rapport au PDA et ce, quelle que soit l'espèce mise en culture. Ce sont les Lentinus et les Pleurotus qui enregistrent les vitesses de croissance mycélienne les plus élevées, de l'ordre de 0,8 à 0,9 cm par jour sur milieu SDA.
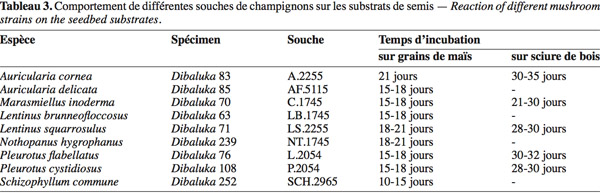
22Production de blanc de semis. Les souches utilisées pour la production de blanc de semis ont été sélectionnées sur base de leur vitesse de croissance mycélienne. Les temps d'incubation varient de 10 à 35 jours (Tableau 3). Le substrat constitué de grains de maïs a permis la conservation à 4 °C du mycélium pendant 2 à 3 mois avec maintien de sa vigueur. Un résultat similaire a été obtenu sur sciure de bois pendant plus de trois mois à température ambiante (~ 25 °C).
23Production des sporophores. Le blanc de semis de neuf souches sélectionnées a été testé sur trois substrats : deux constitués principalement de sciure de bois (S1 et S2) et un à base de tiges de Cyperus papyrus (Cp).
24La vitesse d'envahissement des substrats par le mycélium des différentes espèces était assez uniforme et voisine de 0,5 cm par jour. Une différence notoire a néanmoins été observée avec Marasmiellus inoderma (Berk.) Singer sur C. papyrus (Cp) avec une vitesse de croissance mycélienne proche de 1,5 cm par jour.
25L'apparition des premiers sporophores est observée 3-4 semaines [Pleurotus (Figure 1), Lentinus] à 4-5 semaines [Auricularia (Figure 2)] après l'inoculation des substrats de fructification.


26Les rendements moyens en sporophores (n = 6 répétitions) ont été calculés pour quatre de ces souches. Pour trois des espèces, nous constatons (Tableau 4) que la production des sporophores est nettement plus importante sur le substrat Cp que sur S1 et S2.
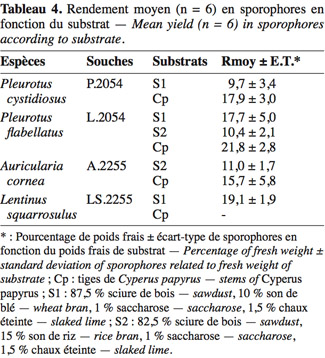
27Sur le substrat Cp, quelle que soit l'espèce mise en culture, les rendements en sporophores avoisinent 15 à 20 %. La souche de Lentinus squarrosulus Mont. testée n'a, par contre, pas fructifié sur ce milieu.
28Des tests préliminaires, dont les résultats ne sont pas repris dans le tableau 4, ont montré également que la souche de Marasmiellus inoderma (C.1745) pouvait croître indifféremment sur sciure de bois et sur tiges de papyrus, alors que les fructifications de Lentinus brunneofloccosus Pegler et de Schizophyllum commune Fr. étaient limitées au substrat Cp avec des rendements de l'ordre de 10 % seulement. Les rendements obtenus avec ces souches doivent encore être validés et feront l'objet de publications ultérieures.
4. Conclusion
29Les résultats que nous avons obtenus sont encourageants car ils démontrent que la culture de souches locales de champignons comestibles est possible dans la région de Kinshasa où les substrats de production sont diversifiés et disponibles en suffisance.
30En Afrique centrale, la culture de champignons devrait trouver sa place dans un système agricole de type intégré qui permettrait de valoriser, comme substrat de culture, les déchets lignocellulosiques produits au niveau de la ferme. Après la récolte des sporophores, le substrat épuisé pourrait être recyclé comme nourriture pour le petit élevage ou comme compost pour les jardins villageois.
31La culture de champignons est néanmoins sujette à de nombreuses contraintes et, même si la construction d'une cabane de fructification et la fabrication d'une boite d'inoculation en constituent les principaux investissements, la production stable d'un produit de qualité est la clé de la rentabilité de cette activité.
32Dans le cadre de notre étude, les rendements en sporophores obtenus à partir de souches locales de pleurotes, de lentins et d'auriculaires avoisinent 15 à 20 % et peuvent être considérés comme très satisfaisants (Oei, 2003). Les résultats des tests préliminaires réalisés avec Marasmiellus inoderma rejoignent ceux enregistrés par De Kesel et al. (2008) et De Kesel et al. (2002, ut Gerronema beninensis nom. inval.) qui ont obtenu un rendement de 10 à 20 % sur des rafles de palmier à huile (Elaeis guineensis), soit à peine inférieur à celui de Pleurotus cystidiosus O.K. Mill s.l. Ces auteurs observent néanmoins que l'envahissement des rafles par M. inoderma est beaucoup plus rapide que par Pleurotus spp., un résultat confirmé par nos observations (croissance de 1,5 cm par jour et temps d'incubation inférieur, voir tableau 3). La vitesse de croissance mycélienne n'est cependant pas en rapport direct avec le rendement ou l'efficacité biologique : M. inoderma semble en effet moins efficace que Pleurotus spp. en ce qui concerne la transformation de son substrat en sporophores. Contrairement aux Pleurotus spp. dont la production est homogène, certains sporophores de M. inoderma sont de petite taille et peu charnus et ne sont généralement pas pris en compte dans les calculs de rendement. Même si la phase finale de la culture de cette espèce nécessite des améliorations en terme d'obtention de sporophores de plus grande taille, de facilitation de la récolte et de maximisation de la production, M. inoderma constitue une espèce prometteuse pour la culture low-tech en Afrique tropicale. À l'instar des techniques utilisées au Ghana, où des déchets animaux (de poisson notamment) sont ajoutés au substrat de culture pour obtenir des sporophores de pleurotes plus charnus et plus consistants (Atikpo, 2008), la possibilité d'enrichissement du substrat de fructification de M. inoderma devrait être étudiée.
33Nos efforts doivent maintenant s'orienter vers le maintien en culture des souches qui ont donné de bons résultats. À l'échelle locale, les principaux obstacles à la culture des champignons proviennent de la difficulté à assurer des conditions de stérilité totale du matériel d'inoculation et à éviter le développement de moisissures. La mise en place d'une filière de production et de distribution de blanc de semis sain à partir d'une unité équipée d'un laboratoire devrait être envisagée, si on souhaite promouvoir la culture des champignons en milieu rural en R.D. Congo.
34Remerciements
35Nous tenons à remercier vivement les responsables de la Coopération Technique Belge (CTB) pour avoir mis à notre disposition les moyens financiers qui nous ont permis de mener ces recherches. Nos remerciements vont également aux habitants des villages avoisinant le site du Lac de Ma Vallée, ainsi qu'aux travailleurs et au représentant de la Conférence Épiscopale Nationale du Congo, pour nous avoir accueillis et avoir partagé avec nous leurs connaissances mycologiques.
Bibliographie
Atikpo M., 2008. Sustainable mushroom production in Africa: a case study in Ghana. Afr. J. Biotechnol., 7(3), 249-253.
Boa E., 2006. Produits forestiers non ligneux 17. Champignons comestibles sauvages. Vue d'ensemble sur leurs utilisations et leur importance pour les populations, http://www.fao.org/docrep/009/y5489f/y5489f00.htm, (10.07.09).
Cailleux R., 1963. Où peut-on cultiver le champignon de couche ? Cah. Maboké, 1, 27-30.
Chang S.T. & Hayes A., 1978. The biology and cultivation of edible mushrooms. New York, NY, USA: Academic Press.
Chang S.T. & Quimio T.H., 1982. Tropical mushrooms. Biological nature and cultivation methods. Hong Kong: Chinese University Press.
De Kesel A., Codjia J.-C. & Yorou N.S., 2002. Guide des champignons comestibles du Bénin. Meise, Belgique : Jardin botanique national de Belgique.
De Kesel A., Guelly A.K., Yorou N.S. & Codjia J.-C., 2008. Ethnomycological notes on Marasmiellus inoderma from Benin and Togo (West Africa). Cryptogamie Mycologie, 29(4), 313-319.
Dibaluka M.S. & Muambi S., 1992. Recherche sur la culture des champignons utiles d'Afrique centrale : essai de culture de Lentinus tuberregium (Fr.) Fr. Rev. Méd. Pharm. Afr., 8(2), 45-52.
Dibaluka M.S., 2005. Inventaire des macromycètes de la forêt du Lac de Ma Vallée (Kinshasa) et essai de mise en culture de quelques espèces comestibles. Mémoire inédit : Faculté des Sciences, Université de Kinshasa (R.D. Congo).
Eyi Ndong H., Cognet S., Degreef J. & Bracke C., 2008. Valorisation des champignons comestibles du Gabon : essai de mise en culture d'une souche sauvage locale de Lentinus squarrosulus Mont. In: Vermeulen C. & Doucet J.L., eds. Les premières forêts communautaires du Gabon. Gembloux, Belgique : Faculté universitaire des Sciences agronomiques de Gembloux, 35.
Heim R. & Cailleux R., 1965. Culture industrielle d'une psalliote tropicale dans les régions chaudes. Cah. Maboké, 3, 109-113.
Mosibono E.E., Habari M.H. & Paulus J.J., 1991. Essai de culture mycélienne de quelques champignons comestibles zaïrois sur milieu semi-synthétique. Tropicultura, 9, 138-139.
Ndoye O., Awono A., Preece L. & Toirambe B., 2007. Marchés des produits forestiers non ligneux dans les provinces de l'Équateur et de Bandundu : présentation d'une enquête de terrain. In : Croizer C. & Trefon T., eds. Quel avenir pour les forêts de la République démocratique du Congo ? Bruxelles : Coopération Technique Belge (CTB), 68-70.
Oei P., 1993. La culture des champignons. Guide technique. Amsterdam, Pays-Bas : CTA, TOOL, FGRET.
Oei P., 2003. Mushroom cultivation. 3rd ed. Leiden, The Netherlands: Backhuys Publishers.
Oei P., 2005. La culture des champignons à petite échelle : pleurotes, shiitakes et auriculaires. Wageningen, Pays-Bas : Fondation Agromisa, CTA.
Quimio T.H., 1982. Physiological considerations on Auricularia spp. In: Chang S.T. & Quimio T.H., eds. Tropical mushrooms. Biological nature and cultivation methods. Hong Kong: Chinese University Press.
Quimio T.H. & de Guzman R., 1982. Taxonomy and basidiocarp development of Auricularia. In: Chang S.T. & Quimio T.H., eds. Tropical mushrooms. Biological nature and cultivation methods. Hong Kong: Chinese University Press.
Rammeloo J. & Walleyn R., 1993. The edible fungi of Africa south of the Sahara. A literature survey. Scripta Bot. Belg., 5, 62.
Vilela L.C. & Silverio C.M., 1982. Cultivation of Auricularia on composted sawdust in the Philippines. In: Chang S.T. & Quimio T.H., eds. Tropical mushrooms. Biological nature and cultivation methods. Hong Kong: Chinese University Press.
Zoberi H., 1978. Some edible mushrooms from the tropics. Mushroom Sci., 10(2), 519-536.
Pour citer cet article
A propos de : Simon Dibaluka Mpulusu
Université de Kinshasa. Faculté des Sciences. Département de Biologie. B.P. 190. Kinshasa XI (R.D. Congo).
A propos de : Félicien Lukoki Luyeye
Université de Kinshasa. Faculté des Sciences. Département de Biologie. B.P. 190. Kinshasa XI (R.D. Congo).
A propos de : André De Kesel
Jardin botanique national de Belgique. Domaine de Bouchout. B-1860 Meise (Belgique).
A propos de : Jérôme Degreef
Jardin botanique national de Belgique. Domaine de Bouchout. B-1860 Meise (Belgique). E-mail : degreef@br.fgov.be.






