- Accueil
- Volume 14 (2010)
- numéro spécial 2
- Développement d'un modèle stœchiométrique de la sulfato-réduction par des bactéries sulfato-réductrices en lagunage anaérobie
Visualisation(s): 5647 (27 ULiège)
Téléchargement(s): 0 (0 ULiège)
Développement d'un modèle stœchiométrique de la sulfato-réduction par des bactéries sulfato-réductrices en lagunage anaérobie

Résumé
Un des inconvénients les plus connus de la technique du lagunage est la génération d'odeurs, souvent associées à la présence de sulfure d'hydrogène (H2S), lui-même engendré par le processus de sulfato-réduction. Dans cet article, nous avons construit un modèle stœchiométrique de la sulfato-réduction en proposant des équations équilibrées vis-à-vis des éléments, des électrons, des charges et de l'énergie. Dans notre modèle, le sulfate agit comme accepteur d'électrons et les composés organiques tels le lactate, le propionate, le butyrate, l'éthanol et l'acétate constituent quant à eux des sources de carbone et de donneurs d'électrons. Ce modèle permet de quantifier la production des sulfures et de prévoir la variation de l'alcalinité du milieu pendant le processus de sulfato-réduction.
Abstract
Development of a stoichiometric model of the sulphate-reduction by the sulphate-reducing bacteria in anaerobic lagoons. One of the most known disadvantages of the technique of lagoon is the generation of smells, often associated with the presence of hydrogen sulfide (H2S), itself generated by the process of sulfate-reduction. In this paper, we have built a stoichiometric model of sulfate-reduction by providing balanced equations against the elements, electrons, charge and energy. In our model, sulfate acts as an electron acceptor and organic compounds such as lactate, propionate, butyrate, ethanol and acetate are in turn sources of carbon and electron donors. This model allows to quantify the production of sulfide and predicts the variation of alkalinity during the process of sulfate-reduction.
Table des matières
1. Introduction
1Un des inconvénients régulièrement cités de la technique du lagunage est la production d'odeurs nauséabondes. Si de telles odeurs apparaissent parfois, et dans certains cas de façon très intense, elles ne sont en rien une conséquence inévitable de la technologie du lagunage (Racault, 1997). Les principaux composés responsables des odeurs gênantes sont classés en trois groupes, à savoir : les composés azotés (ammoniac, amines), les composés soufrés (sulfure d'hydrogène, mercaptans) et les composés oxygénés (acides carboxyliques, aldéhydes, cétones) (Martin, 1991). Au niveau des stations d'épuration, les composés les plus présents sont les composés soufrés à hauteur de 80 à 90 %, suivis par les amines, les aldéhydes, les cétones et enfin les acides gras et les composés organiques volatils (Debrieu, 2004). Toutes ces molécules se forment principalement lors des processus biologiques de fermentation. D'après Gloyna (1972), les sulfures se forment en présence des bactéries sulfato-réductrices (BSR) lorsque ces dernières sont dans un milieu appauvri en oxygène et dont le potentiel d'oxydo-réduction se situe entre -100 et -300 mV ; elles catabolisent les sulfates en libérant les sulfures.
2Le sulfate est l'un des anions les plus abondants trouvés dans l'environnement. Il est produit et rejeté dans beaucoup de processus industriels comprenant la production d'huile de table, la fermentation de mélasse, les opérations des tanneries, la production de nourriture, les centrales fonctionnant grâce à la combustion du charbon et le traitement de pulpe et de papier (Austin, 1984 ; Shin et al., 1997). En plus des sources industrielles, le sulfate, la forme la plus oxydée de soufre, est également produit naturellement, par exemple par l'oxydation des minerais de sulfure dans le drainage acide de mine (Hulshoff et al., 1998). Il est également abondant dans l'eau de mer.
3En dépit des grandes quantités de sulfate déchargé dans l'environnement, peu d'attention a été donnée à la réduction du sulfate en raison de son risque environnemental direct relativement bas comparé à d'autres polluants. La pollution liée aux sulfates est cependant un souci car elle peut causer plusieurs effets indirects sur l'environnement (Liamlean et al., 2007). Les quantités excessives de sulfures libérés par le processus de la sulfato-réduction peuvent affecter les approvisionnements publics en eau et constituer une menace pour la santé. Parmi les composés soufrés, le sulfure d'hydrogène (H2S), très nocif, est le plus répandu ; ses effets sur la santé peuvent être mortels à des doses supérieures à 500 ppm (Lens et al., 2000). À cela s'ajoutent des effets sur l'environnement tels que la forte corrosion des ouvrages (Rinzema, 1988), des surconsommations de coagulants pour les procédés d'épuration chimique et la toxicité pour les autres bactéries épuratrices (Koster et al., 1986 ; Widdel, 1988 ; Kalyuzhnyi, 1998a). En 2000, l'arrêt provisoire des lagunes anaérobies a été décidé par l'entreprise responsable de l'exploitation de la station d'épuration par lagunage de Mèze en France à cause des plaintes liées aux problèmes d'odeurs issues des habitations voisines de la station (Paing, 2001).
1.1. Critères pour éviter les problèmes d'odeurs
4Les recommandations existantes pour éviter les problèmes d'odeurs émises par les lagunes anaérobies sont données dans le tableau 1. Ces recommandations concernent les charges organiques admissibles, mais également la concentration en sulfates dans l'influent. D'après Paing (2001), la prise en compte de ces recommandations pour le dimensionnement des lagunes anaérobies permet la prévention des odeurs. D'après Mara et al. (1994), les problèmes d'odeurs liées aux sulfures volatils risquent d'arriver uniquement lors de la procédure de démarrage et en cas de forte surcharge organique. D'après Pescod (1996), le rejet des sulfures par l'influent brut est parfois plus important que celui occasionné par la lagune anaérobie.

5Ces recommandations s'appuient donc plus sur des observations de terrain que sur des mesures réelles de l'activité des bactéries impliquées dans ces processus. La connaissance de l'activité des bactéries sulfato-réductrices dans les lagunes anaérobies permettra d'avoir des données quantitatives sur le cycle du soufre et la production d'odeurs. L'étape fondamentale dans la conception des systèmes de traitement biologiques est le bilan massique (Rittman et al., 2001).
6Dans cet article, nous avons construit un modèle stœchiométrique de la sulfato-réduction par les BSR par équilibration des éléments, électrons, charges et énergies. Notre approche intègre les facteurs de contrôle de la croissance des BSR et la relation entre cette croissance avec du matériel que les cellules consomment et produisent. Nous serons en mesure de prévoir la quantité de sulfure d'hydrogène produit en fonction des substrats en contact et des paramètres du milieu tels que la température et le pH.
1.2. Métabolisme des BSR en milieu anaérobie
7En conditions anaérobies, les bactéries sulfato-réductrices utilisent les sulfates comme accepteur final d'électrons pour leur respiration. Ces bactéries sont généralement organotrophes, elles oxydent les composés organiques de faible poids moléculaire et simultanément réduisent les sulfates en sulfures (Lens et al., 1998). Leur métabolisme peut être schématisé par la réaction suivante :
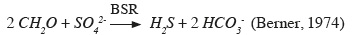
8Divers composés organiques de faible poids moléculaire peuvent servir de donneurs d'électrons. Dans une lagune anaérobie, les donneurs d'électrons couramment utilisés par les grands groupes de sulfato-réduction sont mentionnés dans le tableau 2. Il s'agit de l'acétate, du lactate, du pyruvate, du butyrate, de l'éthanol et de l'hydrogène. Kalyuzhnyi et al. (1998b) ont décrit la séquence des réactions anaérobies où chaque substrat est transformé par les neuf groupes trophiques de bactéries anaérobies (Tableau 2). Parmi ces neuf groupes, nous nous sommes intéressés aux quatre groupes trophiques de bactéries sulfato-réductrices (BSR).

1.3. Répartition du substrat et rendement de conversion cellulaire
9Quand les BSR utilisent un donneur d'électrons pour leur synthèse, une partie des électrons (fe0) est transférée aux sulfates pour fournir l'énergie nécessaire à la conversion de l'autre partie des électrons (fs0) en cellules sulfato-réductrices. Les deux portions d'électrons fe0 et fs0 sont exprimées en électron-équivalents (é-éq) puisque l'énergie de la cellule est générée par des flux d'électrons. Selon Rittman et al. (2001), la somme des fractions d'électrons utilisées pour la production d'énergie et la synthèse sont égales à 1.
10fs0 + fe0 = 1 (1)
11Il est donc essentiel que leur répartition soit exprimée en électron-équivalents. fs0 est égale à é-éq de biomasse produite (Bp) par é-éq de substrat consommé (Sc). La biomasse produite est exprimée en matière volatile en suspension (MVS) et le substrat consommé est exprimé en demande chimique en oxygène (DCO). Dans ce cas, on obtient la formule suivante :
12fs0 = é-éq Bp/ é-éq Sc (2)
13La fraction fs0 peut être convertie en unité massique, gramme de Bp (exprimé en MVS) par gramme de Sc (exprimé en DCO) et vice-versa. Quand la fraction fs0 est exprimée en unité massique, il est appelé rendement de conversion cellulaire (Y).
14Y = gBp/gSc (3)
15En admettant la formule empirique de la biomasse représentée par C5H7O2N et l'ion ammonium comme source d'azote (Rittman et al., 2001), l'oxydation totale d'une mole de C5H7O2N libère 20 moles d'électrons (20 é-éq) selon la réaction chimique suivante :
16C5H7O2N + 8H2O 5CO2 + NH4+ + 19H+ + 20e-
17La masse molaire de la biomasse (C5H7O2N) est égale à 113 g correspondant à 20 é-éq. Nous savons également que 8 g de DCO correspondent à 1 é-éq de DCO, ce qui implique les relations suivantes :
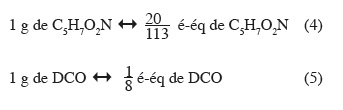
18Pour exprimer fs0 en fonction de « Y », il suffit de remplacer gBp et gSc de l'équation (3) par leur valeur présentée par les relations (4) et (5)
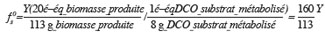
19Donc : fs0 = 1,416 Y (6)
20Le tableau 3 contient des valeurs expérimentales des rendements de conversion de biomasse cellulaire Y pour les principaux groupes de BSR (Kalyuzhnyi, 1998b). Les deux fractions de donneurs d'électrons fs0 et fe0 sont calculées à partir de l'équation (6).

2. Construction de l'équation chimique du métabolisme bactérien
21Selon Rittman et al. (2001), la construction de l'équation chimique du métabolisme bactérien commence par le développement des demi-réactions basées sur un électron-équivalent pour l'accepteur d'électrons (Ra), le donneur d'électrons (Rd) et la formation de cellules (Rc).
2.1. Demi-équations d'oxydo-réduction et de la formation de la cellule
22Réaction d'oxydation des donneurs d'électrons Rd. La construction des équations d'oxydation des substrats donneurs d'électrons constitue une étape importante dans le développement de l'équation globale stœchiométrique pour la croissance des BSR. Pour élaborer la demi-équation d'oxydation du donneur d'électrons, on doit tenir compte du bilan des atomes, des charges et des électrons. L'oxydation totale de composés hydrocarbonés aboutit à la production du CO2. Prenons, par exemple, le cas du butyrate.
23Démarche à suivre :
24– écrire le couple redox :
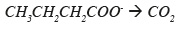
25– équilibrer les atomes de carbone :
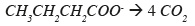
26– équilibrer les atomes d'oxygène en ajoutant des molécules d'eau :
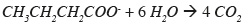
27– équilibrer les atomes d'hydrogène en ajoutant les ions H+ :
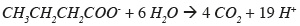
28– équilibrer les charges en ajoutant les électrons :
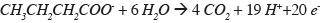
29– écrire la demi-équation d'oxydation pour un électron équivalent du réducteur.
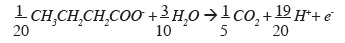
30En milieu anaérobie, le butyrate, le lactate et le propionate sont métabolisés par les BSR jusqu'au stade acétate comme indiqué dans le tableau 3. On tient compte de cet aspect en élaborant les équations stœchiométriques du catabolisme des BSR. Les équations obtenues sont consignées dans le tableau 4.

31Réaction de réduction des sulfates (Ra). La réduction des sulfates conduit à la formation des sulfures, résumés ici au seul H2S :
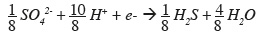
32Réaction de formation des cellules (Rc). Si on admet que la formule empirique des BSR est C5H7O2N avec l'ion ammonium comme source d'azote, nous trouvons l'équation de synthèse suivante :
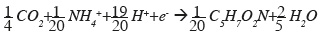
2.2. Réaction globale du métabolisme des BSR
33La réaction globale du métabolisme inclut les processus de production (catabolisme) d'énergie et de synthèse cellulaire (anabolisme). La construction de la réaction globale suit les étapes suivantes :
34– écrire la réaction relative à la production d'énergie (Re) par la cellule à partir du donneur d'électrons (Rd) et de l'accepteur d'électrons (Ra):
35Re = Rd + Ra (7)
36– écrire l'équation relative à la synthèse cellulaire (Rs) à partir du donneur d'électrons Rd et de la formation de la cellule (Rc):
37Rs = Rc+ Rd (8)
38– élaborer la réaction globale (R) à partir des équations (7) et (8) :
39R = fe0Re + fs0Rs (9)
40En substituant Re et Rs par leurs valeurs et en tenant compte de l'équation (1), l'équation (9) devient :
41R = fe0Ra + fs0Rc - Rd (10)
42Conventionnellement, la stœchiométrie du métabolisme cellulaire est établie en considérant la quantité de réactifs nécessaire à la production d'une mole de biomasse. Compte tenu de l'équation (10), nous avons construit le modèle stœchiométrique de la sulfato-réduction des principaux groupes des bactéries sulfato-réductrices en milieu anaérobie (Tableau 5). La validation des coefficients du modèle a été réalisée en vérifiant le bilan de DCO de chaque équation.

2.3. Équations stœchiométriques du métabolisme des principaux groupes des BSR
43Le tableau 3 donne les valeurs expérimentales de Y qui sont souvent utilisées pour la sulfato-réduction. Si nous substituons fs0 du tableau 5 par les valeurs du tableau 3, nous trouvons les équations reprises au tableau 6. À partir de ces équations, nous sommes en mesure de prédire la quantité de sulfure d'hydrogène produite en fonction du substrat et des sulfates disponibles dans le milieu. Nous constatons également une grande consommation de protons, ce qui contribue à augmenter l'alcalinité du milieu. Par ces équations, nous pouvons prévoir la variation de l'alcalinité du milieu dû à l'action des BSR.

3. Conclusion
44Dans cet article, nous avons construit un système d'équations qui modélise la stœchiométrie de la sulfato-réduction des principaux groupes trophiques de BSR en digestion anaérobie. Le modèle est basé sur des équations stœchiométriques équilibrées et des valeurs de rendements de conversion des principales sources d'énergie des BSR disponibles dans la littérature. Notre approche intègre tous les facteurs qui contrôlent la croissance des BSR et les matériels qu'elles consomment et produisent. Le modèle élaboré a été validé par une approche théorique et présente un caractère directement utilisable dans la vie pratique de l'ingénieur, surtout dans la prévention de la production des odeurs par les BSR en fonction des donneurs d'électrons disponibles.
Bibliographie
Austin G.T., 1984. Shreve's chemical process industries. New York, USA: Mcgraw-Hill International Editions.
Berner R.A., 1974. Kinetic models for early diagenesis of nitrogen, sulfur, phosphorus and silicon in anoxic marine sediments. In: Goldberg E.D., ed. The sea. Ideas and observations on the progress in the study of the seas. New York, USA: John Wiley and Sons, 427-450.
Debrieu C., 2004. Lutte contre les odeurs de l'assainissement. Document technique FNDAE n°13. Paris : Fonds National de Développement des Adductions d'Eau (FNDAE).
Gloyna E.F., 1972. Bassins de stabilisation des eaux usées. Génève, Suisse : Organisation Mondiale de la Santé.
Hulshoff L.P., Lens P.N.L., Stams A.J.M. & Lettinga G., 1998. Anaerobic treatment of sulphate-rich wastewaters. Biodegradation, 9, 213-224.
Kalyuzhnyi S.V. & Fedorovich V., 1998a. Mathematical modelling of competition between sulphate reduction and methanogenesis in anaerobic reactors. Bioresour. Technol., 65, 227-242.
Kalyuzhnyi S.V. et al., 1998b. Mathematical modelling as a tool to study population dynamics between sulfate reducing and methanogenic bacteria. Biodegradation, 9, 187-199.
Koster I.W., Lenzima A., de Vegt A.L. & Lettinga G., 1986. Sulfide inhibition of the methanogenic activity of granular sludge at different pH levels. Water Res., 12, 1561-1567.
Lens P.N.L. et al., 1998. Biotechnological treatment of sulfate-rich wastewaters. Crit. Rev. Environ. Sci. Technol., 28(1), 41-88.
Lens P.N.L. & Hulshoff L.P., 2000. Environmental technologies to treat sulphur pollution. Principles and Engineering. London: IWA Publishing.
Liamlean W. & Annachhatre A.P., 2007. Electron donors for biological sulfate reduction. Biotechnol. Adv., 25, 452-463.
Mara D.D. & Will S.W., 1994. Who's afraid of anaerobic ponds? Water Qual. Int., 2, 34-37.
Mara D.D. & Pearson H., 1998. Design manual for waste stabilisation ponds in Mediterranean countries. Leeds, UK: Lagoon Technology International.
Martin G. & Laffort P., 1991. Odeurs et désodorisation dans l'environnement. Paris : Éditions Tec et Doc Lavoisier.
Paing J., 2001. Bilan du carbone et du soufre dans le lagunage anaérobie. Contrôle de l'émission d'H2S pour la réduction des nuisances olfactives. Thèse de doctorat : Université Montpellier I (France).
Pescod M.B., 1996. The role and limitations of anaerobic pond systems. Water Sci. Technol., 33(7), 11-22.
Racault Y., 1997. Le lagunage naturel, les leçons tirées de 15 ans de pratique en France. Antony, France : Cemagref Éditions.
Rinzema A., 1988. Anaerobic treatment of wastewater with high concentrations of lipid or sulphate. PhD thesis: Wageningen Agricultural University (The Netherlands).
Rittman B.E. & McCarty P.L., 2001. Environmental biotechnology. Principles and applications. New York, USA: Mcgraw-Hill International Editions.
Shin H.S, Sae-Eun O. & Chae-Young L., 1997. Influence of sulphur compounds and heavy metals on methanisation of tannery wastewater. Water Sci. Technol., 35(8), 239-245
Widdel F., 1988. Microbiology and ecology of sulphate- and sulphur-reducing bacteria. In: Biology of anaerobic microorganisms. New York, USA: John Wiley and Sons.
Pour citer cet article
A propos de : Casimir Harerimana
Univ. Liège (ULg). Département des Sciences et Gestion de l'Environnement. Unité Assainissement et Environnement. Avenue de Longwy, 185. B-6700 Arlon (Belgique). E-mail : harecasimir@yahoo.fr
A propos de : Besma Harbi
Faculté de Pharmacie. Laboratoire d'Analyse, Traitement et Valorisation des Polluants de l'Environnement et des Produits. Rue Avicenne. TN-5000 Monastir (Tunisie).
A propos de : Jean-Luc Vasel
Univ. Liège (ULg). Département des Sciences et Gestion de l'Environnement. Unité Assainissement et Environnement. Avenue de Longwy, 185. B-6700 Arlon (Belgique).






