- Startpagina tijdschrift
- Volume 15 (2011)
- numéro 4
- Effet du nombre de recyclages de la biomasse de Saccharomyces uvarum sur quelques paramètres de la fermentation primaire au cours de la production de la bière en Côte d'Ivoire
Weergave(s): 5023 (36 ULiège)
Download(s): 255 (1 ULiège)
Effet du nombre de recyclages de la biomasse de Saccharomyces uvarum sur quelques paramètres de la fermentation primaire au cours de la production de la bière en Côte d'Ivoire

Nota's van de redactie
Reçu le 16 novembre 2010, accepté le 7 juin 2011
Résumé
Une étude sur la levure de bière, Saccharomyces uvarum, a été menée afin de déterminer l'impact du nombre de recyclages de la biomasse de cette levure sur certains paramètres de la fermentation primaire et de comprendre la variation des durées de cette fermentation primaire. Le travail a été réalisé avec un total de six cycles de production dont le premier avec la culture initiale de S. uvarum et les cinq autres avec la biomasse de levure recyclée. Après chaque cycle de production de la bière, la biomasse de levure récoltée est réutilisée pour ensemencer un autre moût et la même opération est répétée jusqu'au sixième cycle. Ainsi, au cours de chacun des six cycles de production, plusieurs paramètres tels que la vitesse de fermentation, la durée de réduction du diacétyle, le taux d'alcool, etc. ont été mesurés. Les deux derniers cycles ont les durées de fermentation primaire les plus longues, soit 10 jours et les durées de réduction du diacétyle les plus élevées, 6,8 et 7,6 jours respectivement. Les deux premiers cycles ont les durées de fermentation primaire (8,33 et 8,25 jours respectivement) et de réduction du diacétyle (3,33 jours pour chaque cycle) les plus courtes. Par ailleurs, l'écart entre les atténuations limites théoriques et pratiques varie selon les cycles de production. Ainsi, le dernier cycle présente l'écart le plus élevé, soit 0,51 et le premier, l'écart le plus faible, soit 0,13. La vitesse de fermentation varie de 1,71 à 1,97 °P par jour. La quantité de sucre consommée varie de 8,83 à 10,70 °P et le taux d'alcool de 4,56 à 4,90 °P. Les levures des cinquième et sixième cycles floculent plus rapidement que les autres. Le nombre de cellules en suspension pour ces deux derniers cycles est de 4,2.106 et 4,1.106 cellules.ml-1 contre 25.106 et 20.106 cellules.ml-1 respectivement pour les deux premiers. Les biomasses issues des quatre premiers cycles, qui sont les plus performantes, devraient être utilisées pour la production de la bière, ce qui correspondrait à recycler la levure S. uvarum seulement trois fois au lieu de cinq.
Abstract
Effect of the number of recycled biomass of the yeast Saccharomyces uvarum on some parameters of primary fermentation during beer production in Côte d'Ivoire. A study was conducted on the yeast Saccharomyces uvarum during the production of beer to determine the impact of the number of recycled yeast biomass on some primary fermentation parameters and to understand variations during primary fermentation time. The work was carried out with six cycles of beer production. The first cycle was done with the initial culture of S. uvarum and the five others with its recycled biomass. After each cycle of production, the yeast biomass obtained is re-used to inoculate another mash and the same operation was repeated until the sixth cycle of production of the beer. Thus during each of the six cycles, several parameters such as the rate of fermentation, the diacetyle reduction time, the rate of alcohol production, etc. were measured. The fifth and sixth cycles showed the longest primary fermentation time (10 days) and the longest diacetyle reduction time (6.8 and 7.6 days respectively). The first and second cycles have the shortest primary fermentation time (8.33 and 8.25 days respectively) and diacetyle reduction time (3.33 days for each cycle). The interval between the theoretical and the practical attenuation limit differs according to the cycle of production. The highest gap (0.51) was obtained with the last cycle (sixth) while the shortest was obtained with the first cycle, 0.13. The fermentation rate varied from 1.71 to 1.97°P per day. The quantity of sugar consumed varied from 8.83 to 10.70°P and the rate of alcohol produced from 4.56 to 4.90°P. The yeast from the two last cycles flocculated quicker than the others. The number of cells in suspension for these cycles was 4.1.106 and 4.2.106 cells.ml-1 respectively versus 25.106 and 20.106 cells.ml-1 respectively for the two first cycles. The yeast biomass from the first four cycles should be used for the production of the beer, which would correspond to recycle the yeast S. uvarum only three times instead of five times.
Inhoudstafel
1. Introduction
1La bière est une boisson désaltérante, consommée dans le monde entier et obtenue à partir de certaines céréales, notamment l'orge, le maïs, le riz et le blé, associées à l'eau et au houblon (Caporale et al., 2004). Sa production mondiale dépasse actuellement le milliard d'hectolitres par an (Moll, 1991 ; Boivin, 2005).
2La bière est obtenue par fermentation alcoolique du moût grâce à une levure du genre Saccharomyces (Bartowsky et al., 2004) qui joue un rôle important dans les activités humaines. Elle est en effet utilisée comme modèle d'organisme eucaryote dans de nombreux champs d'expérimentation biologique et génétique et surtout dans de nombreux procédés de fermentation, notamment lors de la préparation de boissons alcoolisées (Fleet et al., 1992; Jolly et al., 2006; Glazer et al., 2007). L'espèce Saccharomyces uvarum, levure de fermentation basse, est utilisée comme agent de fermentation pour la production industrielle de la bière. La fermentation basse se déroule en deux étapes, dont la fermentation primaire et la fermentation secondaire. La fermentation primaire permet la croissance de la levure et donc la transformation des sucres du moût en alcool et la réduction du taux de diacétyle, métabolite secondaire néfaste à la qualité organoleptique de la bière. La fermentation secondaire est l'étape de maturation de la bière. Plusieurs facteurs dont la température et l'état physiologique des levures influencent les durées de fermentation primaire et donc la qualité organoleptique de la bière (Lodolo et al., 2008).
3L'un des problèmes majeurs rencontrés lors de la fabrication de la bière par les brasseries locales ivoiriennes est la variation des durées de fermentation primaire de la levure, variation qui pourrait avoir un impact sur l'homogénéité des produits finis. Cette variation serait liée au nombre de réutilisations de la biomasse de levure, c'est-à-dire au nombre de cycles de production, à la température et à la dose de la levure utilisée. Une fermentation répétée avec des levures recyclées influence la production des composés responsables de la qualité organoleptique de la bière (Pinal et al., 1997). En effet, selon Lodolo et al. (2008), une trop longue durée de fermentation primaire a une conséquence sur l'intégrité du produit fini, c'est-à-dire sur ses caractéristiques organoleptiques et constitue également une perte de temps et une baisse de rentabilité pour l'entreprise (Montague et al., 2008). La durée de fermentation et la levure étant indissociables et déterminant la qualité de la bière, il importe de mieux maitriser ces deux paramètres afin d'obtenir des produits homogènes dans le temps et respectant les normes internationales en matière de qualité. L'objectif de ce travail qui s'inscrit dans ce cadre est donc d'étudier l'effet des différents recyclages successifs de la biomasse de la levure brassicole S. uvarum sur quelques paramètres liés à la qualité de la bière au cours de sa production.
2. Matériel et méthodes
2.1. Matériel
4Le matériel d'étude utilisé au cours de ce travail est constitué de la levure Saccharomyces uvarum (BLV Berlin, Allemagne) et du moût provenant de la salle de brassage d'une brasserie située dans la région de Bouaflé (Côte d'Ivoire) à 380 km d'Abidjan.
2.2. Méthodes
5Propagation de la levure et fermentation du moût. La propagation de la levure lyophilisée a lieu dans une cuve de propagation et permet d'obtenir le ferment. Cette propagation consiste en l'ensemencement de 500 g de levure lyophilisée dans une cuve de propagation contenant 12 hl de moût, ce qui permet l'accroissement de la population de levures jusqu'à une valeur ≥ 7.107 cellules.ml-1. Cette population représente le ferment (culture ou biomasse initiale) qui servira à fermenter le moût.
6Le premier cycle de production de la bière débute avec le transfert de la biomasse initiale de levure de la cuve de propagation dans une cuve de fermentation de 650 hl. Il s'agit d'une fermentation de type fed-batch au cours de laquelle un volume de 610 hl de moût stérile est ajouté et fermenté en trois temps. En effet, à intervalles réguliers de 48 h, sont ajoutés dans la cuve de fermentation 80 hl, 100 hl et 430 hl de moût stérile. Le tout est ensuite laissé fermenter pendant 20 jours. La densité du moût en fermentation est comprise entre 6 et 4 °P (degré Plato) et la fermentation se déroule à 12 °C sous agitation permanente. À la fin de l'étape de la fermentation, le moût fermenté est filtré pour séparer la biomasse de levures du jus de fermentation qui constitue la bière. Cette étape correspond au premier cycle de production (CP1) de la bière.
7Nombres de recyclages de la biomasse de levure et cycles de production de la bière. À la fin du premier cycle de production, la quantité de biomasse récoltée après soutirage de la bière constitue le premier recyclage de la biomasse de levure. Cette biomasse est stockée dans une cuve à levures appelée levurier à peson. Ce levurier permet de connaitre directement la quantité de biomasse de levures obtenue après le soutirage de la bière. Pour le second cycle de production de la bière, cette biomasse est réutilisée pour l'ensemencement d'autres cuves de fermentation, dans les mêmes conditions que celles du premier cycle de production. La biomasse issue du soutirage de la bière après ce second cycle (CP2) de production de la bière constitue ainsi la biomasse recyclée deux fois (2e recyclage de la levure). Ainsi de suite l'on procède de la sorte pour obtenir les biomasses recyclées 3, 4 et 5 fois au cours des 3e, 4e, 5e et 6e cycles de production de la bière (CP3, CP4, CP5 et CP6).
8Échantillonnage. Les prélèvements des différents échantillons sont effectués au démarrage de la fermentation dans les cuves de fermentation et dans le levurier à peson. Ces prélèvements sont réalisés une fois par jour sur toute la période que dure une fermentation c'est-à-dire un cycle de production, soit 20 jours.
9Concernant les prélèvements des échantillons au niveau des cuves de fermentation, une purge d'environ une minute est d'abord effectuée, ce qui permet d'éliminer la levure morte et les matières résiduelles du moût contenues dans le cône de chaque cuve de fermentation. Par la suite, 180 ml sont prélevés dans des conditions aseptiques dans des bouteilles de DURAN stériles et 500 ml dans des bocaux en aluminium, soit au total 680 ml de moût prélevé. Les échantillons de 180 ml servent au dénombrement des populations de levures et au contrôle de leur viabilité, tandis que ceux de 500 ml sont utilisés pour le dosage du diacétyle, pour la détermination de la vitesse de fermentation, la quantité de sucre consommée, le taux d'alcool produit et pour la mesure de l'atténuation limite pratique.
10Concernant le levurier à peson, les prélèvements des échantillons sont réalisés lorsque ce dernier reçoit la biomasse issue des cuves de fermentation. Ainsi, un échantillon de 150 g de biomasse est prélevé dans des bouteilles de DURAN de 200 ml. Les échantillons issus du levurier à peson sont utilisés pour la détermination de la compacité de la levure et de l'atténuation limite théorique.
11Au total, 360 échantillons issus des cuves de fermentation ont été prélevés pour les six cycles de production de la bière (CP1 à CP6), soit 60 échantillons par cycle, tandis que pour le levurier à peson, six échantillons ont été prélevés dont un pour chacune des biomasses issues de chacun des cycles de production. Ces différents échantillons sont directement transportés au laboratoire de la brasserie pour analyse.
12Analyse des échantillons.
13Détermination de la population et du taux de viabilité des levures. Le dénombrement de la population de levures et du taux de viabilité des levures (pourcentage de cellules blanches mesuré par la méthode au bleu de méthylène) a été effectué à l'aide de la cellule de Thoma (hemacymètre) selon la méthode décrite par Cot et al. (2007). Ainsi, dans un tube à essai contenant 2 ml d'eau distillée stérile sont ajoutés 1 ml d'échantillon et quelques gouttes de bleu de méthylène. Le tout est homogénéisé à l'aide d'un agitateur de tubes à essai (Fisher Bioblock, England). Une goutte de la préparation est déposée sur la cellule de Thoma, recouverte d'une lamelle puis laissée reposer pendant quelques secondes pour permettre la stabilisation de la suspension. La lecture s'est faite au microscope optique à l'objectif X40. Le champ du microscope est constitué d'un grand carré composé de 16 petits carrés. Le comptage du nombre de cellules vivantes (incolores) et mortes (bleues) se fait en « U » dans 10 petits carrés de chaque grand carré. La population totale (P) de levures en suspension dans la cuve est donnée par la formule suivante :
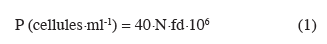
14où N représente le nombre de cellules totales (vivantes et mortes) comptées dans les 10 grands carrés et fd représente le facteur de dilution de l'échantillon (1/3).
15Le taux de cellules blanches (cellules viables et actives) est donné par la formule (2) où C' représente le nombre de cellules vivantes et C le nombre de cellules totales (mortes et vivantes) :

16Les différentes analyses suivantes ont été réalisées selon les méthodes décrites par Manfred (1987) et Benard (2000).
17Détermination de la vitesse de fermentation. La vitesse de fermentation est déterminée par le suivi de la quantité de sucres fermentescibles disponibles dans le moût (densité du moût) au 1er jour et au 4e jour de la fermentation. Pour ce faire, un volume de 100 ml de moût fermenté est filtré sur du papier filtre contenant du Kieselguhr (poudre de diatomée). Le filtrat obtenu est injecté à l'aide d'une seringue dans un saccharimètre (DMA 4500, England). La valeur affichée à l'écran est lue comme étant la quantité de sucres fermentescibles (en °P) disponibles dans le moût. La vitesse de fermentation (Vf) exprimée en degré Plato par jour pendant 4 jours est ensuite calculée selon la formule suivante :
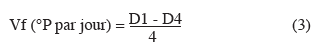
18où D1 (°P) est la valeur de la densité du moût (quantité de sucres fermentescibles) au 1er jour de la fermentation ; D4 (°P) est la valeur de la densité du moût au 4e jour de la fermentation.
19Détermination de la compacité de la levure. La compacité de la levure est déterminée par centrifugation du moût et permet de connaître la consistance de la biomasse de levures. La technique consiste à peser un tube de centrifugation vide sur une balance à précision (Ohauss 117, Germany). La masse obtenue est notée m. Ensuite, 50 g de levure notés M sont mis dans le tube. Le tube est porté à la centrifugeuse (Fisher Bioblock, England) à 6 000 tours.min-1 pendant 10 min. Le surnageant représentant la bière est éliminé. Le tube contenant le culot humide est pesé de nouveau et la valeur obtenue est notée m'. La norme recommandée est comprise entre 60 et 100 %. La compacité notée C et exprimée en % est obtenue par la formule suivante :
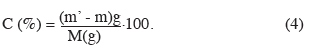
20Détermination de l'écart entre les atténuations limites. L'atténuation limite est la quantité d'extrait (sucres fermentescibles) contenue dans le moût à la fin d'une fermentation. L'atténuation limite théorique correspond à une estimation de la quantité de sucre résiduelle qui doit rester dans le milieu en fin d'une fermentation industrielle (cette estimation se mesure à l'échelle du laboratoire) ; l'atténuation limite pratique est la quantité de sucre résiduelle réellement obtenue en fin de fermentation. Elle permet ainsi de confirmer ou d'infirmer les résultats de l'atténuation limite théorique. L'écart entre les deux atténuations limites permet de savoir si une fermentation est effectivement achevée (Manfred, 1987). Pour une fermentation achevée, l'écart entre ces deux atténuations doit être ≤ 0,4.
21Détermination de l'atténuation limite théorique. Une masse de 60 g de levure utilisée pour une fermentation en cours est pesée sur une balance à précision (Sartorius, France) puis introduite dans un Erlenmeyer propre et stérile de 100 ml contenant 60 ml de moût. L'ensemble est soumis à une agitation pendant 8 h sur un agitateur horizontal (Kibatech, England) à 75 tours.min-1 à une température de 20 °C. Le mélange est filtré avec du Kieselguhr sur du papier filtre. Le filtrat obtenu est injecté au saccharimètre (DMA 4500). La valeur affichée à l'écran est lue comme étant la quantité de sucre résiduelle qui devrait rester dans le milieu en fin de fermentation industrielle, ce qui correspond à l'atténuation limite théorique qui est déterminée pour chaque cycle de production de la bière.
22Détermination de l'atténuation limite pratique. L'atténuation limite pratique est déterminée au cours de la fermentation secondaire lorsque la bière est gardée à 0 °C. Pour ce faire, un volume de 250 ml de bière en garde est filtré avec du Kieselguhr sur du papier filtre. Le filtrat obtenu est injecté au saccharimètre (DMA 4500). La valeur affichée à l'écran est lue comme étant la quantité de sucre résiduelle du milieu en fin de fermentation et correspond à l'atténuation limite pratique.
23Détermination de la quantité de sucre consommée. La quantité de sucre consommée par la biomasse de levure à chaque cycle de production est déterminée par la différence entre la quantité initiale de sucre (°P) contenue dans le moût et celle mesurée à la fin de la fermentation. Un volume de 100 ml de moût est prélevé de la cuve de fermentation avant ensemencement et à la fin de la fermentation primaire. Après homogénéisation, ces volumes de moût sont injectés au saccharimètre (DMA 4500, England). La valeur affichée à l'écran est lue comme étant la quantité de sucre fermentescible contenue dans le moût (°P). La différence entre les valeurs obtenues correspond à la quantité de sucre consommée par la levure.
24Détermination du taux d'alcool. Le taux d'alcool est déterminé à la fin de la fermentation primaire. Un volume de 150 ml de moût fermenté est prélevé à la fin de la fermentation primaire et filtré avec du Kieselguhr sur du papier filtre. Une partie du filtrat obtenu est injecté au saccharimètre (DMA 4500). La valeur affichée à l'écran est lue comme étant la quantité de sucre résiduelle du milieu en fin de fermentation primaire. Cette valeur est appelée extrait réel (ER). Un volume de 1 ml de la seconde partie du filtrat est mis dans un réfractomètre (Bellingham & Stanley LTD, England). La valeur affichée est lue comme l'indice de réfraction (IR) des sucres contenus dans le moût filtré. Les deux valeurs obtenues (ER et IR) permettent de déterminer le taux d'alcool en pourcentage d'alcool par volume (% Vol/Vol).
25Détermination du temps de réduction du taux de diacétyle et de la durée de la fermentation primaire. La détermination du temps de réduction du taux de diacétyle a été réalisée selon la méthode de Sato et al. (1997) au cours du stationnement à chaud qui débute lorsque la densité du moût en fermentation est de 4 °P. Le nombre de jours mis pour atteindre le taux de diacétyle recommandé (0,12 ppm) à partir du début du stationnement à chaud constitue ainsi le temps de réduction du diacétyle qui est alors déterminé au spectrophotomètre (Helios, England) à la longueur d'onde de 335 nm contre un témoin (eau distillée). La durée de fermentation primaire correspond au temps écoulé entre le début de la fermentation et l'atteinte du taux de diacétyle recommandé.
26Analyse statistique
27Les résultats obtenus ont été soumis à une analyse statistique à l'aide du logiciel STATISTICA 7.1. Le test de Duncan a été utilisé pour vérifier si le nombre de recyclages de la biomasse de la levure a une influence sur la durée de fermentation primaire, la vitesse de fermentation, l'écart entre les atténuations limites, la quantité de sucre consommée, le taux d'alcool produit et la réduction du diacétyle. Le niveau de signification est de 0,05.
3. Résultats et discussion
28Le suivi de l'impact du cycle de production, et donc du nombre de recyclages de la biomasse de la levure S. uvarum sur les conditions de la fermentation primaire en brasserie, a permis de montrer qu'il existe une différence significative (P < 0,05) au niveau de la population de levures en suspension pour les différents cycles de production (Tableau 1). Les biomasses de levure utilisées pour les 5e et 6e cycles de production contiennent le nombre le plus faible de cellules en suspension, soit respectivement 4,2.106 et 4,1.106 cellules.ml-1 en moyenne contre 15.106 à 25.106 cellules.ml-1 pour les quatre premiers cycles. Le nombre de levures en suspension le plus élevé (25.106 cellules.ml-1) est obtenu pour le 1er cycle de production (CP1) effectué avec la culture initiale (biomasse non recyclée) de S. uvarum. Ce résultat indique que plus la levure est recyclée, moins elle est performante en termes de reproduction. Un tel résultat laisse supposer que les levures de ces quatre premiers cycles floculent plus facilement en cuve de fermentation. En effet, selon Smukalla et al. (2008) et Reboredo et al. (1996), la floculation est la propriété de certaines espèces de levure à former pendant la fermentation primaire, des flocs de levures contenant plusieurs milliers de cellules. La floculation de levure serait due à l'expression des gènes de floculation (gène FLO) tels que les gènes FLO 1, FLO 5, FLO 8, FLO 9, FLO 10 et FLO 11 (Verstrepen et al., 2003 ; Mulders et al., 2009 ; Soares, 2010). L'expression de ces gènes permet aux cellules floculeuses de libérer à leur surface une protéine adhésive, la lectine ou « flocculin » qui, en se fixant sur des récepteurs situés sur des cellules voisines dans leur champ, forment des flocs (Touhami et al., 2003 ; Nonklang et al., 2009). Sous le poids de la pesanteur, ces flocs sédimentent (Stratford, 1996 ; Smukalla et al., 2008). Toutefois, la floculation des levures est influencée par de nombreux facteurs tels que les conditions nutritives, l'oxygène dissous, le pH, la température, le taux d'alcool, l'état physiologique et génétique des levures, etc. (Stratford, 1996 ; Verstrepen et al., 2003).
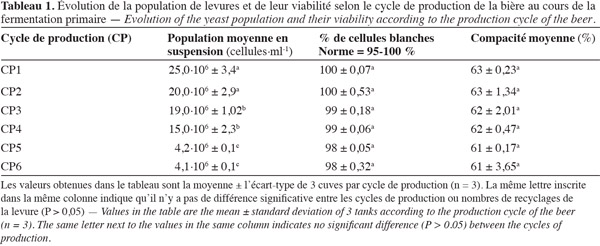
29Cependant, la viabilité des levures, c'est-à-dire le pourcentage de cellules blanches, n'est pas influencée de façon significative (P > 0,05) par le nombre de recyclages de la biomasse de levure. Les valeurs pour ce paramètre se situent entre 98 et 100 % (Tableau 1), respectant ainsi la norme recommandée (95-100 %) (Manfred, 1987). L'homogénéité du pourcentage de cellules blanches (pas de différence significative) (P > 0,05) entre les différents cycles, quel que soit le cycle de production, pourrait être due à une tolérance des levures à l'alcool au cours de la production de la bière. Cette assertion est soutenue par les résultats des travaux de Rupcic et al. (2010) qui ont montré que certains composés tels que les stérols et les acides gras à chaines insaturées sont des éléments qui permettent la protection des biomasses successives de levures actives en maintenant l'intégrité de leur membrane et en augmentant leur résistance à l'éthanol. La compacité des levures n'est également pas influencée par le nombre de recyclages de la biomasse de la levure. En effet, il n'existe pas de différence significative (P > 0,05) entre les différents cycles de production. Les valeurs obtenues pour les différents cycles varient de 61 à 63 %, respectant ainsi les normes en vigueur (Tableau 1). Ce résultat pourrait s'expliquer par le mode de reproduction des levures. En effet, celles-ci se reproduisent par bourgeonnement, c'est-à-dire de la même manière, ce qui conduirait à la production de cellules de même morphologie, d'où les valeurs quasiment identiques de la compacité.
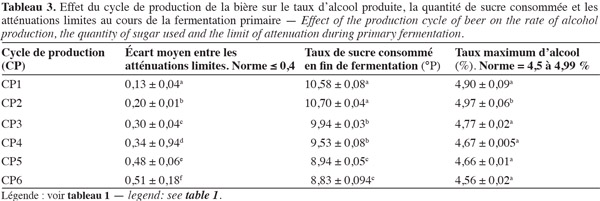
30La vitesse de fermentation, la durée de la fermentation primaire et le temps de réduction du taux de diacétyle sont influencés par le cycle de production et donc le nombre de recyclages de la biomasse de S. uvarum. L'influence des différents cycles de production sur ces paramètres est présentée dans le tableau 2. Les résultats obtenus indiquent que les différents cycles de production ne présentent pas les mêmes vitesses moyennes de fermentation, c'est-à-dire qu'ils n'évoluent pas de la même manière. En effet, ce tableau révèle une différence significative (P < 0,05) entre les différents cycles de production. Toutefois, les trois derniers cycles (CP4, CP5 et CP6) ont la même vitesse moyenne de fermentation, soit 1,76 °P par jour. La vitesse moyenne la plus élevée observée pour le 1er cycle de production est de 1,97 °P par jour. Cependant, toutes les vitesses respectent la norme recommandée (1,6-2 °P par jour). Les vitesses de fermentation traduisant le profil de consommation des sucres du moût (Tableau 3) indiquent que les biomasses de levure qui consomment le plus rapidement les sucres fermentescibles du moût sont celles des 1er (10,58 °P) et 2e (10,70 °P) cycles, qui produisent par ailleurs un peu plus d'alcool, soit 4,90 et 4,97 % respectivement. Il existe une différence significative (P < 0,05) entre la quantité de sucre consommée par les biomasses des différents cycles de production. Si les valeurs du taux d'alcool obtenues pour chaque cycle de production respectent les normes en vigueur (4,5 à 4,99 %), le taux d'alcool le plus élevé enregistré, soit 4,97 %, est obtenu avec les deux premiers cycles. Ces deux cycles semblent contenir les levures consommant le plus de sucre (10,58 et 10,70 °P) et donc les levures les plus vitales. Le 6e cycle de production (CP6) contient les levures qui consomment le moins de sucre (8,83 °P). De tels résultats laissent supposer que la croissance des levures est liée à la vitesse de consommation des sucres.
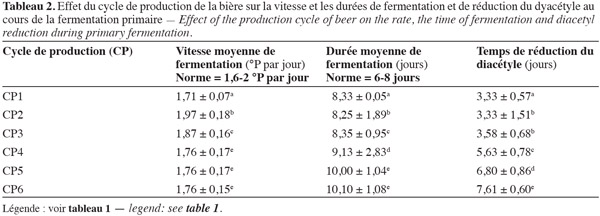
31Les durées moyennes de la fermentation primaire des trois derniers cycles de production de la bière qui sont respectivement de 9,13 jours, 10,00 jours et 10,10 jours sont supérieures à celles des trois premiers cycles (Tableau 2). Les levures de ces trois derniers cycles de production mettent plus de temps (9 à 10 jours) pour réduire le diacétyle jusqu'à la norme recommandée (0,12 ppm). Par ailleurs, les levures des deux premiers cycles de production mettent en moyenne 3 jours pour atteindre la valeur recommandée. Ce résultat s'expliquerait par le fait que les levures de ces cycles mettent plus de temps pour réduire le diacétyle aux valeurs recommandées (≤ 0,12 ppm). Selon Bonciu et al. (2007), la réduction du diacétyle à un taux acceptable est une étape importante dans la limite de la durée de fermentation. Des résultats similaires ont été obtenus par Fichtner et al. (2007) et par Govender et al. (2008) dont les travaux ont montré que les longues durées de fermentation sont généralement dues au nombre de recyclages de la biomasse de levure. La difficulté à réduire le diacétyle par les levures des deux derniers cycles implique également que plus les levures sont recyclées, moins elles sont efficaces. Ainsi, le recyclage des levures les exposerait à de multiples facteurs de stress (conditions nutritives (la source de carbone), l'aération, le pH, la température, le taux d'alcool, etc.).
32L'augmentation de la durée de fermentation pour les deux cycles pourrait s'expliquer par une floculation rapide des levures de ces cycles. En effet, selon Louis-Eugène et al. (2007), la réduction du diacétyle se ferait par une activité enzymatique de la levure. De ce fait, l'atteinte d'un certain seuil dans le temps nécessite une certaine population de levures en suspension. La difficulté qu'ont les levures des deux derniers cycles de production à réduire le diacétyle serait également due à leur vitalité. En effet, selon Rodriguez et al. (2004), la vitalité des levures est due à leur capacité à vaincre ou à s'adapter à un environnement hostile. Il a d'ailleurs été démontré que la vitalité de la levure peut influencer le niveau de nombreux composés tels que les alcools supérieurs et le diacétyle (Guido et al., 2004). Les résultats de nos travaux indiquent donc que les levures des premiers cycles de production, qui sont celles mettant le moins de temps pour réduire le taux de diacétyle, sont plus vitales que celles des derniers cycles.
33Les écarts moyens entre les atténuations limites (quantité de sucres fermentescibles contenue dans le moût à la fin de la fermentation) varient également d'un cycle de production à l'autre (Tableau 3). L'écart moyen le plus élevé (0,51) est obtenu avec le dernier cycle. L'écart le plus petit (0,13) est observé avec le 1er cycle. Ces résultats permettent de montrer le niveau de vitalité des différentes biomasses de levure issues des différents cycles de production de la bière. Dans cette étude, l'écart entre les valeurs de ces atténuations limites est supérieur à la norme recommandée pour les derniers cycles. L'écart permet de mesurer l'aptitude (la vitalité) des levures à utiliser les sucres du moût et à s'adapter au milieu industriel. De tels résultats indiquent que les biomasses des deux derniers cycles ne parviennent pas à dégrader efficacement tout le sucre contenu dans le moût. En effet, selon Benard (2000), la fermentation ou la consommation des sucres est considérée comme achevée lorsque la valeur de l'écart entre les atténuations limite pratique et théorique respecte la norme indiquée (Tableau 3).
34Ainsi, nos résultats pourraient se justifier par le fait que les levures des deux derniers cycles de production s'adaptent difficilement au milieu de fermentation qui leur devient hostile. Une telle interprétation rejoint l'hypothèse selon laquelle le recyclage répété des levures les expose au stress et pourrait occasionner des pertes de certains facteurs pouvant contribuer à la réponse des levures à leur environnement naturel ou aux stress de diverses natures (Sigler et al., 2009). Ces propos sont en phase avec les résultats montrant les longues durées en stationnement à chaud des deux derniers cycles de production et s'expliqueraient par le fait qu'il n'y ait pas de levures en suspension en nombre suffisant pour réduire le taux de diacétyle jusqu'à la norme recommandée. En effet, selon Verbelen et al. (2009), il faut une certaine population de levures en suspension pour réduire convenablement le diacétyle afin que la bière ne soit pas de mauvaise qualité.
4. Conclusion
35Pour améliorer la consistance de la bière produite et maximiser la rentabilité, il serait souhaitable que les brasseries locales utilisent uniquement les quatre premiers cycles de production de la bière, ce qui correspondrait à recycler la levure S. uvarum seulement trois fois au lieu de cinq et obtenir des durées de fermentation respectant les normes. Ces cycles sont ceux dont les valeurs des différents paramètres étudiés, à savoir la compacité, la viabilité, la durée de la fermentation primaire, respectent les normes recommandées.
36Remerciements
37Les auteurs adressent leurs sincères remerciements à la Société de Limonaderie et de Brasserie d'Afrique (SOLIBRA), Bouaflé, Côte d'Ivoire, pour l'assistance technique apportée à cette recherche.
Bibliographie
Bartowsky E.J. & Henschke P.A., 2004. The buttery attribute of wine-diacetyl-desirability, spoilage and beyond. Int. J. Food Microbiol., 96, 235-252.
Benard M., 2000. Determination of repeatability and reproducibility of EBC accepted method: V: Beer submitted on behalf of the analysis committee of the European Brewery Convention. Monatsschr. Brauwiss., 53(5-6), 101-104.
Boivin C., 2005. La bière : son histoire, sa fabrication et sa dégustation. Lac Beauport, Québec, Canada : Éditions Arion.
Bonciu C. & Stoicescu A.G., 2007. Research concerning the use of encapsulated Maturex for beer fermentation. Ann. Univ. Dunarea de Jos of Galati, 4, 82-86.
Caporale G. & Monteleone E., 2004. Influence of information about manufacturing process on beer acceptability. Food Qual. Preference, 15(3), 271-278.
Cot M., Loret M.O., Francois J. & Benbadis L., 2007. Physiological behaviour of Saccharomyces cerevisiae in aerated fed-batch fermentation for high level production of bioethanol. FEMS Yeast Res., 7, 22-32.
Fichtner L., Schulze F. & Braus G.H., 2007. Differential FLO8p-dependent regulation of FLO1 and FLO11 for cell-cell and cell-substrate adherence of S. cerevisiae S288c. Mol. Microbiol., 66, 1276-1289.
Fleet G.H. & Heard G.M., 1992. Growth during fermentation. In: Fleet G.H., ed. Wine microbiology and biotechnology. Newark, NJ, USA: Harwood Academic Publishers, 27-54.
Glazer A.N. & Nikaido H., 2007. Ethanol. In: Microbial biotechnology: fundamentals of applied microbiology. Berkeley, CA, USA: Cambridge University Press, 458-484.
Govender P. et al., 2008. Controlled expression of the dominant flocculation genes FLO1, FLO5 and FLO11 in Saccharomyces cerevisiae. Appl. Environ. Microbiol., 74, 6041-6052.
Guido L.F., Rodriguez C.R., Gonçalves C.R. & Barros A.A., 2004. The impact of physiological condition of the pitching yeast on beer flavour stability: an industrial approach. Food Chem., 87, 187-193.
Jolly N.P., Augustyn O.P.H. & Pretorius I.S., 2006. The role and use of non-Saccharomyces yeasts in wine production. S. Afr. J. Enol. Vitic., 27(1),15-39.
Lodolo E.J., Kock J.L., Axcell B.C. & Brooks M., 2008. The yeast Saccharomyces cerevisiae- the main character in beer brewing. FEMS Yeast Res., 8(7), 1018-1036.
Louis-Eugene S., Ratomahenina R. & Galzy P., 2007. Réduction enzymatique du diacétyle et de l'acétoine par une souche de Saccharomyces uvarum Beijerinck. Z. Allg. Mikrobiol., 24(3), 151-159.
Manfred M., 1987. Analytica-EBC. European Brewery Convention. 4th ed. Zurich, Switzerland: Brauerei-und Getränke-Rundschau.
Moll M., 1991. Bières et couleurs. Cachan, France : Lavoisier, Éditions Tec et Doc.
Montague G.A., Martin E.B. & O'Malley C.J., 2008. Forecasting for fermentation operational decision making. Biotechnol Prog., 24(5),1033-1041.
Mulders S.E.V. et al., 2009. Phenotypic diversity of Flo protein family mediated adhesion in Saccharomyces cerevisiae. FEMS Yeast Res., 9, 178-190.
Nonklang S. et al., 2009. Construction of flocculent Kluyveromyces marxianus strains suitable for high temperature ethanol fermentation. Biosci. Biotechnol. Biochem., 73(5), 1090-1095.
Pinal L., Leden-O.M., Gutierrez H. & Alvarez-Jacobs J., 1997. Fermentation parameter influence higher alcohol production in the tequila process. Biotechnol. Lett., 19(1), 45-47.
Reboredo N.M., Sieiro C., Blanco P. & Villa T.G., 1996. Isolation and characterization of a mutant of Saccharomyces cerevisiae affected in the FL01 locus. FEMS Microbiol. Lett., 137, 57-61.
Rodriguez P. et al., 2004. Vitaltitration: a new method for assessment of yeast vitality. Tech. Q. Master Brew. Assoc. Am., 41, 277-281.
Rupcic J. & Canadi J.G., 2010. Influence of stressful fermentation conditions on neutral lipids of a Saccharomyces cerevisiae brewing strain. World J. Microbiol. Biotechnol., 26(7), 1331-1336.
Sato M. et al., 1997. Winemaking from Koshu variety by the sur lie method: behavior of free amino acids and proteolytic activity in the wine. Am. J. Enol.Vitic., 48, 1-6.
Sigler K., Matoulková D., Dienstbier M. & Gabriel P., 2009. Net effect of wort osmotic pressure on fermentation course, yeast vitality, beer flavor, and haze. Appl. Microbiol. Biotechnol., 6, 1027-1035.
Smukalla S. et al., 2008. Flo1 is a variable green beard gene that drives biofilms-like cooperation in budding yeast. Cell, 135(4), 726-737.
Soares E.V., 2010. Flocculation in Saccharomyces cerevisiae: a review. J. Appl. Microbiol., 110(1), 1-18.
Stratford M.,1996. Induction of flocculation in brewing yeasts by change in pH value. FEMS Microbiol. Lett., 136, 13-18.
Touhami A. et al., 2003. Aggregation of yeast cells: direct measurement of discrete lectin-carbohydrate interactions. Microbiology, 149, 2873-2878.
Verbelen P.J. et al., 2009. Impact of pitching rate on yeast fermentation performance and beer flavour. Appl. Microbiol. Biotechnol., 82(1), 155-167.
Verstrepen K.J., Derdelinckx G., Verachtert H. & Delvaux F.R., 2003. Yeast flocculation: what brewers should know. Appl. Microbiol. Biotechnol., 61, 197-205.
Om dit artikel te citeren:
Over : Arthur Constant Zebre
Université d'Abobo-Adjamé. Laboratoire de Biotechnologie et Microbiologie des Aliments. Unité de Formation et de Recherche des Sciences et Technologies des Aliments (UFR-STA). 02 BP 801. CI-Abidjan 02 (Côte d'Ivoire) – Laboratoire de la Société de Limonaderie et de Brasserie d'Afrique. CI-Bouaflé (Côte d'Ivoire).
Over : Rose Koffi-Nevry
Université d'Abobo-Adjamé. Laboratoire de Biotechnologie et Microbiologie des Aliments. Unité de Formation et de Recherche des Sciences et Technologies des Aliments (UFR-STA). 02 BP 801. CI-Abidjan 02 (Côte d'Ivoire). E-mail : rosenevry2002@yahoo.fr
Over : Marina Koussémon
Université d'Abobo-Adjamé. Laboratoire de Biotechnologie et Microbiologie des Aliments. Unité de Formation et de Recherche des Sciences et Technologies des Aliments (UFR-STA). 02 BP 801. CI-Abidjan 02 (Côte d'Ivoire).
Over : Koné Yacouba
Laboratoire de la Société de Limonaderie et de Brasserie d'Afrique. CI-Bouaflé (Côte d'Ivoire).
Over : Celah Kakou
Université d'Abobo-Adjamé. Laboratoire de Biotechnologie et Microbiologie des Aliments. Unité de Formation et de Recherche des Sciences et Technologies des Aliments (UFR-STA). 02 BP 801. CI-Abidjan 02 (Côte d'Ivoire).






