- Accueil
- volume 16 (2012)
- numéro 3
- Les crèmes végétales : une alternative aux crèmes laitières (synthèse bibliographique)
Visualisation(s): 13779 (113 ULiège)
Téléchargement(s): 1052 (21 ULiège)
Les crèmes végétales : une alternative aux crèmes laitières (synthèse bibliographique)

Notes de la rédaction
Reçu le 3 octobre 2011, accepté le 3 juillet 2012.
Résumé
Les crèmes végétales apparaissent de plus en plus aujourd’hui comme une alternative aux crèmes laitières et ce, pour répondre aux besoins des marchés de plus en plus dynamiques et spécifiques, en termes de fonctionnalités attendues des crèmes. L’objectif de cette synthèse bibliographique est de faire le point sur l’état des connaissances actuelles sur les crèmes, en se focalisant particulièrement sur les crèmes végétales. Les paramètres de formulation et de procédé qui influencent les principales propriétés physico-chimiques des crèmes sont discutés.
Abstract
Vegetal creams: an alternative to dairy creams. A review. Properties expected from creams are changing due to a market becoming increasingly dynamic and specific. Taking this into account, nowadays vegetal creams are increasingly appearing as an interesting alternative to traditional dairy creams to satisfy these needs. The aim of this paper is to give an overview of the current knowledge about creams and, in particular, vegetal creams. Parameters such as formulation and processing, which have a huge impact on the physicochemical properties of creams, are also discussed.
Table des matières
1. Introduction
1Les crèmes laitières sont des produits à plus de 30 % de matière grasse (MG) obtenus par concentration du lait, se présentant sous la forme d’une émulsion de gouttelettes d’huile dans le lait écrémé (Jeantet et al., 2008). Elles peuvent être utilisées pour différentes applications, soit directement comme produit de consommation ou comme matière première en industrie pour la fabrication d’autres produits tels que le beurre, le fromage, les crèmes Chantilly, les sauces, les crèmes glacées, ou encore les nappages et la décoration de gâteaux. Historiquement, la fabrication de la crème laitière remonte à des centaines d’années ; elle s’obtenait dans les crémeries par un processus d’écrémage spontané du lait au repos, du fait de la différence de densité entre les globules gras du lait (ρ = 0,92 g·ml-1) et sa phase aqueuse (ρ ~ 1 g·ml-1). L'invention en 1878 de l'écrémeuse-centrifugeuse par le Suédois Laval et l'Allemand Lefeld a permis d’accélérer le processus de fabrication de la crème et de sa production industrielle. À côté de ces technologies traditionnelles (millénaires ou centenaires) d’obtention de la crème à partir du lait, se sont développées depuis cette dernière décennie, des technologies d’assemblage ou de reconstitution de la crème à partir d’ingrédients laitiers. Ces technologies nouvelles de reconstitution des crèmes laitières présentent des avantages évidents dans les procédés industriels, par rapport à la crème fraiche : faible cout de stockage des matières premières, plus grande flexibilité dans la formulation, indépendance vis-à-vis de la saisonnalité de la composition du lait (Vanderghem et al., 2007 ; Van Lent et al., 2008). Aussi, les crèmes laitières reconstituées peuvent bénéficier de l’image de naturalité généralement attribuée aux produits laitiers (Krause et al., 2007), puisque la réglementation exige pour leur fabrication l’utilisation exclusive d’ingrédients laitiers avec ou non adjonction d’eau potable et les mêmes caractéristiques de produit fini que la crème de lait (Codex Alimentarius, 2007).
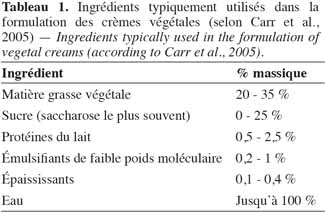
2Le développement du domaine des crèmes laitières reconstituées a ouvert de nouvelles possibilités dans la formulation des crèmes, et plus particulièrement celle de la naissance du concept des crèmes végétales. Les crèmes végétales sont des produits similaires aux crèmes laitières dont la matière grasse laitière (MGL) est remplacée par la matière grasse végétale (MGV) (Codex Alimentarius, codex Stan 192, 1995 ; Carr et al., 2005). L’utilisation d’ingrédients non laitiers dans leur fabrication interdit la dénomination « crèmes laitières » qui est alors remplacée par la dénomination « crèmes végétales ». Elles sont en réalité formulées au départ de quantités bien définies d’eau, de MGV, de protéines laitières ou végétales, de stabilisants, d’épaississants et d’émulsifiants de faibles poids moléculaire. Une formulation type des crèmes végétales est présentée dans le tableau 1 (Carr et al., 2005). À la différence des crèmes laitières, les crèmes végétales offrent plus de possibilités de prise en compte des contraintes technologiques, économiques et nutritionnelles exprimées sur le marché (Berger, 1998 ; Shamsi et al., 2002), ce qui justifie le gain d’intérêt noté autour de ces crèmes, ces dernières années. En effet, la possibilité pour le formulateur de choisir la MG dès le départ dans une large gamme de MGV leur confère un avantage technologique certain : les MGV utilisées seules ou en mélange sont susceptibles de présenter des comportements en cristallisation et en fusion très diversifiés et peuvent de ce fait apporter de nouvelles propriétés dans les fonctionnalités des crèmes (stabilité aux chocs thermiques, aptitude au foisonnement, etc.). Sur le plan financier, la MG butyrique étant plus couteuse que les MGV (facteur 4,5 par exemple en 2006) (Ennifar, 2006 ; Oil World, 2011), son remplacement dans la formulation des crèmes par la MGV permet sans doute de réduire le cout d’un des principaux postes de dépense que constitue la MGL dans les couts des matières premières. En plus des avantages technofonctionnels et économiques, les crèmes végétales peuvent également présenter un intérêt nutritionnel et de santé publique. En effet, un choix adéquat des MGV peut, d’une part, contribuer à un meilleur apport en acides gras (AG) essentiels (amélioration du profil en AG des crèmes) (Lim et al., 2010) et d’autre part, réduire la quantité de cholestérol (Shim et al., 2004). Aussi, les stérols végétaux présents dans les crèmes végétales, connus pour leur effet hypocholestérolémiant, contribuent à la diminution du taux sanguin de cholestérol. Ainsi, tous ces atouts conduisent aujourd’hui aussi bien les chercheurs que les industriels à considérer de plus en plus les crèmes végétales comme une alternative aux crèmes laitières traditionnelles. D’où la réelle nécessité d’une plus grande compréhension ou d’une meilleure maitrise des propriétés physico-chimiques (granulométrie, stabilité, rhéologie, etc.) et technofonctionnelles des crèmes végétales. Ceci passe notamment par une caractérisation fine de ces propriétés du niveau moléculaire au niveau macroscopique.
3Contrairement aux crèmes laitières, très peu de connaissances ont été établies jusqu’à présent sur les crèmes végétales. Cependant, bien qu’elle soit relativement peu abondante, la littérature existante sur les crèmes végétales reste suffisante pour faire l’objet d’une analyse bibliographique. La plupart des travaux recensés à ce sujet portent principalement sur les formulations simplifiées de crèmes végétales produites à partir de MGV de grande consommation (huile de palme, huile de palmiste, huile de colza, huile de tournesol, etc.). Les données recueillies portent également sur les formulations de mix de crèmes glacées qui utilisent la MGV en remplacement de la MGL. Les mix ou encore crèmes primaires servant à la fabrication de crèmes glacées peuvent donc être considérés comme des crèmes végétales au sens où nous l’entendons. Les paramètres physico-chimiques, tels que la granulométrie, la rhéologie, la stabilité et l’aptitude au foisonnement sont les caractéristiques qui intéressent au premier chef les industriels et les chercheurs de ce secteur. C’est pourquoi cette revue se propose de faire le point des connaissances sur les facteurs, tant en relation avec la formulation qu’avec le procédé, qui influencent les propriétés des crèmes végétales, tout en les comparant, quand nécessaire, avec les crèmes laitières.
2. Caractérisation des crèmes végétales
2.1. Granulométrie
4Comme dans toute émulsion, la taille des gouttelettes dispersées (granulométrie) est un paramètre clé de la caractérisation des crèmes car il présente un impact non négligeable, d’une part, sur d’autres propriétés physico-chimiques telles que la rhéologie et la stabilité, et d’autre part, sur les propriétés sensorielles telles la texture et la couleur des crèmes, comme le suggèrent les travaux de McClements (1999). La mesure de la taille des gouttelettes lipidiques présentes dans les crèmes peut s’effectuer à l’aide de différentes techniques telles que la microscopie, la diffraction laser, l’extinction ultrasonique, la rétrodiffusion, etc. La granulométrie laser est la technique la plus répandue car simple, rapide et demandant un volume d’échantillon réduit pour la mesure, mais son inconvénient principal est qu’elle exige une dilution suffisante de l’échantillon pour éviter la diffusion multiple (Canselier et al., 2004). Les facteurs pouvant influencer la granulométrie des crèmes incluent aussi bien les paramètres liés à la formulation que ceux liés au procédé d’émulsification.
5Paramètres liés à la formulation. Les types de MG (triacylglycérols), d'émulsifiant et de stabilisant utilisés dans la formulation des crèmes peuvent présenter des effets sur la distribution et/ou la taille des gouttelettes qui les constituent.
6Effet du type et de la quantité de matière grasse. Des études portant sur des modèles simplifiés de crèmes végétales ont montré que le type de MG et plus particulièrement la composition en AG totaux des triacylglycérols qui la constituent affectent la granulométrie des gouttelettes des crèmes végétales. Ces études impliquent des MGV qui diffèrent tant par leur degré d’insaturation que la longueur des chaines des AG : MGV riche en acide oléique (C18 :1 c9) telles que l’huile de colza ou tournesol oléique, MGV riche en acide laurique (C12 :0) telles que l’huile de palmiste ou de coco, ou encore riche en acide palmitique (C16 :0) telle que l’huile de palme. Ainsi, Sugimoto et al. (2001) ont rapporté, sur base d’un modèle simplifié (40 % MG, 2 % β caséine)1 que la taille moyenne des gouttelettes d’une crème riche en acide oléique est plus grande (1,9 ± 0,1 µm) que celle d’une crème similaire, mais riche en acide laurique (1,6 ± 0,1 µm). Anihouvi (2007) a également montré sur un autre modèle simplifié de crème végétale (30 % de MG, 6,7 % de poudre de babeurre) que la crème à base d’huile laurique présente la taille moyenne des gouttelettes la plus faible (4,7 ±0,1 µm), alors que celle à base d’huile de palme présente une taille intermédiaire (5,4 ± 0,2 µm) et celle contenant l’huile de colza, la taille la plus élevée (5,6 ± 0,1 µm). Ces données montrent que la taille des gouttelettes augmente avec le degré d’insaturation et/ou la longueur des chaines des AG constitutifs des MGV. Ces résultats obtenus sur base de modèles simplifiés confirment ceux de Mutoh et al. (2001) réalisés sur un modèle industriel (40 % de MG, 4 % de poudre de lait écrémé [PLE], 0,5 % de lécithine et 0,2 % d’ester de sucrose) formulé à partir de trois MGV différentes : la première riche en acide oléique, les deux autres étant des graisses lauriques (hydrogénées ou non). Ces résultats ont, par la suite, été confirmés sur des formulations industrielles de mix utilisées dans la fabrication des crèmes glacées (8 % MG, 10 % PLE, 12 % sucrose, 6 % sirop de glucose, 0,3 % mono-diglycérides [MDG]) préparées à partir de différentes MGV : huile de palme raffinée, huile de coco raffinée ou hydrogénée (Granger et al., 2005a).
7Dans les mêmes conditions d’émulsification (quantité d’émulsifiant constante et paramètres opératoires identiques, etc.), la fraction volumique de la MG dans la formulation affecte également les propriétés granulométriques des crèmes végétales comme le suggèrent les travaux de Reiffers-Magnani et al. (1999) et ceux de Floury et al. (2000). En effet, Reiffers-Magnani et al. (1999) ont montré qu’une formulation de crème végétale à base d’huile de soja (40 %) et de poudre de lactosérum (9,8 %) engendre la formation de gouttelettes de taille plus élevée (196 nm) qu’une autre similaire, mais à 20 % de MG (300 nm). Vanderghem et al. (2007) ont fait le même constat sur une crème laitière à 30 ou 20 % de MG.
8Effet du type d’émulsifiant. L’influence du type d’émulsifiant inclut tant les émulsifiants de faible poids moléculaire tels les mono, di-glycérides et phospholipides, que ceux de haut poids moléculaire comme les proteins, ainsi que des interactions protéines/émulsifiants de faible poids moléculaire.
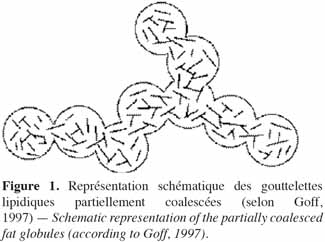
9La littérature rapporte que l’utilisation d’un émulsifiant lipidique sous forme saturée ou partiellement insaturée affecte la taille des gouttelettes des crèmes. En effet, Holstborg et al. (1999) ont montré, sur base d’un modèle simplifié de crèmes végétales (30 % d’huile de soja, 1 % de PLE, 0,5 % de diglycéride [DG]) que la taille moyenne des gouttelettes est plus grande pour la crème à base de DG mono-oléate, en comparaison de la crème à base de DG mono-stéarate. Ces résultats sont similaires à ceux rapportés par Granger et al. (2005a, 2005b) qui ont étudié l’effet de la nature (saturée ou partiellement insaturée) d’un mélange de MDG sur la taille des gouttelettes, en utilisant d’une part un modèle industriel de formulation de crèmes glacées (Granger et al., 2005a) et d’autre part, un modèle simplifié de crèmes végétales (8 % de MG, 10 % de PLE et 0,3 % MDG) (Granger et al., 2005b). Ces auteurs ont montré que les crèmes produites à partir d’un MDG partiellement insaturé donnent des tailles de gouttelettes plus élevées, quel que soit le type de MG utilisé dans la formulation des crèmes (Tableau 2). En effet, la partie hydrophobe des émulsifiants lipidiques adsorbés à l’interface des gouttelettes peut servir de point de nucléation pour la cristallisation des triacylglycérols : les émulsifiants lipidiques contenant des chaines hydrocarbonées saturées sont connus pour être de meilleurs initiateurs de cristallisation, en accélérant plus la nucléation que les insaturés. Des taux de solide de MG supérieurs sont alors généralement observés dans les crèmes contenant des émulsifiants lipidiques saturés (Barfod et al., 1991 ; Euston, 2008), ce qui pourrait limiter, par exemple, une agrégation des gouttelettes par coalescence partielle (Figure 1) et expliquer, au moins en partie, le fait que les crèmes formulées avec ce type d’émulsifiant lipidique présentent des tailles de gouttelettes plus faibles. Enfin, la concentration de l’émulsifiant lipidique influence également la taille des gouttelettes des crèmes. Dans les systèmes stabilisés par des protéines, une concentration très élevée de l’émulsifiant lipidique peut entrainer une forte augmentation de la taille moyenne des gouttelettes, du fait d’une forte agrégation des gouttelettes suite à la désorption des protéines (Holstborg et al., 1999).
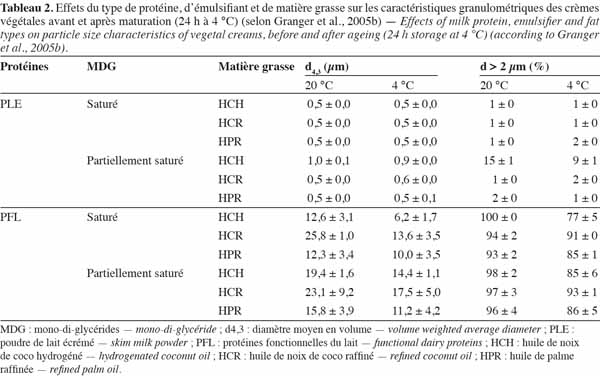
10Le type de protéines utilisées dans la formulation peut également affecter la granulométrie des crèmes. En effet, dans les mêmes conditions d’émulsification, les crèmes à base de sources protéiques riches en caséines, telles la poudre de lait écrémé, présentent en général des diamètres moyens de gouttelettes plus petits que celles à base de sources protéiques riches en protéines de lactosérum, telles que la poudre de lactosérum (Relkin et al., 2003 ; Granger et al., 2005b ; Van Lent et al., 2008). En effet, les travaux de Granger et al. (2005b) ont rapporté sur un modèle simplifié de crèmes végétales (8 % de MG, 10 % de source protéique et 0,3 % MDG), que les crèmes formulées à partir des protéines fonctionnelles du lait (60 % de protéines de lactosérum et 40 % de caséines) présentent des diamètres moyens de gouttelettes beaucoup plus grands que celles formulées à partir de la poudre de lait écrémé (80 % de caséines et 20 % de protéines de lactosérum) (Tableau 2). Cette même tendance a également été observée pour des crèmes végétales (9 % d’huile de palmiste hydrogénée, 1-3,5 % de protéines du lait) formulées selon un modèle industriel à partir d’isolats de caséines (caséinates) ou à base d’isolats de protéines de lactosérum (Relkin et al., 2003 ; Sourdet et al., 2003 ; Relkin et al., 2005). Les différences de granulométrie entre les crèmes préparées à partir des deux sources protéiques (caséines ou protéines de lactosérum) sont liées aux différences de propriétés interfaciales à l’interface huile/eau, les caséines ayant une plus grande capacité d’abaissement de la tension interfaciale que les protéines de lactosérum (Relkin et al., 2003 ; Croguennec et al., 2008). Par ailleurs, la concentration en protéines dans la formulation influence la granulométrie des crèmes. En effet, il a été démontré qu’à fraction massique d’huile constante, la taille des gouttelettes diminue avec la concentration en protéines jusqu’à une certaine concentration au-delà de laquelle la taille varie très peu (Sánchez et al., 2005).
11La présence simultanée des molécules amphiphiles de poids moléculaire faible (surfactif) et élevé (protéines) dans une formulation de crèmes se traduit généralement par une diminution de la taille des gouttelettes au cours de l’émulsification (Holstborg et al., 1999). Par ailleurs, l’adsorption compétitive à l’interface huile/eau entre tensioactifs et protéines conduit généralement au cours de la maturation à une désorption des protéines de la surface des gouttelettes (Davies et al., 2000 ; Granger et al., 2003 ; Granger et al., 2005b), ce qui peut entrainer des modifications granulométriques.
12Effet du type de stabilisant. Les agents stabilisants sont habituellement utilisés dans la formulation des crèmes pour augmenter la viscosité des crèmes et donc leur stabilité, ceci à travers l’augmentation de la viscosité de leur phase aqueuse (Anton et al., 2005). Divers stabilisants (agar, xanthane, carboxyméthylcellulose [CMC], guar, alginate, etc.) sont employés dans la formulation des émulsions H/E (Koupantsis et al., 2009), mais ce sont les carraghénanes qui sont les plus utilisés dans les crèmes, soit seuls (Spagnuolo et al., 2005), soit en mélange avec d’autres hydrocolloïdes (guar, caroube, xanthane, CMC), comme le suggèrent de nombreux travaux de recherche (Shamsi et al., 2002 ; Anton et al., 2005 ; Vega et al., 2005 ; Bazmi et al., 2008).
13Le type d’agent stabilisant utilisé dans la formulation des crèmes végétales peut également avoir un effet sur la granulométrie des crèmes. Surh et al. (2006) ont montré que le type de pectine utilisé dans une crème végétale (10 % d’huile de maïs, 1 % de caséinate de sodium, 0,5 % de pectine) peut modifier la granulométrie en fonction du pH du milieu. Ainsi, à pH 7, les crèmes contenant la pectine faiblement ou fortement méthoxylée ont présenté une taille moyenne et un pourcentage de gouttelettes de taille supérieure à 1 µm, plus élevés que la crème qui ne contient pas de pectine, du fait d’une forte agrégation des gouttelettes. Par contre, à pH 5, la présence de la pectine diminue fortement l’agrégation des gouttelettes, ce qui se traduit par une taille moyenne et un pourcentage de gouttelettes ayant une taille supérieure à 1 µm plus faibles. À ce pH, la pectine acquiert une charge négative et s’adsorbe à la surface des gouttelettes grâce aux interactions électrostatiques qu’elle noue avec les protéines chargées positivement (pH en dessous du point isoélectrique). Cette interaction de la pectine avec les protéines adsorbées à l’interface huile/eau renforce l’épaisseur de la couche protectrice autour des gouttelettes, ce qui accroît les répulsions électrostatiques et stériques et par conséquent, limite leur agrégation (Surh et al., 2006).
14Paramètres liés au procédé d’émulsification et à la maturation
15Effet du procédé d’émulsification. L’émulsification est le procédé qui permet de disperser un fluide sous forme de gouttelettes dans un autre fluide non miscible, via la création d'interfaces. Ceci implique la déformation puis la fragmentation d'une goutte en plusieurs autres gouttes (au moins deux) plus petites. Il existe de nombreuses techniques d'émulsification que l'on regroupe en fonction du régime d'écoulement imposé lors de la fragmentation.
16Le type de procédé d’émulsification, ainsi que les conditions opératoires de l’émulsification, affectent fortement la distribution de taille des gouttelettes des émulsions en général et des crèmes en particulier. Quel que soit le procédé d’émulsification utilisé, la distribution de taille, de même que la taille moyenne des gouttelettes des crèmes, dépendent fortement de la durée de résidence de la crème dans la zone d’émulsification, de l’énergie mise en œuvre pendant l’émulsification ainsi que de la géométrie (design) du système d’émulsification (Leal-Calderon et al., 2007 ; Jafari et al., 2008).
17Les systèmes d’émulsification de type rotor/stator (Ultra Turrax, Silverson, etc.), dans lesquels le mécanisme de rupture des gouttes est principalement lié aux forces de cisaillement (en écoulement laminaire et turbulent), sont caractérisés par des temps de résidence dans la zone d’émulsification compris entre 0,1 et 1 s, des densités d’énergie faibles à élevées, conduisant à la formation de gouttelettes de taille minimum autour de 1 µm. Et comme on pouvait s’y attendre, ces systèmes permettent, la plupart du temps, la formation des macro-émulsions (Canselier et al., 2004 ; Tadros, 2004 ; Jafari et al., 2008). Au contraire, les procédés dits à haute pression (homogénéiseur haute pression, microfluidiseur, etc.) dans lesquels le mécanisme de fragmentation des gouttes est beaucoup plus lié à la cavitation (en écoulement laminaire extensionnel) ont, comme caractéristiques principales, des temps de résidence plus courts (entre 0,1 et 3 ms) et des densités d’énergie moyennes à élevées, conduisant à la formation de gouttelettes de taille minimum de l’ordre de 0,1 µm. À la différence du procédé rotor/stator, ce type de procédé permet la fabrication de micro-émulsions (Canselier et al., 2004 ; Jafari et al., 2008). À l’instar du procédé haute pression, le procédé à ultrasons permet également la production de micro-émulsions. Dans ce cas, le mécanisme de rupture des gouttes est assuré par les forces de cavitation, mais en régime de microturbulence (Jafari et al., 2008).
18Effet des conditions « post-émulsification » (température, maturation). La température et la maturation peuvent affecter les propriétés de répartition de la taille des gouttelettes des crèmes au cours du stockage. Granger et al. (2005b) ont montré sur un modèle simplifié de crèmes végétales que leurs effets dépendent de la formulation (types de protéine, de MG et émulsifiant). Ainsi, tandis que pour les crèmes à base de poudre de lait écrémé, la maturation n'a pas modifié les caractéristiques de taille des gouttelettes, les diamètres moyens des gouttelettes ont diminué, dans des proportions relatives de 19 à 51 %, selon la composition en MG et en émulsifiant, pour les systèmes à base de protéines fonctionnelles du lait après 24 h de stockage à 4 °C (Tableau 2). Cette diminution de taille pourrait être due à une désagrégation partielle des gouttelettes qui se trouvaient préalablement reliées par pontage.
19Par ailleurs, à l’instar des crèmes laitières, l’application aux crèmes végétales d’un cycle thermique de cristallisation/fusion/recristallisation peut entrainer une augmentation de la taille de leurs gouttelettes, probablement du fait d’une coalescence partielle (Mutoh et al., 2001 ; Sugimoto et al., 2001). En effet, au cours de l’étape de la fusion, la migration vers l’interface des cristaux lipidiques résiduels favorise, lors de la recristallisation, une coalescence partielle des gouttelettes induite par un mécanisme de cristallisation hétérogène (Figure 1) (Boode et al., 1991 ; Mutoh et al., 2001).
2.2. Rhéologie
20La détermination des propriétés rhéologiques des produits alimentaires est d’une grande importance car elle permet de prévoir leur comportement mécanique non seulement au cours des différentes étapes de l’élaboration de l’aliment, mais également au cours de son stockage (Scher, 2006). En outre, les propriétés rhéologiques sont à l’origine des comportements perçus lors de l’évaluation sensorielle de la texture. La rhéologie des crèmes est mesurée au moyen de viscosimètres dont les plus couramment utilisés sont les viscosimètres capillaires et les viscosimètres rotatifs (rhéomètres). À la différence des viscosimètres simples (capillaire, par exemple) qui effectuent une mesure ponctuelle de la viscosité apparente, les rhéomètres permettent une étude plus complète du comportement rhéologique des crèmes via l’établissement des courbes d’écoulements en faisant varier le taux de cisaillement (Scher, 2006). Les facteurs pouvant influencer le comportement rhéologique des crèmes incluent aussi bien ceux liés à la formulation (types de MG, d’émulsifiant, stabilisant) que ceux liés au procédé d’émulsification.
21Paramètres liés à la formulation
22Effet du type et de la quantité de matière grasse. Comme dans toute émulsion H/E, le type de MG, et plus précisément sa composition en AG, de même que la concentration de la MG utilisée dans la formulation des crèmes végétales, peuvent affecter fortement leurs propriétés rhéologiques (Granger et al., 2003 ; Granger et al., 2005b ; Anihouvi, 2007). Des différences de comportement rhéologique ont, en effet, été notées au niveau des crèmes végétales de formulation simplifiée en fonction de la nature de la MGV (Granger et al., 2003 ; Granger et al., 2005b). Ces auteurs indiquent que la crème à base de la fraction oléique de l’huile de tournesol (plus riche en AG insaturés : AGI) montre, au gradient de vitesse de 1 s-1, la plus faible viscosité apparente qui, par ailleurs, évolue très peu pendant la maturation. Par contre, les crèmes à base d’autres MGV (huile de palme raffinée, huile de coco raffinée ou hydrogénée), plus riches en AG saturés (AGS), ont montré, au même gradient de vitesse, une plus grande viscosité apparente qui, de plus, s’accroît au cours de la maturation. Cette tendance a été confirmée, par la suite, par Anihouvi (2007) qui a rapporté qu’une crème végétale formulée avec l’huile de colza, plus riche en AGI, présente un comportement moins rhéofluidifiant et moins visqueux que celles préparées avec de l’huile de palme ou une MG laurique, plus riches en AGS. Par ailleurs, des résultats similaires ont été observés pour une formulation industrielle de mix de crèmes glacées laitières préparées à partir de la MG laitière ou de ses fractions (Abd El-Rahman et al., 1997). Ce résultat est par contre différent de ceux observés pour une autre formulation de mix de crèmes glacées laitières préparées à partir de la MGL seule ou en mélange (2/1 poids pour poids) avec la fraction oléique ou la fraction stérique (Bazmi et al., 2008). Ils ont, en effet, rapporté qu’après une maturation de 24 h à 5 °C, la crème enrichie avec la fraction oléique présente, à 5 s-1, une viscosité comparable à celle à base de la fraction entière seule et supérieure à celle enrichie avec la fraction stéarique. L’ensemble de ces résultats montre que le comportement rhéologique des crèmes ne peut être lié au seul facteur qu’est le type de MG, mais dépend des autres ingrédients (stabilisants, émulsifiants, etc.) utilisés dans la formulation ainsi que de leurs interactions. Granger et al. (2005b) ont d’ailleurs rapporté que les valeurs de viscosité des crèmes ne résultent pas seulement d’un seul facteur (taille des gouttelettes ou quantité de protéines dans la phase aqueuse ou cristallisation de la MG), mais sont plutôt la conséquence des interactions complexes entre la MG, les protéines et les émulsifiants de faible poids moléculaires.
23D’autre part, les résultats de Desrumaux et al. (1998) ont montré que le comportement rhéologique et la viscosité des crèmes varient fortement en fonction de la concentration de la MG dans la formulation et ce, quel que soit le procédé d’émulsification utilisé (Ultra Turrax ou homogénéiseur haute pression). Ainsi, ces crèmes présentent un comportement newtonien jusqu'à une fraction massique d'huile de 50 % et un comportement rhéofluidifiant pour des concentrations supérieures. Ces différents comportements rhéologiques observés selon la fraction massique de l’huile utilisée dans la formulation ont été confirmés par Floury et al. (2000) sur une crème végétale à base d’huile de soja (10 à 50 %) et de concentrés de protéines de lactosérum (1,5 %). Adapa et al. (2000) ont également montré, suite à l’utilisation du test de cisaillement dynamique, que le module élastique (G’) des crèmes augmente avec la concentration en MG (6,8 et 12 % de MG). Enfin, comme pour toute émulsion H/E, la viscosité apparente des crèmes augmente de façon importante avec l’augmentation du pourcentage de MG, comme le suggèrent de nombreux travaux (Boode et al., 1993a ; Adapa et al., 2000 ; Floury et al., 2000).
24Par ailleurs, Marquez et al. (2010) ont montré des modifications rhéologiques importantes (augmentation du module élastique G’ et du module visqueux G’’) sur des crèmes végétales contenant des sels de calcium préparées sous forme d’émulsions doubles (eau/huile/eau) et formulées à partir de l’huile de tournesol (32 %), du lait de soja, de l’eau, de la gomme xanthane et de l’émulsifiant lipidique polyricinoléate de polyglycérol. Ce comportement rhéologique observé sur des émulsions doubles s’explique, d’une part, par le gonflement des gouttelettes E/H du fait du gradient osmotique généré par l’inclusion de sels solubles dans la phase aqueuse interne et d’autre part, par la floculation des gouttelettes E/H en raison des interactions des sels présents dans la phase aqueuse externe avec les protéines du soja à l’interface.
25Effet du type d’émulsifiant. Une étude menée par Granger et al. (2005b) sur une formulation de crèmes végétales préparées à partir de différentes MGV a montré que la viscosité des crèmes varie fortement selon le type de protéines (poudre de lait écrémé contenant 80 % de caséines et 20 % de protéines de lactosérum ou protéines fonctionnelles du lait contenant 60 % de protéines de lactosérum et 40 % de caséines) et le type d’émulsifiant lipidique (MDG saturé ou partiellement insaturé). En appliquant un gradient de vitesse de 1 s-1 pour des crèmes fabriquées avec la poudre de lait écrémé, aucun écart de viscosité significatif (entre 0 et 0,2 Pa.s) n’est observé ni avant ni après une maturation de 24 h à 4 °C, quel que soit le type de MDG ou le type de MG. Par contre, des écarts de viscosité importants (entre 0,2 et 1,6 Pa.s) sont observés au même gradient de vitesse pour des crèmes stabilisées avec des protéines fonctionnelles du lait, en fonction du type d’émulsifiant lipidique et du type de MG. Ces résultats confirment ceux de Davies et al. (2000) qui ont observé un effet significatif de la concentration de l’émulsifiant lipidique (glycérol mono-oléate : GMO) sur la viscosité de crèmes végétales formulées à partir de l’huile d’arachide (40 %) et de caséinate de sodium (1 %). Ainsi, les crèmes contenant moins de 3,5 % de GMO restent liquides après un refroidissement jusqu’à 5 °C, tandis que celles qui en contiennent plus de 3,5 % ont épaissi, du fait d’une forte coalescence partielle des gouttelettes à la suite de la désorption des protéines.
26Effet du type de stabilisant. Comme évoqué précédemment, les carraghénanes sont les agents stabilisants les plus utilisés dans la formulation des crèmes. Ce sont des polysaccharides linéaires constitués de molécules de galactose plus ou moins substitués par des groupements sulfates. Il existe trois principaux types de carraghénanes aux propriétés différentes, qui se distinguent par le nombre de groupements sulfates. Le κ-carraghénane (faiblement sulfaté) possède des propriétés gélifiantes remarquables et est le plus utilisé dans la formulation des crèmes car il permet de contrôler plus efficacement le phénomène d’incompatibilité noté, en général, entre les protéines du lait et les hydrocolloïdes, incompatibilité qui se traduit par une séparation de phase de ces deux ingrédients (Vega et al., 2005). En effet, ce polysaccharide interagit avec la κ-caséine par le biais d’interactions électrostatiques pour former un gel induisant une augmentation de la viscosité de la phase aqueuse. La présence d'ions Ca2+ favorise cette gélification par formation de ponts Ca2+ entre les molécules, permettant alors d’éviter ou de freiner la séparation visuelle des biopolymères incompatibles. Par ailleurs, le κ-carraghénane est fréquemment utilisé en association avec certains hydrocolloïdes incompatibles avec les protéines du lait (guar, caroube, xanthane, etc.) pour la stabilisation des crèmes et des mousses (Vega et al., 2005 ; Zamorano, 2006). Le λ-carraghénane (très sulfaté) présente un caractère stabilisant et épaississant. Enfin, comme le κ-carraghénane, le ι-carraghénane présente également des propriétés gélifiantes, mais a la particularité de former un gel élastique, ce qui fait qu’il est très souvent utilisé pour la création des produits flasques et malléables (Zamorano, 2006).
27Paramètres liés aux conditions d’émulsification et de maturation
28Effet des conditions d’émulsification. Selon Walstra (1983), les conditions d’homogénéisation peuvent avoir un important effet sur la rhéologie des crèmes. Une augmentation de la pression d’homogénéisation (de 0 à 300 atm) se traduit par une augmentation de la viscosité des crèmes (Figure 2a). Cet effet est le plus souvent dû à la formation de clusters de gouttelettes qui partagent la même molécule d’émulsifiant (protéine), du fait que la quantité d’émulsifiant est insuffisante pour couvrir la nouvelle interface créée (Floury et al., 2000). Cependant, certains auteurs ont révélé que l’influence croissante de la pression d’homogénéisation sur la viscosité des crèmes est valable pour une gamme de pressions au-delà de laquelle la viscosité diminue (Floury et al., 2000 ; Desrumaux et al., 2002). La recherche d’une pression optimum d’homogénéisation pour chaque produit se révèle donc indispensable. La perte de viscosité d’une crème végétale formulée avec de l’huile de tournesol et les protéines du lactosérum a été attribuée à la dénaturation des protéines au cours de l’homogénéisation ultra haute pression (Desrumaux et al., 2002). Cette dénaturation des protéines affecte probablement leurs propriétés émulsifiantes, ce qui se traduit par une augmentation de la taille des gouttelettes formées. Long et al. (2012) a également montré, en utilisant des pressions d’homogénéisation conventionnellement pratiquées dans les industries laitières (entre 20 et 50 Mpa), que le comportement rhéologique d’une crème laitière se rapproche de plus en plus de celui d’un gel lorsque la pression augmente.
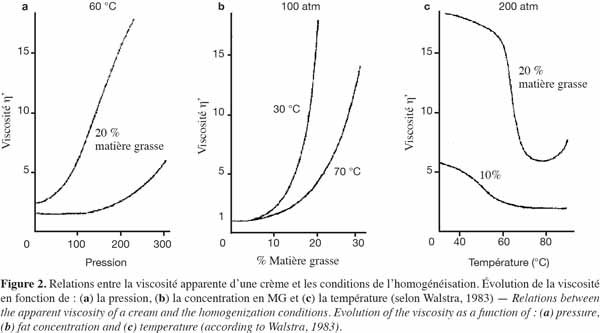
29La viscosité apparente augmente avec la fraction de la MG utilisée dans la formulation des crèmes (Figure 2b) et diminue avec l’augmentation de la température d’homogénéisation (Figure 2c).
30Effet des conditions « post-émulsification » (température, maturation). Comme le montrent les travaux de Granger et al. (2003, 2005b) et ceux de Marquez et al. (2005), après l’émulsification, la viscosité augmente généralement avec l’abaissement de la température et avec la maturation des émulsions (par exemple, un stockage pendant 24 h à 4 °C). L’augmentation de la viscosité apparente peut être due à différents facteurs tels qu'une variation de la viscosité de la phase aqueuse elle-même, un changement de la fraction volumique du corps dissout, une augmentation de la concentration de gouttelettes et/ou une variation de leur taille.
31En outre, Boode et al. (1991) ont montré, sur des crèmes laitières, que la texture des crèmes peut évoluer d’un état liquide à l’état de gel lorsqu’elles sont soumises à un cycle thermique de cristallisation/fusion/recristallisation. Sugimoto et al. (2001) et Mutoh et al. (2001) ont mis en évidence le même phénomène sur des crèmes végétales et établi une relation entre le taux de solide (SFC) de la MG des crèmes après l’étape de fusion et l’état solide ou liquide résultant. Ainsi, les températures induisant un SFC bas engendrent une solidification de la crème. Par contre, la crème reste liquide lorsque les températures d’exposition entrainent un pourcentage de SFC nul. Ceci semble en conformité avec les résultats d’Arboleya et al. (2005) qui ont montré que la microviscosité (mesurée par résonance paramagnétique électronique) à l’intérieur des gouttelettes d’une émulsion huile de palme/eau dépend de la température et qu’une température de stockage en dessous du point de fusion de la MG est cruciale pour une augmentation de la microviscosité, en raison de la solidification de la graisse. Par ailleurs, les résultats de Reiffers-Magnani et al. (1999) portant sur un modèle simplifié de crèmes végétales (20 ou 40 % d’huile de soja, 9,8 ou 13 % de protéines de lactosérum) ont mis en évidence au cours d’un traitement de chauffage de 25 à 80 °C, que leur comportement rhéologique déterminé au moyen de la technique de cisaillement oscillant est compris entre celui d’un gel polymérique et d’un gel de particules.
2.3. Stabilité
32Plusieurs études ont mis en évidence les mécanismes traditionnels de déstabilisation physique des émulsions dans les crèmes aussi bien végétales (Mutoh et al., 2001 ; Sugimoto et al., 2001 ; Granger et al., 2003 ; Granger et al., 2005b ; Koupantsis et al., 2009) que laitières (Boode et al., 1993a ; Bazmi et al., 2007 ; Vanderghem et al., 2007 ; Bazmi et al., 2008). Les protéines laitières ainsi que les agents stabilisants (carraghénanes, agar, xanthane, alginate, etc.) sont les ingrédients de la formulation les plus utilisés pour améliorer la stabilité cinétique des crèmes. Ainsi, la stabilité au cours du temps est une caractéristique fondamentale à vérifier car c'est l'un des paramètres qui garantit au consommateur un produit de qualité constante et optimale (Curt, 1994 ; Tadros, 2004).
33Différentes méthodes peuvent être utilisées pour la caractérisation de la stabilité cinétique des crèmes : action de la gravité, mesures des teneurs en matières grasses et en eau, méthodes optiques, utilisation de la RMN, conductimétrie, etc. La méthode optique utilisant la lumière rétrodiffusée à balayage vertical est très utilisée actuellement car elle est rapide et efficace, et permet de comprendre les mécanismes physiques impliqués dans la déstabilisation des émulsions et d’aborder les aspects cinétiques de la déstabilisation (Curt, 1994).
34Paramètres liés à la formulation
35Effet du type et de la quantité de matière grasse. Towler (1982) a rapporté que la composition de la MG influence la stabilité des crèmes et a observé que les crèmes végétales élaborées à partir d’huile de palme (riche en C16 :0) ou de palmiste (riche en C12 :0) sont généralement plus stables que les crèmes à base de MGL. Shamsi et al. (2002) ont par la suite confirmé ces résultats en rapportant que les crèmes végétales ont tendance à être plus stables que les crèmes laitières, notamment dans les régions chaudes. Les températures élevées induisent probablement au niveau des crèmes laitières (plus riches en AG à courtes chaines) un SFC susceptible de provoquer une agrégation des gouttelettes via la coalescence partielle, comparativement aux crèmes végétales élaborées avec des huiles saturées. Par ailleurs, Anihouvi (2007) a montré pour un modèle simplifié de crèmes végétales, que des crèmes à base d’huile de palme ou d’une MG laurique sont beaucoup plus stables face au crémage qu’une crème élaborée dans les mêmes conditions, mais à base d’une huile de colza (contenant plus de 90 % d’AGI).
36En outre, une faible teneur en MG engendre une faible concentration en gouttelettes, ce qui défavorise la coalescence partielle et de ce fait, améliore la stabilité de la crème (Thivilliers, 2007).
37Effet du type d’émulsifiant. Les protéines du lait (protéines solubles, caséines) sont largement utilisées pour améliorer la stabilité cinétique des crèmes (Dalgleish, 1997). En effet, la présence des protéines autour des gouttelettes lipidiques améliore la stabilité face à la coalescence2 et à la floculation3 et ce, par le biais des interactions répulsives électrostatiques et stériques, qui contribuent à maintenir les gouttelettes dans un état dispersé en limitant leur rapprochement. L’efficacité de la stabilité dépend du type de protéine utilisé dans la formulation ainsi que des caractéristiques biochimiques de la phase dispersée (pH, force ionique, etc.) qui impactent la structure des protéines (Granger et al., 2005b ; Lepoudère et al., 2010). Les protéines sériques, caractérisées par une plus faible activité interfaciale, à cause de leur structure globulaire, forment un film interfacial fin, et de ce fait stabilisent moins bien les crèmes, que les caséines qui forment un film plus épais autour des gouttelettes (du fait de leur structure micellaire) (Lepoudère et al., 2010).
38Par ailleurs, la présence dans la formulation d’émulsifiants de faible poids moléculaire, en plus des protéines, entraine le plus souvent une déstabilisation des crèmes qui peut se manifester par une floculation, une coalescence ou une coalescence partielle en cas de présence de cristaux lipidiques. Leur présence crée en fait une instabilité de l’interface à travers la désorption des protéines de la surface des gouttelettes (Davies et al., 2000). Ainsi, les tensioactifs non ioniques (tweens, esters de sucrose, etc.) sont, en général, plus efficaces que les tensioactifs ioniques (MDG, esters de sorbitol, etc.) pour déplacer les protéines des surfaces hydrophobes (Dalgleish, 1997) : les tensioactifs ioniques interagissent en général fortement avec les protéines pour former des complexes mixtes à l’interface huile/eau, ce qui limite une plus grande désorption des protéines (Chen et al., 1995). De plus, la désorption des protéines est fortement liée à leur stabilité conformationnelle ; les protéines flexibles et désordonnées comme les caséines, ayant une plus grande capacité à adapter leur conformation, résistent mieux à la désorption que les protéines compactes et globulaires telles que les protéines sériques (Schorsch, 2007 ; Croguennec et al., 2008). Le contrôle de la déstabilisation des films, initialement protégés par des couches protéiques par ajout de tensioactifs, est mis à profit dans la formulation de certains types de crèmes telles que la crème Chantilly ou la crème à fouetter. Ce type de produits requiert en effet une déstabilisation contrôlée du film pour favoriser la coalescence partielle, ce qui est nécessaire pour la réussite de l’opération du foisonnement (Schorsch, 2007).
39Effet du type de stabilisant. Les principaux agents stabilisants utilisés dans la formulation des crèmes ont été déjà discutés. Ils sont essentiellement constitués de polyosides. Selon les travaux de Leal-Calderon et al. (2007), les polysaccharides contribuent à l’inhibition du crémage4 des crèmes et de la séparation de phases au cours du stockage sans agitation, à travers la régulation de la rhéologie du film de la phase continue localisé entre les gouttelettes lipidiques. Par ailleurs, selon le pH du milieu et la nature du stabilisant, la stabilité de la crème peut être renforcée ou fragilisée. En effet, Surh et al. (2006) ont mis en évidence sur une formulation simplifiée de crèmes végétales (10 % huile de maïs, 1 % caséinate de sodium) que la présence de la pectine faiblement ou fortement méthoxylée améliore significativement la stabilité au crémage aux pH 4 et 5 ; par contre, elle déstabilise fortement la crème aux pH 6 et 7 (floculation par déplétion). La grande stabilité au crémage notée aux pH 4 et 5 serait probablement liée à l’adsorption de la pectine sur la surface des gouttelettes, dont le corollaire est l’accroissement des forces de répulsions stérique et électrostatique entre les gouttelettes. Par contre, en l’absence de pectine, la crème présente une forte stabilité au crémage aux pH 6 et 7 et une moindre stabilité aux pH 4 et 5. Par ailleurs, Koupantsis et al. (2009) ont rapporté, toujours en utilisant un modèle simplifié de crème végétale (10 % huile de maïs, 1 % protéines de lactosérum), que la stabilité des crèmes à la floculation, au crémage, et dans une moindre mesure à la coalescence, dépend fortement de la présence de la CMC et des interactions protéine-polysaccharide en fonction du pH du milieu.
40Effet de la température. Comme il a été montré précédemment, la temperature, tant au cours du stockage que de la maturation, peut entrainer des modifications granulométriques, dont l’intensité varie avec la formulation, et par conséquent affecte la stabilité physique des crèmes. Par ailleurs, comme dans toute émulsion, une élévation de la température de la crème intensifie l’agitation thermique qui multiplie les collisions, rendant ainsi plus probables les occasions de coalescence (Canselier et al., 2004). En outre, lorsque les émulsions à base de protéines sont soumises à une élévation de température (pasteurisation, stérilisation), les protéines tendent généralement à s’agréger et à engendrer la floculation des gouttelettes (Leal-Calderon et al., 2007). Il est important de signaler que les protéines sériques sont plus thermosensibles que les caséines (Lepoudère et al., 2010). La β-lactoglobuline, par exemple, se dénature pour des températures supérieures à 73 °C (Blecker, 1998).
41D’un autre côté, une diminution de la température engendre la formation de cristaux lipidiques qui peuvent être à l’origine de l’avènement de la coalescence partielle suite à la fragilisation de la membrane autour des gouttelettes lipidiques. L’hypothèse de l’influence de la cristallisation sur la résistance des gouttelettes aux changements physiques dans les émulsions huile/eau en général et dans les crèmes, en particulier, est fortement soutenue (Boode et al., 1993a ; Boode et al., 1993b). Plus spécifiquement, Davies et al. (2000) ont rapporté que l’augmentation du taux de la matière grasse cristallisée favorise la coalescence partielle des gouttelettes ; ils mettent aussi en exergue l’importance de la taille et de la forme des cristaux.
42Par ailleurs, comme évoqué précédemment, l’application d’un cycle thermique de cristallisation/fusion/recristallisation peut induire une augmentation de la taille des gouttelettes des crèmes qui affecte négativement leur stabilité ; une solidification par coalescence partielle est alors invoquée (Mutoh et al., 2001 ; Sugimoto et al., 2001 ; Thivilliers, 2007).
2.4. Aptitude au foisonnement et stabilité des crèmes foisonnées
43Les propriétés physiques (taille de gouttelettes, viscosité, stabilité) des mix utilisés pour élaborer des crèmes foisonnées ont un impact significatif sur leur aptitude au foisonnement ainsi que leur stabilité et leur texture (Stanley et al., 1996). Comme démontré précédemment, les propriétés physico-chimiques des crèmes dependent, quant à elles, fortement de la formulation et du procédé. Nous mettrons l’accent, dans ce qui suit, sur les paramètres de formulation et principalement sur la MG, qui influencent le plus le foisonnement et la stabilité des mousses. Pour ce faire, nous développerons le cas particulier des crèmes fouettées de type Chantilly, où la MG joue un rôle essentiel. Les effets des conditions de foisonnement seront également abordés.
44Paramètres liés à la formulation
45Effet du type de MG. La présence de cristaux de MG est essentielle à la fabrication des émulsions foisonnées. En effet, Anihouvi (2007) a montré dans le cas d’une formulation simplifiée de crèmes végétales qu’il est impossible, dans les conditions habituelles, de foisonner une crème à base d’huile de colza comme seule MG, ne contenant de ce fait aucune fraction solide. Au contraire, dans les mêmes conditions, les crèmes à base d’huile de palme ou d’une MG laurique qui elles, contiennent une quantité significative de MG solide, incorporent correctement de l’air dans leur structure. La nécessité d’avoir des cristaux de MG pour réussir un foisonnement s’explique par le fait qu’ils constituent des sites d’interaction entre les gouttelettes (Figure 1) : ces cristaux dirigent la coalescence partielle au moment du foisonnement et donc favorisent la formation d’un réseau de gouttelettes interconnectées (Van Aken, 2001 ; Schorsch, 2007). En outre, selon Riaublanc et al. (2005), dans le cas des crèmes laitières, le taux de foisonnement augmente avec la teneur en MG solide de la phase dispersée, mais évolue très peu à partir d’une valeur seuil (autour de 20 % de solide) pour atteindre son maximum pour un taux de solide autour de 60 %.
46Par ailleurs, dans les crèmes laitières foisonnées où la teneur en MG est forte (30-40 %), comme les crèmes Chantilly, la stabilité cinétique des bulles d'air est assurée simultanément par la présence de gouttelettes aux interfaces de bulles d'air et par la formation d'agrégats de MG interconnectés entre les bulles d'air (Schorsch, 2007). Remarquons cependant que les conditions de formation de ces agrégats, attribuées au battage et au cisaillement qu'il fait subir aux gouttelettes, ne sont pas encore bien élucidées. Néanmoins, il est utile d’indiquer que l’état du réseau cristallin et de sa connectivité, qui assurent la stabilité des mousses, dépendent en grande partie de la nature de la MG, de la vitesse de refroidissement de la crème après l’étape de pasteurisation, mais aussi des conditions de maturation (Riaublanc et al., 2005).
47En outre, les formes polymorphiques des cristaux de MG peuvent également avoir une influence sur l’aptitude au foisonnement et la stabilité des mousses. Che Man et al. (2003) ont rapporté que les cristaux de type β’ sont plus appropriés pour l’élaboration et la stabilisation des mousses. Selon ces auteurs, ces cristaux, souvent de petite taille et en forme d’aiguille, croissent simultanément et forment un réseau cristallin avec une large surface, capable de retenir une plus grande quantité de MG liquide dans leur structure, favorisant également une plus grande incorporation de gaz.
48Comparées aux crèmes laitières, certaines formulations de crèmes végétales, plus particulièrement celles utilisant des MG lauriques ou de l’huile de palme, présentent de meilleures propriétés de foisonnement et une plus grande stabilité après foisonnement lorsque les températures de stockage sont élevées (20 à 40 °C) (Nesaretnam et al., 1993 ; Berger, 1998 ; Shamsi et al., 2002). Shamsi et al. (2002) ont par ailleurs indiqué que la teneur en AGI, particulièrement celui de l’acide oléique, influence positivement la stabilité des mousses en travaillant sur des crèmes végétales formulées à partir de mélanges d’huiles de palme (riche en C16 :0 et C18 :1) et de palmiste (riche en C12 :0). Cette influence positive de la teneur en AGI des MG semble être également confirmée par Bazmi et al. (2007) sur des mousses laitières de formulation industrielle préparées à partir de la MGL seule ou en mélange (2/1 poids pour poids) avec la fraction oléique ou la fraction stérique. En outre, les crèmes végétales peuvent présenter une stabilité à des cycles chaud et froid et offrent, dans certains cas, la possibilité d’être travaillées à l’avance. Elles peuvent présenter la propriété de résistance à la congélation, caractéristique très recherchée dans la fabrication des crèmes glacées (Richard, 2005).
49Effet du type d’émulsifiant. Dans la formulation des crèmes fouettées, outre des protéines, les émulsifiants de faible poids moléculaire sont utilisés pour assurer une désorption de celles-ci au cours de la maturation. Cette désorption des protéines par les émulsifiants de faible poids moléculaire est nécessaire pour induire un début de déstabilisation des gouttelettes, en vue de contrôler le niveau de coalescence partielle nécessaire pour la réussite du foisonnement et la stabilisation ultérieure des bulles de gaz (Stanley et al., 1996 ; Van Aken, 2001). Les protéines désorbées des interfaces huile/eau diffusent rapidement aux interfaces gaz/eau pour assurer la stabilité à court terme, en particulier lors du foisonnement. Les micelles de caséine sont les plus impliquées dans cette stabilité à court terme, du fait de leur plus grande capacité à adapter leur conformation (Schorsch, 2007). Les protéines sériques interviennent, quant à elles, dans la stabilisation à long terme (au cours du stockage) des crèmes fouettées allégées, mais cette stabilisation cinétique est moins efficace que celle assurée par le réseau de gouttelettes interconnectées (Dalgleish, 1997 ; Schorsch, 2007).
50Effet du type de stabilisant. L’addition de stabilisants, tels que les polysaccharides, dans la formulation augmente la viscosité de la phase aqueuse des mix et permet de limiter après foisonnement, le phénomène de drainage des mousses (Vega et al., 2005). La nature des stabilisants utilisés peut également affecter les performances au foisonnement des crèmes. Anton et al. (2005) ont, par exemple, montré des différences dans les capacités de foisonnement ainsi que la répartition de taille des bulles d’air au niveau de formulation industrielle de mousses laitières de type Chantilly, préparées à partir de différents mélanges d’hydrocolloïdes.
51Paramètres liés au procédé
52Effet de la pression d’homogénéisation. La pression d’homogénéisation affecte aussi bien la stabilité que la texture finale des crèmes. Selon Schorsch (2007), une pression d'homogénéisation trop haute entraine une déstabilisation de l'émulsion, à moins de reformuler le système de façon adéquate, par exemple, en diminuant le taux protéique. Elle entraine aussi d’autres répercussions négatives comme, par exemple, une moindre aptitude au foisonnement et une stabilité réduite des mousses (Schorsch, 2007). La figure 3 donne une parfaite illustration de l’effet d’une pression trop élevée sur la texture d’une crème foisonnée de type Chantilly. La mousse obtenue à partir de la crème homogénéisée avec une pression de 150 bars présente une structure moins bien aérée et une texture moins ferme qui tient difficilement dans une cuillère, alors que la mousse élaborée au départ de la crème émulsionnée à 100 bars présente les caractéristiques recherchées pour une mousse classique (bonne stabilité, texture bien ferme, etc.).
53Effet des conditions de foisonnement. Les conditions de foisonnement, à savoir le type de foisonneur (Labbafi et al., 2005), la durée du foisonnement (Van Aken, 2001), mais aussi la température (Stanley et al., 1996 ; Shamsi et al., 2002 ; Schorsch, 2007) sont connus pour leurs effets sur le taux de foisonnement et la stabilité des mousses. Une température inférieure à 10 °C est généralement recommandée pour réaliser l’opération de foisonnement, alors qu’une température plus élevée entraine une teneur en MG liquide supérieure, ce qui est défavorable au foisonnement (Riaublanc et al., 2005).
54Par ailleurs, l’application d’un cycle thermique de fusion partielle/cristallisation aux crèmes foisonnées permet d’augmenter considérablement leur fermeté et d’améliorer leur stabilité physique dans le temps. Cette consolidation des mousses est généralement attribuée, comme dans le cas des crèmes non foisonnées, à l’augmentation de la connectivité du réseau de gouttelettes, du fait de l’accentuation du phénomène de coalescence partielle à la suite du traitement thermique (Riaublanc et al., 2005).
3. Conclusion
55Cette étude bibliographique a permis de faire le point sur l’influence des différents paramètres de formulation et de procédé sur les propriétés physico-chimiques des crèmes, en se focalisant particulièrement sur les crèmes végétales. Il apparait que les conditions d’émulsification, le choix des ingrédients (tant protéiques que lipidiques) utilisés dans la formulation, ainsi que la température, influencent les propriétés finales des crèmes. Cependant, peu de données existent dans la littérature sur les crèmes végétales contrairement aux crèmes laitières, du fait que ce domaine est assez récent et que ces connaissances constituent souvent un « savoir-faire technique secret » industriel peu diffusé au niveau des publications scientifiques. Néanmoins, il apparait que les crèmes végétales peuvent conduire à de nouvelles propriétés technofonctionnelles. Ainsi, la résistance à la congélation pouvant conférer une grande stabilité aux crèmes glacées en est un exemple. Elles peuvent également présenter une stabilité en liaison chaude ou froide, ce qui est un avantage considérable, puisque ces crèmes peuvent être utilisées indifféremment dans la préparation de plats chauds ou froids.
56Si les crèmes végétales peuvent apporter de nouvelles fonctionnalités et montrer des propriétés texturales comparables voire plus intéressantes que celles des crèmes laitières (Nesaretnam et al., 1993 ; Berger, 1998 ; Carr et al., 2005), il n’en demeure pas moins qu’elles peuvent présenter des défauts sensoriels, notamment par rapport à leur gout et leur odeur, même parfois après l’ajout d’arômes (Shim et al., 2004 ; Wan Rosnani et al., 2008). Par contre, les crèmes laitières continuent d’être appréciées pour leur sensation en bouche agréable, leur gout et leur odeur en raison de leurs fortes proportions en AG à courte chaine (Croguennec et al., 2008). Bien que les crèmes végétales élaborées avec des huiles saturées se positionnent comme des alternatives sérieuses et intéressantes aux crèmes laitières foisonnées (du fait du rôle essentiel des cristaux lipidiques dans le développement de leurs propriétés), les crèmes végétales à base d’huiles liquides contenant des sels solubles dans la formulation, préparées selon la technologie d’émulsions doubles E/H/E, peuvent également constituer une alternative potentielle de substitution des crèmes laitières foisonnées. En effet, Marquez et al. (2010) ont montré qu’il est possible de moduler la consistance de ces crèmes (dépourvues de cristaux de MG), en agissant sur la concentration et le type de sel, la concentration de l’émulsifiant lipidique, la teneur en huile et le pourcentage de phase aqueuse dispersée.
57Enfin, le marché des crèmes évoluant de façon fort dynamique et devenant de plus en plus spécifique par rapport aux propriétés attendues des crèmes, il y a nécessité aujourd’hui de déterminer et de comprendre les voies technologiques qui permettent d’obtenir des propriétés maitrisées et adaptées aux applications, afin de pouvoir être en mesure de répondre aux besoins actuels et futurs des consommateurs ou des industriels. Dans ce contexte bien particulier, des recherches doivent être menées sur les crèmes végétales afin d’approfondir les connaissances sur l’influence de la MG et d’autres ingrédients (protéines, émulsifiants de faible poids moléculaire, stabilisants) et de leurs interactions (protéines-protéines, protéines-MG, protéines-eau, etc.) sur les propriétés finales des crèmes ; en effet, les interactions entre les différents composants impliqués dans l’organisation structurale des crèmes provoqueraient des modifications de leurs propriétés texturales et organoleptiques. Les améliorations actuelles et futures des propriétés des crèmes passeront alors par une meilleure maitrise de ces systèmes tant au niveau microscopique (morphologie des cristaux de MG) que moléculaire via la compréhension des interactions entre les différents ingrédients (MG, protéines, émulsifiants de faible poids moléculaire, etc.) aux interfaces et au sein de chaque phase. Les spectroscopies infrarouge et de fluorescence, parmi d’autres, pourraient alors apporter des informations pertinentes permettant d’expliquer in fine les interactions qui peuvent avoir lieu entre les différents composants et de leurs influences sur la stabilité, le comportement rhéologique ainsi que les propriétés texturales et organoleptiques des crèmes.
58Liste des abréviations
59AG : acides gras
60AGI : acides gras insaturé
61AGS : acides gras saturé
62CMC : carboxyméthylcellulose
63DG : diglycéride
64Émulsion H/E : émulsion huile/eau
65Émulsion double E/H/E : émulsion eau/huile/eau
66G’ : module élastique
67G’’ : module visqueux
68GMO : glycérol mono-oléate
69Gouttelette E/H : gouttelette eau/huile
70HCH : huile de coco hydrogénée
71HCR : huile de coco raffinée
72HPR : huile de palme raffinée
73MG : matière grasse
74MGL : matière grasse laitière
75MGV : matière grasse végétale
76MDG : mono-diglycéride
77PFL : protéines fonctionnelles du lait
78PLE : poudre de lait écrémé
79SFC : solid fat content (taux de solide)
80RMN : résonance magnétique nucléaire
Bibliographie
Abd El-Rahman A.M., Madkor S.A., Ibrahim F.S. & Kilara A., 1997. Physical characteristics of frozen desserts made with cream, anhydrous milk fat or milk fat fractions. J. Dairy Sci., 80, 1926-1935.
Adapa S., Dingeldein H., Schmidt K.A. & Herald T.J., 2000. Rheological properties of ice cream mixes and frozen ice creams containing fat and fat replacers. J. Dairy Sci., 83, 2224-2229.
Anton M. et al., 2005. Stabilisation des mousses émulsionnées laitières : substitution de la gélatine par des mélanges de polysaccharides. Sci. Aliments, 25(5-6), 443-453.
Arboleya J.C., Sutcliffe L.H., Wilde P.J. & Fairhurst S.A., 2005. Density and microviscosity studies of palm oil/water emulsions. J. Agric. Food Chem., 53(11), 4448-4453.
Barfod N.M., Krog N., Larsen G. & Buchheim W., 1991. Effects of emulsifiers on protein-fat interaction in ice cream mix during ageing. I. Quantitative analyses. Fat Sci. Technol., 93, 24-29.
Bazmi A., Duquenoy A. & Relkin P., 2007. Aeration of low fat dairy emulsions: effects of saturated-unsaturated triglycerides. Int. Dairy J., 17, 1021-1027.
Bazmi A., Launay B., Cuvelier G. & Relkin P., 2008. Impact of crystalline milk fat on rheological properties of ice cream mix emulsions during aging time at 4°C. J. Texture Stud., 39, 309-325.
Berger K.G., 1998. Recent results on palm oil uses in food products. Palm Oil Dev., 29, 7-12.
Blecker C., 1998. Étude de la modification des propriétés fonctionnelles du lactosérum par hydrolyse enzymatique de sa matière grasse résiduelle. Thèse de doctorat : Faculté universitaire des Sciences agronomiques de Gembloux (Belgique).
Boode K., Bisperink C. & Walstra P., 1991. Destabilization of O/W emulsions containing fat crystals by temperature cycling. Colloids Surf., 61, 55-74.
Boode K. & Walstra P., 1993a. Partial coalescence in oil-in-water emulsions. 1. Nature of the aggregation. Colloids Surf., A, 81, 121-137.
Boode K., Walstra P. & de Groot-Mostert A.E.A., 1993b. Partial coalescence in oil-in-water emulsions. 2. Influence of the properties of the fat. Colloids Surf., A, 81, 139-151.
Canselier J.-P. & Poux M., 2004. Procédés d’émulsification. Mécanismes de formation des émulsions. Tech. Ing., article [J 2 152].
Carr N.O. & Hogg W.F., 2005. A manufacturer’s perspective on selected palm-based products. Asia Pac. J. Clin. Nutr., 14(4), 381-386.
Che Man Y.B., Shamsi K., Yusoff M.S.A. & Jinap S., 2003. A study on the crystal structure of palm oil-based whipping cream. J. Am. Oil Chem. Soc., 80, 409-415.
Chen J. & Dickinson E., 1995. Protein/surfactant interracial interactions Part 3. Competitive adsorption of protein + surfactant in emulsions. Colloids Surf., A, 101, 77-85.
Codex Alimentarius, codex Stan 192, 1995. Norme générale Codex pour les additifs alimentaires. Rome : FAO/OMS.
Codex Alimentarius, 2007. Lait et produits laitiers. Rome : FAO/OMS.
Croguennec T., Jeantet R. & Brulé G., 2008. Fondements physico-chimiques de la technologie laitière. Paris : Lavoisier, Tec & Doc.
Curt C., 1994. Méthodes d'évaluation de la stabilité des émulsions. Principe, applications, avantages et inconvénients. Sci. Aliments, 14(6), 699-724.
Dalgleish D.G., 1997. Food emulsions stabilized by proteins. Cur. Opin. Colloid Interface Sci., 2, 573-577.
Davies E., Dickinson E. & Bee R., 2000. Shear stability of sodium caseinate emulsions containing monoglyceride and triglyceride crystals. Food Hydrocolloids, 14, 145-153.
Desrumaux A. & Della Valle D., 1998. Rhéologie d'émulsions alimentaires huile/eau : influence du procédé d'émulsification. Cah. Rhéol., 16(3), 358-363.
Desrumaux A. & Marcand J., 2002. Formation of sunflower oil emulsions stabilized by whey proteins with high-pressure homogenization (up to 350 MPa): effect of pressure on emulsion characteristics. Int. J. Food Sci. Technol., 37, 263-269.
Ennifar M., 2006. La problématique de la matière grasse dans la filière laiterie européenne. Bilan depuis 1990 et perspectives à l’horizon 2014. Paris : Office de l’Élevage.
Euston S.R., 2008. Emulsifiers in dairy products and dairy substitutes. In: Hasenhuettl G.L. & Hartel R.W., eds. Food emulsifiers and their applications. New York, USA: Springer Science + Business Media, LLC, 195-232.
Floury J., Desrumaux A. & Lardières J., 2000. Effect of high-pressure homogenization on droplet size distributions and rheological properties of model oil-in-water emulsions. Innovative Food Sci. Emerg. Technol., 1, 127-134.
Goff H.D., 1997. Instability and partial coalescence in whippable dairy emulsions. J. Dairy Sci., 80(10), 2620-2630.
Granger C. et al., 2003. Influence of the fat characteristics on the physicochemical behavior of oil-in-water emulsions based on milk proteins-glycerol esters mixtures. Colloids Surf., B, 32, 353-363.
Granger C. et al., 2005a. Influence of formulation on the structural networks in ice cream. Int. Dairy J., 15, 255-262.
Granger C., Barey P., Veschambre P. & Cansell M., 2005b. Physicochemical behavior of oil-in-water emulsions: influence of milk protein mixtures, glycerol ester mixtures and fat characteristics. Colloids Surf., B, 42, 235-243.
Holstborg J., Pedersen B.V., Krog N. & Olesen S.K., 1999. Physical properties of diglycerol esters in relation to rheology and stability of protein-stabilised emulsions. Colloids Surf., B, 12, 383-390.
Jafari S.M., Assadpoor E., He Y. & Bhandari B., 2008. Re-coalescence of emulsion droplets during high-energy emulsification. Food Hydrocolloids, 22, 1191-1202.
Jeantet R. et al., 2008. Les produits laitiers. 2e éd. Paris : Lavoisier, Tec & Doc.
Koupantsis T. & Kiosseoglou V., 2009. Whey protein-carboxymethylcellulose interaction in solution and oil-in-water emulsions systems. Food Hydrocolloids, 23, 1156-1163.
Krause A.J., Lopetcharat K. & Drake M.A., 2007. Identification of the characteristics that drive consumer liking of butter. J. Dairy Sci., 90(5), 2091-2102.
Labbafi M. et al., 2005. Impact de la technologie et des conditions du foisonnement sur l'élaboration de mousses laitières de type « topping ». Sci. Aliments, 25(5-6), 381-395.
Leal-Calderon F., Thivilliers F. & Schmitt V., 2007. Structured emulsions. Curr. Opin. Colloid Interface Sci., 12, 206-212.
Lepoudère A., Snappe J.-P. & Sredzinski N., 2010. Protéines laitières. Tech. Ing., article [F 4 820].
Lim C.W., Norziah M.H. & Lu H.F.S., 2010. Effect of flaxseed oil towards physicochemical and sensory characteristic of reduced fat ice creams and its stability in ice creams upon storage. Int. Food Res. J., 17, 393-403.
Long Z. et al., 2012. Effect of homogenisation and storage time on surface and rheology properties of whipping cream. Food Chem., 131(3), 748-753.
Marquez A.L., Palazolo G.G. & Wagner J.R., 2005. Cream-like emulsions prepared with soy-milk 3: effect of temperature cycling. Grasas Aceites, 56(3), 182-187.
Marquez A.L. & Wagner J.R., 2010. Rheology of double (w/o/w) emulsions prepared with soybean milk and fortified with calcium. J. Texture Stud., 41(5), 651-671.
McClements D.J., 1999. Food emulsions: principles, practice and techniques. Boca Raton, FL, USA: CRC Press.
Mutoh T.-A. et al., 2001. Relationship between characteristics of oil droplets and solidification of thermally treated creams. J. Am. Oil Chem. Soc., 78(2), 177-182.
Nesaretnam K., Robertson N., Basiron Y. & Machphie C.S., 1993. Application of hydrogenated palm kernel oil and palm stearin whipping cream. J. Sci. Food Agric., 61, 401-407.
Oil World, 2011. Oil World Annual 2011. Hamburg, Germany: ISTA Mielke GmbH.
Reiffers-Magnani C.K., Cuq J.L. & Watzke H.J., 1999. Composite structure formation in whey protein stabilized O/W emulsions. I. Influence of the dispersed phase on viscoelastic properties. Food Hydrocolloids, 13, 303-316.
Relkin P., Ait-Taleb A., Sourdet S. & Fosseux P-Y., 2003. Thermal behavior of fat droplet as related to adsorbed milk proteins in complex food emulsions. A DSC study. J. Am. Oil Chem. Soc., 80(8), 741-746.
Relkin P. & Sourdet S., 2005. Factors affecting fat droplet aggregation in whipped frozen protein-stabilized emulsions. Food Hydrocolloids, 19, 503-511.
Riaublanc A. et al., 2005. Impact des cristaux de matière grasse sur l'aptitude au foisonnement et la stabilité des émulsions laitières foisonnées. Sci. Aliments, 25(5-6), 427-441.
Richard S., 2005. Friesland Madibic Food Service lance la « crème végétale ». RIA, 657, 51.
Sánchez C.C. & Rodríguez Patino J.M., 2005. Interfacial, foaming and emulsifying characteristics of sodium caseinate as influenced by protein concentration in solution. Food Hydrocolloids, 19, 407-416.
Scher J., 2006. Rhéologie, texture et texturation des produits alimentaires. Tech. Ing., article [F 3 330].
Schorsch C., 2007. Formulation des mousses laitières. Tech. Ing., article [J 2 268].
Shamsi K., Che Man Y.B., Yusoff M.S.A. & Jinap S., 2002. A comparative study of dairy whipping cream and palm oil-based whipping cream in terms of FA composition and foam stability. J. Am. Oil Chem. Soc., 79(6), 583-588.
Shim S.Y., Ahn J. & Kwak H.S., 2004. Functional properties of cholesterol-removed compound whipping cream by palm oil. Asian-Austr. J. Anim. Sci., 17(6), 857-862.
Sourdet S., Relkin P. & Cesar B., 2003. Effects of milk protein type and pre-heating on physical stability of whipped and frozen emulsions. Colloids Surf., B, 31, 55-64.
Spagnuolo P.A., Dalgleish D.G., Goff H.D. & Morris E.R., 2005. Kappa-carrageenan interactions in systems containing casein micelles and polysaccharide stabilizers. Food Hydrocolloids, 19, 371-377.
Stanley D.W., Goff H.D. & Smith A.K., 1996. Texture-structure relationship in foamed dairy emulsions. Food Res. Int., 29(1), 1-13.
Sugimoto T. et al., 2001. Effects of fat crystallization on the behavior of proteins and lipids at oil droplet surfaces. J. Am. Oil Chem. Soc., 78(2), 183-188.
Surh J., Decker E.A. & McClements D.J., 2006. Influence of pH and pectin type on properties and stability of sodium-caseinate stabilized oil-in-water emulsions. Food Hydrocolloids, 20, 607-618.
Tadros T., 2004. Application of rheology for assessment and prediction of the long-term physical stability of emulsions. Adv. Colloid Interface Sci., 108/109, 227-258.
Thivilliers F., 2007. Gels d’émulsions à base d’huiles cristallisables : mécanismes de formation et propriétés rhéologiques. Thèse de doctorat : Université Bordeaux 1 (France).
Towler C., 1982. Cream products for the consumer. New Zeal. J. Dairy Sci. Technol., 17, 191-202.
Van Aken G.A., 2001. Aeration of emulsions by whipping. Colloids Surf., A, 190, 333-354.
Vanderghem C., Danthine S., Blecker C. & Deroanne C., 2007. Effect of proteose-peptone addition on some physico-chemical characteristics of recombined dairy creams. Int. Dairy J., 17, 889-895.
Van Lent K., Le C.T., Vanlerberghe B. & Van der Meeren P., 2008. Effect of formulation on the emulsion and whipping properties of recombined dairy cream. Int. Dairy J., 18, 1003-1010.
Vega C., Dalgleish D.G. & Goff H.D., 2005. Effect of κ-carrageenan addition to dairy emulsions containing sodium caseinate and locust bean gum. Food Hydrocolloids, 19, 187-195.
Walstra P., 1983. Physical chemistry of milk fat globules. In: Fox P.F., ed. Developments in dairy chemistry. 2: Lipids. London: Applied Science Publishers, 119-154.
Wan Rosnani A.I., Nor Aini I. & Noor Lida H.M.D., 2008. Palm-based trans-free whipped toppings as an alternative to dairy cream. Palm Oil Dev., 48, 20-25.
Zamorano J., 2006. Carraghénanes : agents gélifiants, épaississants et stabilisants. Tech. Ing., article [F 5 050].
Notes
Pour citer cet article
A propos de : Prudent Placide Anihouvi
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Science des Aliments et Formulation. Passage des Déportés, 2. B- 5030 Gembloux (Belgique). E-mail : ppanihouvi@student.ulg.ac.be
A propos de : Sabine Danthine
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Science des Aliments et Formulation. Passage des Déportés, 2. B- 5030 Gembloux (Belgique).
A propos de : Gaoussou Karamoko
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Science des Aliments et Formulation. Passage des Déportés, 2. B- 5030 Gembloux (Belgique).
A propos de : Christophe Blecker
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Science des Aliments et Formulation. Passage des Déportés, 2. B- 5030 Gembloux (Belgique).






