- Startpagina tijdschrift
- Volume 19 (2015)
- numéro 4
- Maitrise du risque lié à Vibrio parahaemolyticus dans les produits halieutiques destinés à l’exportation : cas d’une usine sénégalaise de pêche
Weergave(s): 3280 (27 ULiège)
Download(s): 424 (5 ULiège)
Maitrise du risque lié à Vibrio parahaemolyticus dans les produits halieutiques destinés à l’exportation : cas d’une usine sénégalaise de pêche

Nota's van de redactie
Reçu le 22 juillet 2014, accepté le 11 mai 2015
Résumé
Description du sujet. L’article traite de la mise en œuvre de procédures assainissantes fondées sur le HACCP dans une entreprise sénégalaise spécialisée dans l’exportation de produits halieutiques.
Objectifs. L’objectif de l’étude est la maitrise du risque Vibrio parahaemolyticus dans les produits halieutiques sénégalais exportés en Europe.
Méthode. L’étude a porté sur 101 échantillons de produits finis qui ont été analysés par la méthode ISO 8914:1990 pour apprécier la présence de souches pathogènes de V. parahaemolyticus. Le procédé de fabrication initial a ensuite été modifié en renforçant les bonnes pratiques d’hygiène et les traitements assainissants au chlore. Le nouveau procédé a été testé avec 26 échantillons pour apprécier son efficacité. Les 26 échantillons ont été analysés en utilisant la même méthode ISO 8914:1990.
Résultats. Sur les 101 échantillons provenant du premier procédé de fabrication, des souches de Vibrio parahaemolyticus ont été isolées à un taux de 6,9 %. Elles étaient toutes porteuses des gènes tlh, mais dépourvues des gènes de virulence tdh et trh. Toutefois, aucune souche de Vibrio cholerae ou de Vibrio vulnificus n’ont été détectées. Le nouveau procédé a significativement réduit le taux de présence de V. parahaemolyticus sur le produit fini puisqu’un contrôle effectué sur 26 échantillons a démontré l’absence de Vibrio spp. dès l’étape de l’isolement bactériologique.
Conclusions. La mise en œuvre rigoureuse des Bonnes Pratiques d’Hygiène et de Fabrication et le renforcement des traitements assainissants au chlore ont permis de réduire significativement le taux de Vibrio spp. sur les produits finis.
Abstract
Control of Vibrio parahaemolyticus risk in exported seafood products: Case of a Senegalese fishing factory
Description of the subject. The article deals with the implementation of sanitizing procedures based on HACCP in a Senegalese company specialized in exporting seafood products.
Objectives. The objective of the study was to improve the risk control of Vibrio parahaemolyticus in Senegalese seafood products exported to Europe.
Method. The study focused on 101 samples of finished products, which were analyzed using the ISO 8914:1990 method, to assess the presence of pathogenic V. parahaemolyticus. The initial manufacturing process was then modified by increasing good hygiene practices and sanitizing chlorine treatments. The new process was tested with 26 samples to assess its effectiveness. The 26 samples were analyzed using the same method, ISO 8914:1990.
Results. Of the 101 samples obtained from the first manufacturing method, V. parahaemolyticus strains were isolated at a rate of 6.9%. All of these were found to possess the tlh, but not the tdh or trh genes. However, no strains of Vibrio cholerae or Vibrio vulnificus were detected. The new process significantly reduced the rate of V. parahaemolyticus detected in the finished products, as evidenced by the 26 checks on product samples, which showed the absence of Vibrio spp. strains from the bacteriologic isolation stage.
Conclusions. The rigorous implementation of good hygiene and manufacturing practices and the reinforcement of sanitizing chlorine treatments significantly reduced the rate of V. parahaemolyticus in the finished products.
Inhoudstafel
1. Introduction
1Avec une façade maritime d’environ 718 km, le Sénégal est la partie de l’Afrique de l’Ouest la plus avancée dans l’océan Atlantique. Cette région maritime occidentale, réputée très poissonneuse (PNUE, 2004 ; FAO/COPACE/COREP, 2010) confère au pays une position stratégique dans le cadre de l’exploitation et du commerce international des produits de la mer (Figure 1). Avec 301 milliards de francs CFA (environ 460 millions d’euros) de chiffre d’affaires en 2011, la pêche maritime contribue au PIB national et aux recettes d’exportation respectivement pour 1,3 % et 12,3 % (ANSD, 2013). Aujourd’hui, le secteur emploie environ 17 % de la main-d’œuvre nationale.
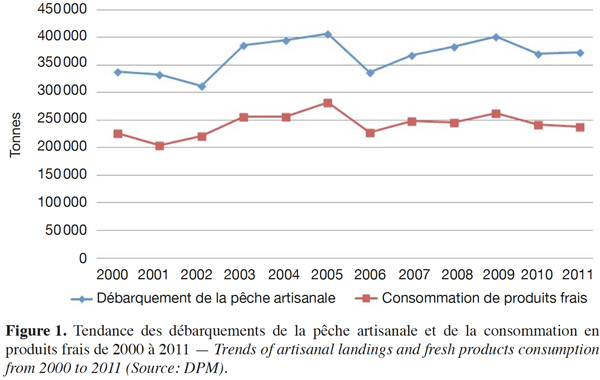
2De 1970 à nos jours, le volume des débarquements a été multiplié quasiment par 10 passant de 50 000 t à plus de 450 000 t (ANSD, 2007 ; 2008 ; 2009 ; 2010 ; 2011 ; 2013). En effet, la pêche occupe une place de choix dans l’économie et la société sénégalaises du fait de sa contribution à l’équilibre de la balance des paiements, à la baisse du chômage et à la couverture des besoins en protéines de la population sénégalaise (ANSD, 2007 ; 2008 ; 2009 ; 2010 ; 2011 ; 2013).
3En aout 2013, 136 unités agréées pour pratiquer le mareyage à l’exportation ont été recensées au Sénégal. Toutefois, l’Union européenne subordonne l’importation à partir d’un pays tiers de produits de la pêche dans le marché de l’Union, à la mise en place d’un programme de gestion de la qualité basé sur le système « Hazard Analysis Critical Control Point » (HACCP). Malgré les efforts consentis et les progrès réalisés dans ce domaine par la plupart des structures exportatrices au Sénégal, les rapports des missions de l’Office Alimentaire et Vétérinaire montrent que le Sénégal devrait offrir des garanties suffisantes concernant les conditions sanitaires des produits de la pêche destinés à être importés dans l’UE (DG[SANCO], 2010; DG[SANCO], 2013). D’ailleurs, ces 15 dernières années, la détection de Vibrio spp. pathogènes dans les produits halieutiques sénégalais présentés à l’importation dans le marché de l’Union européenne a été à l’origine de cinq alertes sanitaires (Ministère de l’Économie Maritime/D.I.T.P/D.I.C, 2011). En outre, de 1971 à nos jours, le Sénégal a enregistré plusieurs épidémies de choléra dont les quatre dernières ont affecté environ 50 000 personnes, en faisant quasiment un millier de morts. L’origine de la contamination était souvent les aliments et/ou l’eau (Diop et al., 1991 ; Sow et al., 1997 ; Aidara et al., 1998 ; MSPM/OMS/UNICEF/CROIX ROUGE, 2006 ; Ndour et al., 2006). Les analyses de laboratoire effectuées au cours de ces épidémies ont souvent montré la coexistence de souches de Vibrio cholerae avec des souches pathogènes de Vibrio parahaemolyticus (Miyamoto et al., 1969 ; Barker et al., 1974 ; Sow et al., 1997).
4En France, l’instruction technique DGAL/SDSSA/2014-487 du 24 juin 2014 (Ministère de l’Agriculture, de l’Agroalimentaire et de la Forêt, 2014), qui abroge la note de service DGAL/SDSSA/MCSI/N2004-8255 du 28 octobre 2004 (Ministère de l’Agriculture, de l’Alimentation, de la Pêche et des Affaires rurales, 2004), fixe la conduite à tenir ainsi que les mesures à appliquer lors des contrôles officiels des produits de la pêche et des coquillages contaminés par des Vibrio. Pour sa part, le comité du codex sur l’hygiène alimentaire, lors de sa 37e session tenue à Buenos Aires, en Argentine en mars 2005, a considéré V. parahaemolyticus comme un important pathogène bactérien véhiculé par les produits halieutiques (FAO/OMS, 2005 ; Martinez-Urtaza et al., 2005).
5Le genre Vibrio contient une dizaine d’espèces pathogènes pour l'homme. Mais celles qui sont les plus citées dans les maladies d’origine alimentaire sont Vibrio parahaemolyticus, Vibrio cholerae et Vibrio vulnificus (FAO/OMS, 2010 ; López-Hernández et al., 2014 ; Haendiges et al., 2015). L’espèce la plus connue est V. cholerae, l’agent du choléra, qui peut se retrouver aussi bien dans les eaux douces que dans les milieux marins et estuariens (Alam et al., 2014), alors que les autres espèces du genre sont inféodées aux environnements marins et estuariens. Les souches de V. parahaemolyticus possédant au moins un des gènes d’hémolysine à l’origine de leur pathogénicité (hémolysines TDH et/ou TRH) et V. cholerae sont principalement isolés dans des cas de gastro-entérite imputables à la consommation d'aliments contaminés ou d'eau contaminée (V. cholerae). La recherche des gènes codant pour les hémolysines TDH ou TRH est indispensable pour prouver le caractère pathogène de V. parahaemolyticus, alors que le gène tlh est présent dans toutes les souches de V. parahaemolyticus (Peterson, 2000). Concernant V. cholerae, les souches reconnues responsables du choléra sont celles appartenant aux sérogroupes O1 et O139 ou les souches de V. cholerae non O1 ou non O139, mais possédant le gène ctx codant pour la toxine cholérique. L’étude de leur sérologie et/ou la détection du gène ctx sont indispensables pour établir leur caractère pathogène ou non. Vibrio vulnificus est principalement signalé comme la cause d'infections extra intestinales (septicémies, blessures, etc.) et les cas de septicémie primaire dus à V. vulnificus sont souvent associés à la consommation de produits de la pêche (FAO/OMS, 2009b). Ainsi, la présence de souches pathogènes de Vibrio spp. dans les produits de la pêche est devenue une préoccupation majeure dans le cadre du commerce international des produits de la pêche régi par des normes sanitaires réactualisées et strictes (FAO/OMS, 2009a ; FAO/OMS, 2009b ; WHO/FAO, 2011 ; Wang et al., 2015).
6La présente étude a été menée dans une entreprise sénégalaise spécialisée dans la transformation et l’exportation de produits halieutiques. Le but visé était d’étudier l’impact des mesures d’hygiène et des traitements assainissants sur la maitrise du risque lié aux espèces pathogènes du genre Vibrio, notamment V. parahaemolyticus. Ceci, aux fins de contribuer à la réduction des alertes sanitaires dues à ces pathogènes.
2. Matériel et méthodes
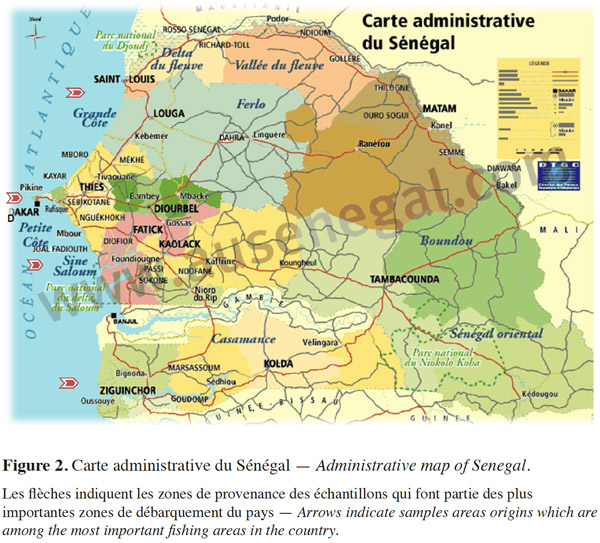
7Ce travail a été mené au Sénégal entre avril 2005 et aout 2007, dans un établissement de traitement et d’exportation de produits halieutiques. Les produits traités dans cette entreprise proviennent des grandes zones de débarquement situées le long du littoral du Sénégal (Figure 2) : Saint Louis au Nord, Dakar et la petite côte (Mbour-Joal-Djiffer) au Centre et Ziguinchor au Sud.
2.1. Échantillonnage
8L’étude a consisté à rechercher les souches pathogènes de Vibrio spp. dans les produits élaborés destinés à l’exportation (crevettes et filets de poisson). Les échantillons étaient prélevés au hasard sur le stock de produits finis congelés (boites de 1 kg ou de 2 kg par échantillon). Après prélèvement au niveau de la section démoulage des produits congelés, les échantillons ont été placés dans des glacières isothermes et acheminés au laboratoire pour y être analysés dans les quatre heures (délai au cours duquel le produit devait décongeler au réfrigérateur).
9Au total, 101 échantillons ont été prélevés dont 25 de crevettes entières, 45 de crevettes décortiquées, 22 de filets de sole et 9 de filets de rouget.
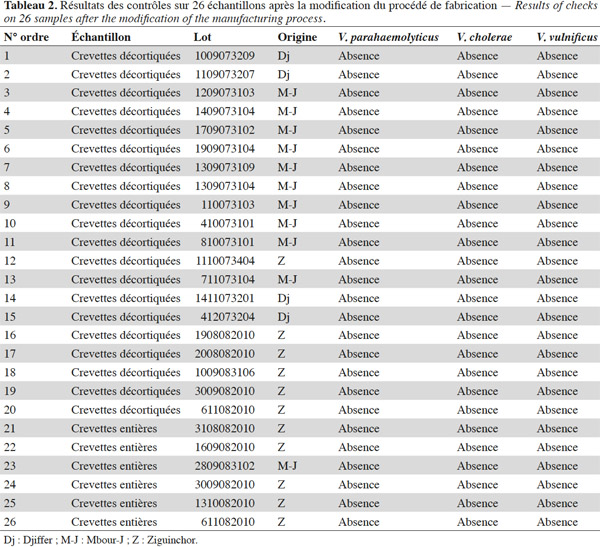
10Les résultats obtenus après analyse des 101 échantillons poussèrent le département qualité et productions de l’entreprise à modifier le procédé de fabrication des produits élaborés. Un contrôle portant sur 26 échantillons fabriqués avec le nouveau procédé a été effectué de septembre 2007 à novembre 2008. Les 26 échantillons qui ont été prélevés au hasard sur le stock de produits finis se composaient de 20 échantillons de crevettes décortiquées et de 6 échantillons de crevettes entières.
2.2. Analyse microbiologique
11Préparation de l’échantillon. La méthode ISO 8914:1990 (ISO 8914:1990, 1990) a été utilisée pour l’isolement et l’identification des souches. Quelques modifications ont été apportées à cette technique, comme indiqué sur la figure 3 :
12– le milieu d’isolement dénommé gélose à la tryptone, à la peptone de soja et au chlorure de triphényltétrazolium (TSAT) a été remplacé par le milieu CHROMagar™ Vibrio (meilleure discrimination des Vibrio) ;
13– les galeries Api 20E (BioMérieux, France) ont été préférées aux galeries biochimiques classiques très fastidieuses dans leur mise en œuvre, puisque comportant un grand nombre de tubes à essais à ensemencer et à incuber.
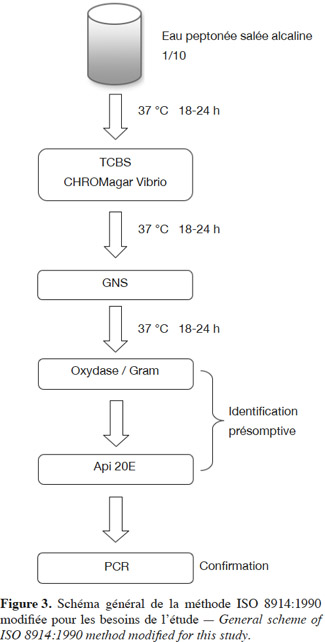
14Vingt-cinq grammes de chaque échantillon ont été prélevés aseptiquement, découpés à l’aide de ciseaux stériles, puis placés dans un sac stomacher et broyés dans un stomacher (HUMEAU laboratoires, France) avec 225 ml d’eau peptonée salée alcaline (3 % NaCl, pH 8,6). Le mélange a été incubé à 37 °C pendant 24 h : c’est l’enrichissement.
15Ensemencement sur milieux d’isolement TCBS et CHROMagar™ Vibrio. À partir de la culture obtenue avec l’enrichissement, la surface d’une gélose TCBS et de CHROMagar™ Vibrio a été ensemencée puis incubée à 37 °C pendant 24 h.
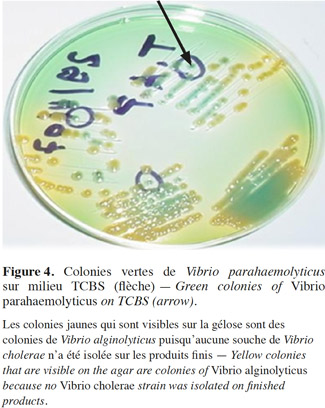
16Sur milieu TCBS, les colonies vertes (saccharose négatif : figure 4) sont présumées appartenir à l’espèce V. parahaemolyticus ou à V. vulnificus, alors que les colonies jaunes (saccharose positif : figure 4) sont présumées appartenir à l’espèce V. cholerae ou à l’espèce Vibrio alginolyticus.
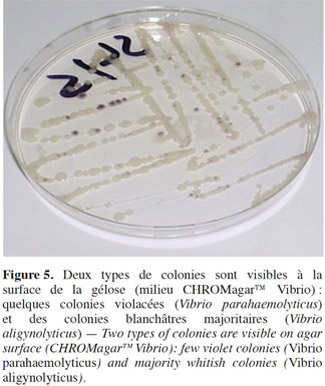
17Sur milieu CHROMagar™ Vibrio, les colonies violettes (Figure 5) sont présumées appartenir à l’espèce V. parahaemolyticus, alors que les colonies bleues sont présumées appartenir à l’espèce V. cholerae ou à l’espèce V. vulnificus.
18Après incubation, cinq colonies caractéristiques ont été prélevées sur chaque milieu d’isolement et ensemencées séparément sur la surface d’une gélose nutritive salée alcaline et incubée pendant 24 h à 37 °C.
19Une colonie bien isolée a été prélevée à partir de chaque boite de gélose nutritive salée alcaline, puis ensemencée dans un tube de gélose nutritive salée alcaline inclinée. Après incubation à 37 °C pendant 24 h, les cultures pures obtenues ont été utilisées pour les tests présomptifs et les essais biochimiques.
20Essai à l’oxydase et coloration de Gram. Une portion de la culture pure a été soumise au test à l’oxydase et à la coloration de Gram. Les souches oxydase positive et Gram- ont été retenues pour les tests de mobilité.
21Examen de la mobilité. Les souches de Vibrio spp. ont montré dans leur majorité une mobilité à l’état frais.
22Les essais biochimiques ont été réalisés à l’aide des galeries Api 20E qui permettent un gain en temps et en efficacité par rapport aux galeries classiques.
23Les souches de V. parahaemolyticus et de V. cholerae isolées à partir des galeries Api 20E doivent faire l’objet d’investigations supplémentaires
24Après l’identification biochimique des souches de V. parahaemolyticus, une caractérisation moléculaire (recherche des gènes tlh, tdh et trh) a été réalisée à l’Institut Pasteur de Dakar.
2.3. Caractérisation moléculaire
25Extraction d’ADN. Les colonies de V. parahaemolyticus obtenues sur gélose nutritive salée alcaline ont été mises à incuber à 37 °C toute une nuit en agitation dans un bouillon Luria-Bertani à 2 % NaCl.
26Après incubation, 1 ml de la culture a été centrifugé à 10 000 tours pendant 7 min. Après centrifugation, le surnageant a été éliminé et le culot a été dissout dans 300 µl de solution tampon (10 M Tris : 1 m MEDTA) puis passé au bain-marie bouillant pendant 10 min. Une centrifugation a ensuite été effectuée à 13 000 tours pendant 5 min, puis le surnageant a été recueilli dans des tubes Eppendorf : c’est l’extrait d’ADN qui a été gardé au frigo entre +2 °C et +4 °C lorsque la PCR devait se faire le même jour. Les extraits d’ADN qui n’ont pas été utilisés le même jour ont été gardés en congélation à -20 °C.
27Analyse PCR. La détection des gènes tlh, tdh et trh a été réalisée selon le protocole décrit par Bej et al. (1999). Les amorces tlh sens et antisens, tdh sens et antisens et trh sens et antisens qui ont été sélectionnées étaient les suivantes :
28– tlh (5'-AAAGCGGATTATGCAGAAGCACTG-3' et 5'-GCTACTTTCTAGCATTTTCTCTGC-3');
29– tdh (5'-GTAAAGGTCTCTGACTTTTGGAC-3' et 5'-TGGAATAGAACCTTCATCTTCACC-3');
30– trh (5-TTGGCTTCGATATTTTCAGTATCT-3' et 5’-CATAACAACATATGCCCATTTCCG-3’).
31Le mélange réactionnel qui était de 50 μl se composait de : tampon Taq polymerase, 200 μM deoxynucleotide triphosphates, 50 pmol de chaque primer (Proligo, Paris, France), 1 U de Taq DNA polymerase et 25 ng d’ADN. L’amplification PCR a été réalisée dans un thermocycleur 2720 (Applied Biosystems, TheNetherlands) en utilisant les paramètres PCR suivants : dénaturation initiale à 94 °C pendant 5 min, suivie par 35 cycles d’amplification de 94 °C pendant 1 min, 57 °C (trh) ou 58 °C (tlh, tdh) pendant 1 min et 72 °C pendant 1 min, avec une extension finale de 72 °C pendant 10 min. Les produits d’ADN amplifiés ont été séparés par migration électrophorétique conventionnelle sur du gel d’agarose visualisée à l’aide de bromure d’éthydium.
32Les souches de V. parahaemolyticus de référence ATCC 43996 (tdh+, trh−) et AQ 4037 (trh+, tdh−) ont été utilisées comme contrôle positif dans tous les tests biochimiques et la PCR.
3. Résultats
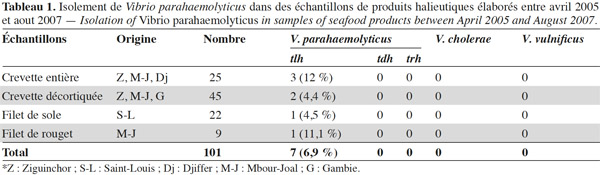
33Vibrio parahaemolyticus a été isolé dans 6,9 % des 101 échantillons analysés, comme illustré sur le tableau 1. En effet, V. parahaemolyticus a été détecté dans 7 échantillons : 3 de crevettes entières, 2 de crevettes décortiquées, 1 de filet de sole et 1 de filet de rouget. En considérant les résultats par type d’échantillon, on constate que V. parahaemolyticus a été détecté dans 12 % des échantillons de crevettes entières, 4,4 % des échantillons de crevettes décortiquées, 4,5 % des échantillons de filets de sole et 11,1 % des échantillons de filets de rouget (Tableau 1). Les recherches ont été faites uniquement sur le produit fini, c'est-à-dire en fin de processus de fabrication. Toutes les souches de V. parahaemolyticus isolées étaient porteuses du gène tlh spécifique de l’espèce. Cependant, aucune d’entre elles n’était porteuse de gène de virulence tdh et/ou trh. La technique d’investigation bactériologique utilisée dans cette étude est basée sur une recherche qualitative (présence/absence) sans dénombrement.
34Les résultats obtenus, présence de V. parahaemolyticus dans 6,9 % des produits finis congelés, ont été jugés élevés par le département qualité et production de l’entreprise. Le procédé de fabrication a alors été modifié aux fins d’arriver à une réduction du taux de présence de V. parahaemolyticus dans le produit fini.
35Après modification du procédé de fabrication, des contrôles ont été effectués sur 26 échantillons dont 20 échantillons de crevettes décortiquées et 6 échantillons de crevettes entières (Tableau 2). Aucun des 26 échantillons contrôlés n’était porteur de souches de Vibrio spp. dès l’étape de l’isolement bactériologique : aucune colonie caractéristique de V. parahaemolyticus ou de V. cholerae ou de V. vulnificus sur TCBS et CHROMagar™ Vibrio.
4. Discussion
36Sur un total de 101 échantillons analysés, V. parahaemolyticus a été isolé dans 6,9 % des échantillons de produits finis, avec un taux d’isolement plus élevé dans la crevette entière (12 %). Ces taux peuvent paraitre élevés pour des produits finis fabriqués au sein d’un établissement appliquant le système HACCP (Hazard Analysis Critical Control Point). En réalité, cette présence relativement élevée de V. parahaemolyticus a été favorisée par un accroissement du risque de contamination croisée lié à une production de crevettes alternée avec des productions de filets de sole et de rouget, sur les mêmes lignes de fabrication. En effet, la crevette peut héberger initialement une importante flore indigène spécifique dont V. parahaemolyticus (Liston, 1980 ; Bourgeois et al., 1996). La mesure qui a été prise pour réduire le taux de présence de V. parahaemolyticus dans les produits finis était la modification du procédé de fabrication (Figures 6 et 7) avec notamment quatre mesures phares :
37– renforcement du glaçage précoce de la crevette et maintien de la chaine du froid des lieux de capture jusqu’à l’usine ;
38– séparation dans l’espace ou dans le temps (nettoyage et désinfection efficaces entre deux opérations différentes) de la ligne de production de la crevette des lignes réservées aux autres espèces ;
39– renforcement des bonnes pratiques de fabrication et d’hygiène au cours de la manutention et du traitement du produit (hygiène du procédé) ;
40– renforcement des traitements assainissants avec une décontamination efficace à la réception (Figure 7) et un renforcement des lavages et des trempages dans une eau glacée (t ≤ 2 °C), contenant un désinfectant autorisé (le chlore), dans les étapes précédant l’emballage.
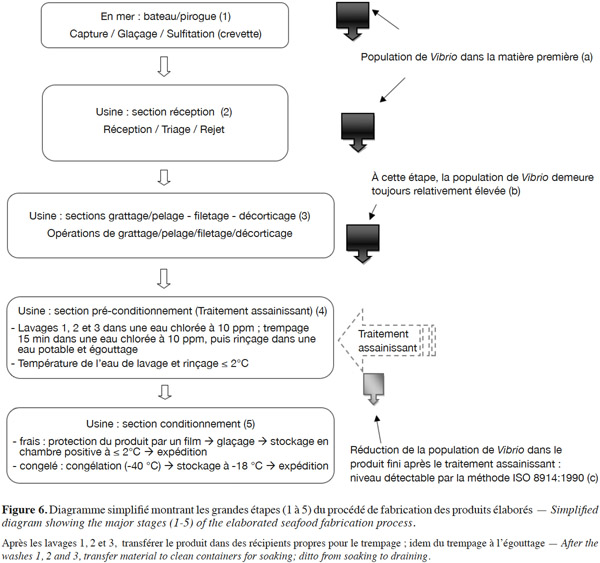
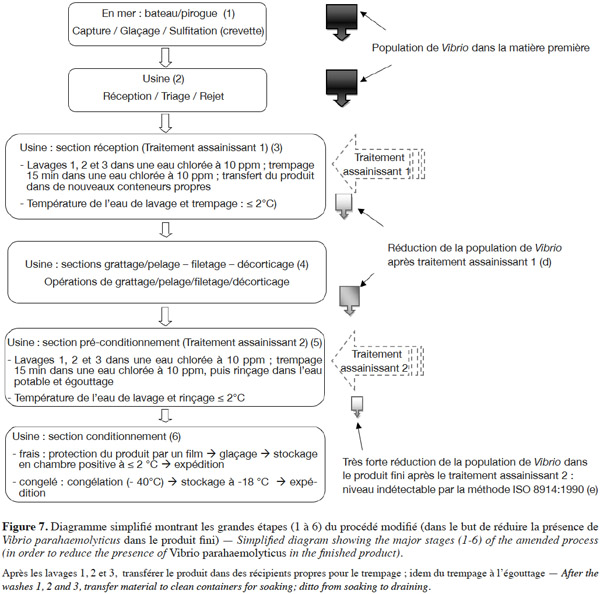
41Suite aux corrections apportées au premier procédé de fabrication (Figures 6 et 7), un contrôle a été réalisé entre septembre 2007 et novembre 2008 pendant les périodes de forte production de crevettes. Le contrôle a porté sur 26 échantillons, comme illustré au tableau 2. Les résultats négatifs obtenus dès l’étape 2 de la figure 3 (isolement sur TCBS et CHROMagar™ Vibrio) sont révélateurs de l’importance des mesures correctives précédemment citées. En effet, la taille de la population de Vibrio dans le produit fini est passée d’un niveau détectable (Figure 6, étape 4) à un niveau indétectable (Figure 7, étape 5) par la même méthode de recherche, c’est-à-dire la méthode ISO 8914:1990. Dans le premier procédé de fabrication, comme le montre la figure 6, il n’y avait pas de traitement assainissant (pas de lavage ni de trempage) à l’étape réception. La seule étape réservée à l’assainissement du produit (étape de pré-conditionnement) ne permettait pas de réduire la population de Vibrio en dessous du seuil de détection par la méthode ISO 8914:1990. Par ailleurs, l’utilisation d’un désinfectant autorisé incorporé dans l’eau de lavage et de trempage a permis de réduire de façon significative la taille de la population de Vibrio spp. dans le produit fini. Le désinfectant utilisé est l’hypochlorite de calcium à une concentration maximum de 10 mg·l-1, comme recommandé par le Codex Alimentarius (FAO/WHO, 2000 ; FAO/WHO, 2008a ; FAO/OMS, 2012). Par ailleurs, tous les ustensiles, surfaces, plans de travail et films qui sont entrés en contact directement ou indirectement avec le produit ont été préalablement désinfectés avec une solution d’hypochlorite de calcium à 100 ppm, puis rinçés avec de l’eau potable ou présentant une faible tension en chlore (1,5 ppm). En effet, la désinfection efficace de toutes les surfaces qui entrent en contact directement ou indirectement avec le produit réduit de façon significative les risques de contaminations croisées qui sont souvent responsables de l’introduction de germes pathogènes en cours de fabrication (FAO/WHO, 2008b ; Santé Canada, 2009 ; EDES/DITP, 2013).
42Les mécanismes par lesquels le chlore agit sur les micro-organismes n’ont pas été entièrement élucidés. Toutefois, d’après bon nombre d’études, la perturbation de la membrane cellulaire et des fonctions vitales du micro-organisme semblent être une étape décisive menant à son inactivation (Bourgeois et al., 1996 ; Santé Canada, 2009). D’après Bourgeois et al. (1996), l’action d’un désinfectant se déroule en quatre étapes principales :
43– entrée en contact du désinfectant avec le micro-organisme ;
44– fixation du désinfectant sur la paroi du micro-organisme ;
45– pénétration du désinfectant à travers la paroi du micro-organisme ;
46– action du désinfectant sur le micro-organisme entrainant une perturbation, voire l’arrêt, de ses fonctions vitales.
47L’efficacité du chlore dépend beaucoup du pH et de la température du milieu aqueux, conditions qui déterminent l’importance de la transformation en l’une ou l’autre des trois espèces chlorées libres, Cl2, HOCl et OCl. À un pH faible, le HOCl (acide hypochloreux) est prédominant et est plus efficace pour inactiver les microbes (Santé Canada, 2009). L’acide hypochloreux est obtenu à partir des réactions chimiques suivantes (WHO/IARC, 1991 ; Connell, 1996 ; White, 1999 ; Santé Canada, 2009) :
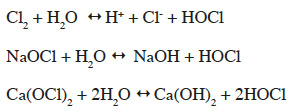
48Cl2 : chlore gazeux ; Cl- : ion chlorure ; NaOCl : hypochlorite de sodium ; Ca(OCl)2 : hypochlorite de calcium.
49Le HOCl se dissocie ensuite en anion hypochlorite (OCl-), selon l’équation chimique :
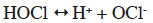
50Toutefois, nombreux sont ceux qui soutiennent que l’utilisation du chlore actif dans la production d’aliments devrait être soumise à des lignes directrices strictes en ce qui concerne le type de composant chloré, la concentration du produit, le stade du processus de production où l’utilisation du chlore est permise, la durée maximale d’application et sa fréquence, ainsi que les types d’aliments pour lesquels l’autorisation est accordée. Les pays de l’Union européenne sont opposés à l’utilisation de niveaux élevés de chlore dans l’industrie du poisson, du fait du risque de formation de dérivés chlorés susceptibles de présenter un danger pour la santé des consommateurs ; d’autre part, ils craignent que le chlore soit utilisé pour masquer de mauvaises pratiques d’hygiène. Par contre, les États-Unis, le Canada et les pays en développement soutiennent une plus large utilisation du chlore pour assurer une meilleure sécurité alimentaire (FAO/WHO, 2000 ; FAO/WHO, 2008a ; Santé Canada, 2009). Toutefois, le traitement au chlore doit obligatoirement être suivi d’un rinçage à l’eau potable aux fins d’éliminer le chlore résiduel.
51Cependant, des études toxicologiques poussées s’avèrent nécessaires sur les niveaux et la réactivité du chlore utilisé dans l’industrie, sur l’identité et la toxicité des dérivés chlorés et sur le niveau d’exposition des consommateurs à ces substances.
52Toutes ces investigations réalisées au sein de l’entreprise ont été rendues possibles par l’existence d’un laboratoire interne d’autocontrôle performant, qui participe par ailleurs aux essais d’inter-comparaison organisés par le Réseau d’Analyse et d’Échange en Microbiologie Alimentaire (RAEMA). Néanmoins, il n’existe pas d’essais RAEMA pour Vibrio. Fondamentalement, l’obligation de sécurité alimentaire incombe aux professionnels qui ont la responsabilité de mettre en place des autocontrôles fondés sur la démarche HACCP, l’absence ou l’inefficacité des autocontrôles pouvant entrainer une perte de maitrise inacceptable de la sécurité sanitaire des productions.
53La maitrise du risque lié à Vibrio spp. dans les produits de la mer est fortement tributaire du respect de la chaine du froid et de la réduction de la flore initiale du produit par des moyens de traitement adéquats. Le respect des bonnes pratiques d’hygiène pendant la transformation des produits halieutiques doit permettre d’éviter les contaminations croisées et les recontaminations après traitement assainissant. Cette démarche est d’ailleurs largement préconisée par les experts du comité mixte du codex sur l’hygiène alimentaire dans différents rapports d’activités (FAO/OMS, 2005 ; FAO/OMS, 2008). La réduction de la charge de Vibrio spp. lors du traitement assainissant des produits halieutiques entraine également une réduction du risque lié aux vibrions pathogènes éventuellement présents. Toutefois, la plupart des souches de V. parahaemolyticus isolées des produits halieutiques et de l’environnement sont dépourvues de gène de virulence tdh et/ou trh. En effet, il est démontré que plus de 99 % de ces souches sont avirulentes (Nishibuchi et al., 1995 ; Islam et al., 2004 ; FAO/OMS, 2005). Néanmoins, quelle que soit l’origine de la souche (clinique ou environnementale), l’analyse PCR est requise pour la détection des gènes de virulence.
54En sus des mesures qui doivent nécessairement être prises au sein des établissements de production et d’exportation à travers la mise en place d’un système d’autocontrôle et de validation des procédés de fabrication, le devoir régalien de l’autorité compétente est de contrôler de façon rigoureuse l’application par les professionnels des dispositions règlementaires en matière de sécurité sanitaire des aliments. Par ailleurs, pour une meilleure stratégie de prévention des risques d’alertes sanitaires dues à la détection de souches pathogènes de Vibrio spp. dans les produits halieutiques sénégalais exportés en Europe, les structures compétentes de l’État doivent mettre en œuvre ou renforcer les plans de surveillance à quatre niveaux :
55– surveillance des productions dans les établissements en réalisant des contrôles microbiologiques et chimiques fréquents ;
56– surveillance des résultats d’analyses de tous les laboratoires impliqués dans l’autocontrôle dans le secteur de la pêche (laboratoires internes des entreprises et laboratoires officiels de contrôle) et surveillance de la fiabilité de ces résultats (mise en place d’un réseau d’inter-comparaison) ;
57– exploitation et suivi rigoureux des informations ayant trait aux alertes sanitaires ;
58– surveillance environnementale.
59Les mauvaises habitudes suivantes doivent être bannies par les pouvoirs publics :
60– le laxisme noté quand il s’agit de faire respecter les normes sanitaires par les établissements agréés pour l’exportation de produits halieutiques ;
61– attendre la « veille » des missions d’inspection de l’Office Alimentaire et Vétérinaire (OAV) de l’UE pour demander aux entreprises de se conformer totalement aux exigences sanitaires.
62Fondamentalement, le HACCP et l’autocontrôle demeurent des outils très puissants en production dans le cadre de la maitrise des risques microbiologiques et de l’amélioration des procédés de fabrication et de leur validation.
Bibliographie
Aidara A. et al., 1998. Phenotypic and genotypic characterization of Vibrio cholerae isolates from a recent cholera outbreak in Senegal: comparison with isolates from Guinea-Bissau. Am. J. Trop. Med. Hyg., 58(2), 163-167.
Alam M.T. et al., 2014. Monitoring water sources for environmental reservoirs of toxigenic Vibrio cholerae O1, Haiti. Emerg. Infect. Dis., 20, 356-363.
ANSD (Agence Nationale de la Statistique et de la Démographie), 2007. Note d’Analyse du Commerce Extérieur. Dakar : ANSD.
ANSD (Agence Nationale de la Statistique et de la Démographie), 2008. Note d’Analyse du Commerce Extérieur. Dakar : ANSD.
ANSD (Agence Nationale de la Statistique et de la Démographie), 2009. Note d’Analyse du Commerce Extérieur. Dakar : ANSD.
ANSD (Agence Nationale de la Statistique et de la Démographie), 2010. Note d’Analyse du Commerce Extérieur. Dakar : ANSD.
ANSD (Agence Nationale de la Statistique et de la Démographie), 2011. Note d’Analyse du Commerce Extérieur. Dakar : ANSD.
ANSD (Agence Nationale de la Statistique et de la Démographie), 2013. Situation économique et sociale du Sénégal. Dakar : ANSD.
Barker W.H. Jr & Gangarosa E.J., 1974. Food poisoning due to Vibrio parahaemolyticus. Annu. Rev. Med., 25, 75-81.
Bej A.K. et al., 1999. Detection of total and hemolysin-producing Vibrio parahaemolyticus in shellfish using multiplex PCR amplification of tlh, tdh and trh. J. Microbiol. Methods, 36, 215-225.
Bourgeois C.M., Mescle J.F. & Zucca J., 1996. Microbiologie alimentaire. Vol. 1 : aspect microbiologique de la sécurité et de la qualité des aliments. 2e éd. Paris : Lavoisier Tec & Doc.
Connell G.F., 1996. Water disinfection series: the chlorination/chloramination handbook. Denver, CO, USA: American Water Works Association.
DG(SANCO), 2010. DG(SANCO) 2010-8545 - RM FINAL. Rapport d’une mission effectuée au Sénégal du 27 avril au 6 mai 2010 afin d’évaluer les systèmes de contrôle en place régissant la production des produits de la pêche destinés à l’exportation vers l’Union européenne. Commission européenne, Direction Générale de la Santé et des Consommateurs.
DG(SANCO), 2013. DG(SANCO) 2013-6708 - RM FINAL. Rapport d’un audit effectué au Sénégal du 22 janvier au 1er février 2013 afin d’évaluer les systèmes de contrôle en place régissant la production des produits de la pêche destinés à l’exportation vers l’Union européenne. Commission européenne, Direction Générale de la Santé et des Consommateurs.
Diop B.M. & Coll-Seck A.M., 1991. Environnement et santé : le choléra à Dakar. Afr. Med., 30, 251-254.
EDES/DITP (Direction des Industries de Transformation de la Pêche), 2013. Guide sectoriel d’autocontrôle (GSAC) pour le secteur Pêche du Sénégal. Version n°1.
FAO/COPACE/COREP, 2010. Rapport de l’atelier sous-régional FAO FISHCODESTP/COPACE/COREP visant à améliorer l’information sur la situation et les tendances des pêches de capture dans le golfe de Guinée, Douala, Cameroun, 15-18 avril 2008. Rome : FAO, www.fao.org/docrep/012/k7440f/k7440f00.pdf, (20/08/2015).
FAO/OMS, 2005. CX/FH 05/37/13. Document de travail sur les stratégies de gestion des risques présentés par Vibrio spp. dans les poissons et fruits de mer, 37e session, 14-19 mars 2005, Buenos Aires, Argentine. Rome : FAO.
FAO/OMS, 2008. CX/FH 08/40/1. Programme mixte FAO/OMS sur les normes alimentaires, 40e session, 1-5 December 2008, Guatemala City, Guatemala. Rome : FAO.
FAO/OMS, 2009a. CX/FH 09/41/6. Avant-projet proposé de directives sur l’application des principes généraux d’hygiène alimentaires à la maîtrise de Vibrio spp. dans les fruits de mer à l’étape 4, 16-20 Novembre 2009, San Diego, USA. Rome : FAO.
FAO/OMS, 2009b. Alinorm10/33/13. Rapport de la 41e session du comité du codex sur l'hygiène alimentaire, 16-20 novembre 2009, San Diego, USA. Rome : FAO.
FAO/OMS, 2010. CAC/GL 73, 2010. Directives sur l’application des principes généraux en matière d’hygiène sur la maîtrise de Vibrio spp. dans les fruits de mer. Rome : FAO.
FAO/OMS, 2012. CAC/RCP 52-2003, 2012. Code d’usages pour les poissons et les produits de la pêche. 2e éd. Rome : FAO.
FAO/WHO, 2000. The use of chlorine in fish processing: safety and risks. Infofish Int., 3, 58-62.
FAO/WHO, 2008a. Code of practice for fish and fishery products. CAC/RCP 52, adopted 2003, revision 4. Roma: FAO.
FAO/WHO, 2008b. Benefits and risks of the use of chlorine-containing disinfectants in food processing. Report of a Joint FAO/WHO Expert Meeting, 27-30 May 2008, Ann Arbor, MI, USA. Roma: FAO.
Haendiges J. et al., 2015. Characterization of Vibrio parahaemolyticus clinical strains from Maryland (2012-2013) and comparisons to a locally and globally diverse V. parahaemolyticus strains by whole-genome sequence analysis. Front. Microbiol., 6, article 125, doi: 10.3389/fmicb.2015.00125
Islam M.S. et al., 2004. Pandemic strains of O3:K6 Vibrio parahaemolyticus in the aquatic environment of Bangladesh. Can. J. Microbiol., 50, 827-834.
ISO 8914:1990, 1990. Microbiology - General guidance for the detection of Vibrio parahaemolyticus. ISO TC 34/SC 9. France: AFNOR.
Liston J., 1980. Microbiology in fishery science. In: Connel J.J., ed. Advanced in fish science and technology. Farnham, UK: Fishing News book Ltd, 138-157.
López-Hernández K.M., Pardío-Sedas V.T. & Williams J.J., 2014. Evaluación del riesgo microbiológico a Vibrio spp. en alimentos de origen marino en México. Salud Publ. Mex, 56, 295-301.
Martinez-Urtaza J. et al., 2005. Pandemic Vibrio parahaemolyticus O3:K6, Europe. Emerg. Infect. Dis., 11, 1319-1320.
Ministère de l’Agriculture, de l’Agroalimentaire et de la Forêt, 2014. Instruction technique DGAL/SDSSA/2014-487 du 24 juin 2014. Paris : Ministère de l’Agriculture, de l’Agroalimentaire et de la Forêt.
Ministère de l’Agriculture, de l’Alimentation, de la Pêche et des Affaires rurales, 2004. Note de service DGAL/SDSSA/MCSI/N2004-8255 du 28 octobre 2004. Classement : SSA373/72 et EI 333-62. Paris : Ministère de l’Agriculture, de l’Alimentation, de la Pêche et des Affaires rurales.
Ministère de l’Économie Maritime/D.I.T.P/D.I.C, 2011. Bilan des alertes sanitaires de l’Union européenne de 1999 à 2010 suivies par l’autorité compétente. Dakar : Ministère de l’Économie Maritime.
MSPM/OMS/UNICEF/CROIX ROUGE, 2006. Mission conjointe dans la région de Diourbel : épidémie de choléra au Sénégal. Dakar : Ministère de la Santé et de la Prévention Médicale du Sénégal.
Miyamoto Y. et al., 1969. In vitro hemolytic characteristic of Vibrio parahaemolyticus: its close correlation with human pathogenicity. J. Bacteriol., 100, 261-266.
Ndour C.T. et al., 2006. L’épidémie de choléra de 2004 à Dakar : aspects épidémiologiques, cliniques et thérapeutiques. Med. Trop., 66, 33-38.
Nishibuchi M. & Kaper J.B., 1995. Thermostable direct hemolysin gene of Vibrio parahaemolyticus: a virulence gene acquired by a marine bacterium. Infect. Immun., 63, 2093-2099.
Peterson K.M., 2000. Molecular pathogenesis of Vibrio infections. In: Cary J.W., Linz J.E., Bhatnagar D., eds. Microbial foodborne diseases, mechanisms of pathogenesis and toxin synthesis. Lancaster, PA, USA: Technomic Publishing Co, 157-185.
PNUE (Programme des Nations Unies pour l’Environnement), 2004. Mise en œuvre de mesures de conservation et gestion durables des ressources halieutiques : le cas du Sénégal. UNEP/ETP/2004/11.
Santé Canada, 2009. Recommandations pour la qualité de l’eau potable au Canada : document technique – Le chlore. N° de catalogue H128-1/09-588F. Ottawa, On, Canada : Santé Canada.
Sow A.I. et al., 1997. Diversité bactérienne au cours de l’épidémie de choléra à Dakar, Sénégal (1995-1996). Bull. Soc. Pathol. Exot., 90, 160-161.
Wang W., Li M. & Li Y., 2015. Intervention strategies for reducing Vibrio parahaemolyticus in seafood: a review. J. Food Sci., 80, 1.
White G.C., 1999. Handbook of chlorination and alternative disinfectants. 4th ed. New York, NY, USA: John Wiley & Sons.
WHO/FAO, 2011. Risk assessment of Vibrio parahaemolyticus in seafood: interpretative summary and technical report. Microbiological Risk Assessment Series No. 16. Roma: FAO.
WHO/IARC, 1991. Evaluation of carcinogenic risks to humans. Vol 52: chlorinated drinking water, chlorinated by-products, some other halogenated compounds, cobalt and cobalt compounds. Lyon, France: IARC.






