- Startpagina tijdschrift
- Volume 15 (2011)
- numéro 1
- Synthèse des connaissances sur la déshydratation osmotique
Weergave(s): 20727 (73 ULiège)
Download(s): 1955 (4 ULiège)
Synthèse des connaissances sur la déshydratation osmotique

Nota's van de redactie
reçu le 18 janvier 2010, accepté le 24 juin 2010
Résumé
Parmi les procédés de conservation des produits végétaux, la déshydratation osmotique présente un intérêt économique et nutritionnel certain. Cette technique, économe en énergie, est susceptible de prolonger la période de disponibilité des produits alimentaires et leur confère des propriétés sensorielles nouvelles et appréciées. Elle permet ainsi aux acteurs de la filière agro-alimentaire d'écouler leurs productions à de meilleurs prix et aux consommateurs d'en disposer tout au long de l'année. Cette technique est un outil facile à mettre en place, surtout dans les pays en voie de développement, en raison de son faible cout. Le présent article a pour objectif de présenter une synthèse de la littérature concernant la technique de déshydratation osmotique afin d'en rappeler les bases théoriques et pratiques, mais aussi d'en préciser les nouvelles tendances et voies de recherches récentes.
Abstract
Synthesis of knowledge about osmotic dehydration. Among the preservation processes of vegetal products, osmotic dehydration presents an economic and a nutritional interest. This technique consumes a low quantity of energy, prolongs the period of availability of foodstuffs, and gives new and appreciated sensory properties to products. Therefore, the producers can sell their productions at better prices and the consumers are able to consume fruits and vegetables throughout the year. This technique is very easy to set up, especially in the developing countries due to its low cost. The aim of this article is to present a synthesis of the literature concerning the osmotic dehydration technique, and also to specify the new tendencies and directions of recent research.
Inhoudstafel
1. Introduction
1Les industriels du secteur agro-alimentaire sont aujourd'hui confrontés à deux problèmes majeurs : d'une part, l'attente croissante des consommateurs pour des produits de haute qualité nutritionnelle et organoleptique et, d'autre part, l'augmentation des couts énergétiques. En réponse à ces défis, les techniques de stabilisation et de conservation des aliments, telles que le séchage ou les techniques du froid, connaissent des améliorations constantes et sont de mieux en mieux intégrées aux filières industrielles.
2Une catégorie de méthodes de séchage fait intervenir une ou plusieurs étapes de mise en contact des denrées avec une solution aqueuse concentrée en sels (par exemple, saumurage des légumes, viandes, poissons ou fromages), en acide (par exemple, marinage des produits carnés) ou en sucres (confisage et semi-confisage des fruits). Ce traitement vise à réduire, à moindre cout, le risque d'altération de la qualité nutritionnelle et organoleptique du produit traité (Ade-Omowaye et al., 2003). Le confisage est une des techniques traditionnelles dont les développements récents ont donné naissance aux procédés dits de « déshydratation osmotique » (DO) ou de « déshydratation-imprégnation par immersion » (DII) (Albagnac et al., 2002).
3La déshydratation osmotique présente un certain nombre d'atouts par rapport aux techniques traditionnelles de séchage. En particulier, l'aliment est traité à plus basse température (entre 5 et 85 °C) et à l'abri de l'oxygène (puisqu'il est immergé), ce qui est particulièrement favorable pour les produits sensibles aux réactions de dégradation oxydative et thermique (Lerica et al., 1985 ; Garcia-Segovia et al., 2010).
4De plus, la DO permet de reduire la charge microbienne et ainsi de prolonger la période de conservation des produits (Castello et al., 2009).
5La déshydratation osmotique est attribuée au phénomène d'osmose qui se manifeste à travers les membranes cellulaires « semi-perméables » (perméables à l'eau, mais moins aux solutés) des tissus. Raoult-Wack (1994) a montré que le moteur de ce transfert est une différence de concentration entre la solution et le matériau à traiter. Il se traduit par deux écoulements simultanés à contre-courant : une diffusion de l'eau des cellules du produit (la solution la moins concentrée) vers la solution hypertonique où l'aliment est plongé (déshydratation) et une entrée de soluté de la solution vers l'aliment (imprégnation). L'aliment peut ainsi perdre jusqu'à 50 % de la teneur initiale en eau en moins de trois heures (Lerica et al., 1985). La sortie d'eau s'accompagne généralement d'une perte de solutés propres au produit alimentaire. Ce transfert, quantitativement négligeable par rapport aux deux premiers, soulève des critiques quant à son impact sur les qualités organoleptiques et nutritionnelles du produit transformé (Albagnac et al., 2002).
6Afin d'améliorer l'efficacité du processus de déshydratation osmotique, divers traitements peuvent être appliqués pour faciliter la diffusion de l'eau : ultrasons, irradiation, champ électrique pulsé, etc. Pour une conservation de très longue durée, le produit obtenu après déshydratation osmotique peut encore subir un traitement complémentaire, tel qu'un séchage à l'air ou une congélation (Garcia-Segovia et al., 2010).
7Employée industriellement depuis les années 1960, la DO fait récemment l'objet d'un certain regain d'intérêt. Au cours de la dernière décennie, la progression constante du nombre d'articles scientifiques publiés annuellement sur le sujet en témoigne. Le présent travail se propose de rappeler les bases de la déshydratation osmotique, d'exposer les différents facteurs influençant ce processus et de présenter les dernières avancées scientifiques en termes d'amélioration des performances de la technique.
2. Généralités sur la déshydratation osmotique
2.1. Cinétique de la déshydratation osmotique
8Les cinétiques de transfert de matière dans les produits végétaux (Tableaux 1 et 2) peuvent se décomposer en deux phases : une première phase, responsable de l'essentiel des transferts d'eau et de solutés, suivie d'une seconde phase, pendant laquelle la perte en eau ralentit fortement tandis que les débits d'entrée en solutés continuent d'augmenter régulièrement (Kowalska et al., 2008). Il semble probable que les membranes cellulaires soient victimes d'une perte de leur caractère semi-perméable, permettant progressivement aux solutés de pénétrer dans la cellule (Raoult-Wack, 1994). La durée de la première phase est très variable suivant le produit traité, d'une demi-heure à deux heures dans les conditions les plus courantes (morceaux de petites tailles, de l'ordre du cm3). Ces transferts se déroulent à travers les parois et membranes cellulaires du produit. À l'intérieur de ces derniers, les espaces intercellulaires servent de lieux d'accumulation ou de passage pour les substances échangées (Raoult-Wack, 1994 ; Lenart, 1996 ; Kowalska et al., 2008).
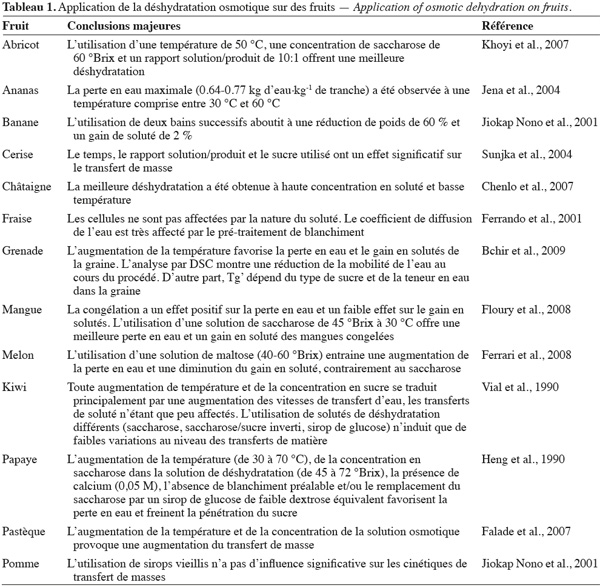

9Deux approches sont employées afin d'étudier la cinétique de la déshydratation osmotique :
10– L'approche classique qui se base sur la détermination de deux paramètres. En effet, des travaux antérieurs ont prouvé que deux paramètres peuvent quantitativement représenter le processus osmotique. Ces paramètres sont la perte d'eau (« Water loss », WL), indiquant l'eau qui sort du matériel cellulaire vers la solution et le gain en solides (« Solids Gain », SG). Ces paramètres sont habituellement déterminés par la mesure des solides totaux ou par analyse chimique (Krokida et al., 2000 ; Riva et al., 2005 ; Garcia-Segovia et al., 2010).
11Dans la littérature, des travaux de modélisation ont recours au coefficient de diffusion (Deff) issu de l'équation de Fick (Eq. 1) (Crank, 1975) :

12où m est le flux de matière traversant la surface S pendant l'unité de temps t (kg.s-1) ; S est la section normale à la direction du flux (m²) ; C est la concentration (kg.m-3); Deff est le coefficient de diffusion (m².s-1) ; x est la distance sur un axe parallèle à la direction du flux (m).
13– L'approche fine qui se base sur l'étude des paramètres déterminés à partir de la calorimétrie différentielle à balayage et la résonance magnétique nucléaire (RMN).
14Ces techniques permettent d'approcher les liaisons de l'eau dans le produit.
15Calorimétrie différentielle à balayage. La calorimétrie différentielle à balayage (« differential scanning calorimetry », DSC) est une méthode thermo-analytique permettant la mesure de propriétés physiques d'un échantillon soumis à un programme de température. Le principe de la DSC est de comparer le flux de chaleur nécessaire pour maintenir la température d'un échantillon (capsule contenant l'échantillon) égale à celle d'une référence (capsule vide), chauffés ou refroidis à une vitesse contrôlée. Ce flux de chaleur à une température donnée est directement proportionnel à la chaleur spécifique (Cp) du matériau à cette température (Eq. 2) :

16où Q est le flux de chaleur absorbé ou libéré par l'échantillon (mW.g-1), Cp est la chaleur spécifique de l'échantillon (J.g-1), T est la température (°C), t le temps et f(t,T) est une fonction dépendante du temps et de la température.
17Des transformations thermodynamiques de 1er ordre, comme la cristallisation ou la fusion, vont se traduire respectivement par un pic exothermique de cristallisation ou un pic endothermique de fusion. La position de ces pics indique la température de transformation (T°fusion ou T°cristallisation) ; leur aire est proportionnelle à l'enthalpie du processus. Une transformation de 2è ordre sera caractérisée par une marche, trahissant un saut de Cp, dont le point d'inflexion correspond à la température de transition vitreuse (Tg). Cette transition est, au chauffage, le changement réversible de la phase amorphe d'un polymère d'une forme vitreuse (relativement dur, à faible mobilité de l'eau) en une forme visqueuse ou caoutchoutique (mou, à plus forte mobilité de l'eau). La transformation est inverse au refroidissement. La détermination de la température de transition vitreuse, la température de fusion et de cristallisation et de l'enthalpie de fusion et de cristallisation au cours du temps permet de quantifier la teneur en eau libre et liée dans le produit, ainsi d'étudier la cinétique de déshydratation du produit (Cornillon, 2000 ; Ohkuma et al., 2008).
18Résonance magnétique nucléaire (RMN). La méthode par RMN repose sur l'analyse de l'interaction entre l'eau et la matrice macromoléculaire. Les molécules d'eau peuvent interagir de manière labile ou permanente, définissant ainsi des compartiments distincts dits d'eau faiblement liée (ou vacuolaire) et d'eau d'hydratation (ou de surface). Au cours des processus d'échange, les protons de l'eau interagissent avec ceux de la matrice soit par échange chimique direct, soit par une interaction magnétique (dipôle-dipôle). Pendant la détection RMN (base résolution impulsionnelle) de l'aimantation des noyaux, certains protons peuvent changer d'état (de compartiment) et cette modification affecte le signal RMN enregistré. Le retour à l'équilibre de l'aimantation est caractérisé par deux temps de relaxation des protons de l'eau. La relaxation T1 ou relaxation spin-réseau caractérise le retour à l'équilibre des populations spins. La relaxation T2 ou spin-spin représente l'amortissement de l'aimantation dans le plan transversal. La détection et l'analyse de cette perturbation (transfert d'aimantation) sont à la base de la quantification des proportions d'eau libre et d'eau d'hydratation, et de l'analyse de la cinétique des échanges entre ces deux systèmes (Riggs et al., 2001). Actuellement, d'autres méthodes comme l'imagerie par résonance magnétique (IRM) sont mises à profit afin d'étudier la structure du produit et de quantifier les échanges internes (Derossi et al., 2008).
2.2. Principaux facteurs influençant les performances de la DO
19Les cinétiques de transfert d'eau et de solutés dépendent de trois facteurs (Rastogi et al., 2004 ; Dermesonlouoglou et al., 2008 ; Garcia-Segovia et al., 2010) :
20– les propriétés intrinsèques des tissus traités : la structure poreuse, la taille, la forme, la superficie du produit,
21– les conditions opératoires de traitement : temps, température de traitement, pression, agitation de la solution, composition de la solution,
22– le mode de mise en contact des phases entre aliment solide et solution liquide.
23Propriétés des tissus biologiques. Tout ce qui est préjudiciable à l'intégrité des tissus, tel qu'une maturation trop avancée, la mise en œuvre de prétraitements thermiques, chimiques ou enzymatiques, peut entraver la perte en eau tout en favorisant le gain en soluté. La grande variabilité observée dans le comportement des végétaux au cours d'un traitement de DO est généralement attribuée aux différentes propriétés tissulaires. Ces dernières incluent la compacité des tissus, l'importance relative des espaces intra- et extra-cellulaires, la porosité et la teneur initiale en matières sèches (Lenart, 1996). En effet, la porosité de l'aliment affecte sa texture et influence sa fermeté. Les changements de porosité causés par le processus osmotique favorisent l'action des forces d'entrainement non diffusionelles telles que des gradients de pression (Nieto et al., 2004). La majorité des produits végétaux (Tableaux 1 et 2) sont découpés en cube ou en sphère avant le traitement de déshydratation osmotique, ce qui facilite le transfert de matière grâce à un contact direct entre les cellules et la solution (Kowalska et al., 2008).
24Lors d'une DO, quelques cellules peuvent devenir non viables, tandis que les autres restent pratiquement inchangées. Les traitements osmotiques impliquent ainsi un stress cellulaire par suite de la réduction de l'eau disponible dans les cellules, ce qui modifie leur physiologie (Rastogi et al., 2004).
25Concentration et composition de la solution osmotique. La différence de concentration en soluté entre le produit à traiter et la solution est le moteur du transfert de masse en DO. La perte en eau est plus importante lorsque cet écart est initialement élevé (Raoult-Wack, 1994). En effet, Vial et al. (1990) ont montré que toute augmentation de la concentration en sucre se traduit principalement par une augmentation des vitesses de transfert d'eau, les transferts de soluté n'étant que peu affectés. Pour la déshydratation des fruits, des solutions de sucre concentrées de 50 à 70 °Brix ont été employées (Lerica et al., 1985 ; Corrêa et al., 2010). Néanmoins, il existe une concentration seuil (entre 50 et 65 °Brix) au-delà de laquelle l'imprégnation décroît (Raoult-Wack, 1994 ; Lenart, 1996).
26La composition des solutions (type, masse moléculaire du soluté) mises en œuvre en DO est un facteur clé du procédé (Corrêa et al., 2010). Les solutions sont préparées à partir de solutés cristallins solubles ou de solvants miscibles à l'eau, utilisés seuls ou en mélange. Les constituants doivent être dépourvus de toute toxicité, présenter une solubilité suffisante et être, idéalement, bon marché (Rastogi et al., 2004). Le choix du soluté est le résultat d'un compromis entre les exigences technologiques et la qualité du produit final, c'est-à-dire ses caractéristiques physicochimiques (pH, structure, etc.), ses propriétés nutritionnelles et organoleptiques (texture, couleur, etc.), ses propriétés fonctionnelles spécifiques (pouvoir aromatique, sucrant, colorant, état de surface collant ou brillant – dans l'exemple du glucose) et son pouvoir dépresseur de l'activité en eau. Les solutions à base de sucres (saccharose) sont les plus couramment utilisées dans la DO des fruits (Lenart, 1996). Toutefois, il est essentiel de prendre en compte le cout de ces solutés, qui peut se révéler prohibitif (Giraldo et al., 2003).
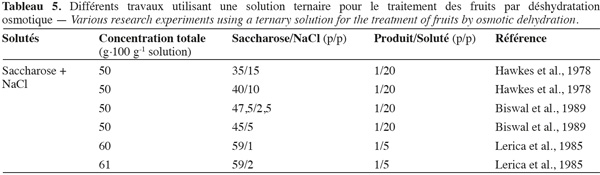
27Utiliser différents solutés en mélange permet de tirer parti de l'effet respectif de chacun (masse molaire, propriétés de diffusion, etc.), mais aussi de développer des interactions spécifiques (soluté-soluté et soluté-aliment) pour mieux maitriser les niveaux de déshydratation et d'imprégnation (Giraldo et al., 2003). En pratique, l'utilisation de sucres de masse molaire élevée (hydrolysats d'amidon de faible indice d'équivalent dextrose), en mélange avec le saccharose, conduit à des niveaux de déshydratation plus élevés et des niveaux d'imprégnation plus faibles que ceux obtenus avec une solution de saccharose. Au contraire, l'utilisation de solutés de masses molaires plus faible que le saccharose, tels que les sucres invertis (fructose, glucose), permet d'obtenir des niveaux d'imprégnation plus élevés (Saurel et al., 1995 ; Torreggiani et al., 2001 ; Corrêa et al., 2010). Pour intégrer au mieux ces deux impératifs et optimiser la déshydratation tout en limitant l'imprégnation, il faut utiliser une solution mixte mettant en œuvre deux solutés de masse molaire bien distinctes (Saurel et al., 1995). L'intérêt de solutions ternaires, ou plus complexes, associant le saccharose avec d'autres sucres de masse molaire différente, ou associant sucres et chlorure de sodium, a été mis en évidence expérimentalement (Lenart, 1996). L'addition de NaCl à une solution osmotique semble augmenter la force d'entrainement lors de la déshydratation. Ce phénomène est attribué à la capacité du NaCl d'abaisser l'activité de l'eau (aw) (Kowalska et al., 2008). LeMaguer et al. (1997) ont montré que l'utilisation d'une solution osmotique contenant 44 % de saccharose et 7 % de NaCl permet d'optimiser les conditions de déshydratation osmotique des carottes.
28Température de la solution osmotique. Le rôle de la température en DO a été étudié sur un large éventail de températures (5-85 °C), le domaine de travail devant être adapté pour chaque famille de produit (Lerica et al., 1985 ; Floury et al., 2008). Une température opératoire comprise entre 20 et 40 °C est souvent considérée comme optimale sur le plan qualitatif (Lerica et al., 1985). À ces températures, la semi-perméabilité des membranes cellulaires de différents végétaux est à peine affectée. L'extraction de l'eau est alors possible seulement par des processus osmotiques. Les transferts d'eau sont favorisés par des températures élevées (Floury et al., 2008). Aussi, le sucrage et confisage des fruits sont habituellement réalisés à 60 °C. Cependant, une température trop élevée n'est pas souhaitable car la température est l'un des facteurs responsables de la rupture des tissus végétaux et des membranes. Par exemple, les membranes plasmatiques commencent à subir des dommages irréversibles et une perte de sélectivité à 55 °C (Thebud et al., 1982). Ceci provoque une modification de la structure et de la texture du matériau, mais aussi le développement de réactions de brunissement enzymatique et de dégradation de la couleur. Pour chaque fruit et légume existe en outre une température seuil, au-delà de laquelle la qualité du produit est affectée et les transferts de soluté prennent le pas sur le transfert d'eau (Floury et al., 2008).
29Durée du traitement. La durée du traitement est un facteur important à considérer, quels que soient les produits traités. Généralement, la perte d'eau, la réduction de masse et le gain en solides augmentent avec le temps de traitement (Rastogi et al., 2004 ; Kowalska et al., 2008).
30Marchal et al. (2005) ont rapporté un changement de sélectivité au cours de la déshydratation, c'est-à-dire que le rapport de la perte en eau sur le gain en solide (WL/SG) décroît au cours du temps. Ce phénomène déjà mentionné est attribué à la mort des cellules qui accompagne l'augmentation de la concentration en sucre dans le tissus (Mavroudis et al., 2004). Ceci conduit à la perte de fonctionnalité de la membrane cellulaire et peut affecter la qualité du produit. Lenart (1996) a montré que la durée de déshydratation de morceaux de pomme ne doit pas dépasser une durée de 15 min à une température comprise entre 70 et 90 °C.
31Mode de mise en contact des phases, effet de l'agitation et du rapport solide/solution. Dans le cas de tranches de fruits, les coefficients de transfert d'eau libre et de saccharose de la solution de déshydratation augmentent, non seulement avec la concentration en saccharose, mais aussi avec l'agitation (Vial et al., 1990). Marouzé et al. (2001) ont montré que le transfert de masse nécessite une agitation entre la solution et le produit qui, pouvant être discontinue, permet un gain d'énergie. En effet, Mavroudis et al. (2004) ont mesuré les effets de l'agitation sur le transfert de masse en termes de nombre de Reynolds et ont montré qu'une forte agitation augmente la perte en eau. Au cours du temps, la perte en eau s'avère moindre lorsque la DO est réalisée en écoulement laminaire plutôt que turbulent. Le gain en solide n'est que peu affectée par le niveau d'agitation, ce qui s'explique par l'existence d'une couche limite diluée autour de l'aliment (Giroux et al., 1994).
32Les transferts de matière dépendent fortement de la manière dont sont mises en contact les phases solide (fragile et « légère » ; l'aliment) et liquide (« lourde » et visqueuse, la solution hypertonique). Une viscosité élevée du liquide augmente la résistance externe (à l'interface solide/liquide) aux transferts de matière et nécessite la mise en œuvre d'un système de brassage adapté, compatible avec la fragilité des produits.
33Des études ont montré qu'un rapport pondéral, solution de déshydratation/tranches de fruit, trop grand (facteur de dilution trop marqué), rend difficile la détermination des différentes substances diffusées et le suivi efficace du phénomène osmotique. Par contre, un rapport petit ralentit le taux de diffusion (Adamrounou et al., 1994).
34Pour une meilleure efficacité de la DO, les systèmes de mise en contact des phases doivent permettre de réduire la dispersion des temps de séjour, forcer l'immersion des produits, réduire les effets de couches limites et préserver la forme et la fragilité des produits.
35Mise en œuvre de la déshydratation osmotique. Chaque fruit ou légume présentant ses propres conditions optimales de déshydratation osmotique, il est difficile de mettre en avant une méthodologie universelle.
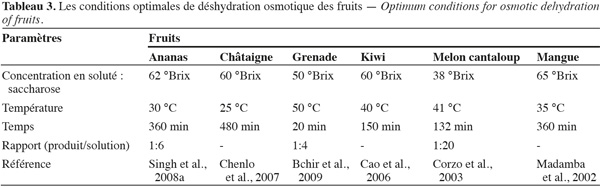
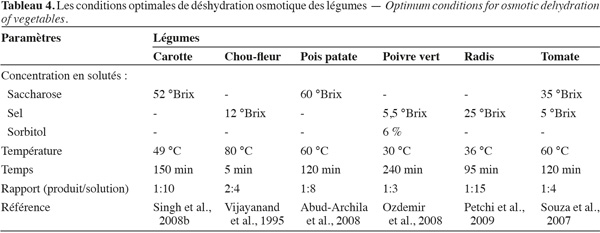
36Typiquement, tant pour les fruits que pour les légumes, le régime turbulent est préféré, avec des temps de séjour compris entre 5 et 480 min. L'optimum de température se trouve habituellement entre 25 °C et 80 °C, et le rapport produit/solution évolue généralement entre 1/2 et 1/20.
37Le soluté le plus fréquemment rencontré est le saccharose, employé à des concentrations comprises entre 38 °Brix et 65 °Brix pour les fruits, entre 35 °Brix et 60 °Brix pour les légumes. L'usage du sel comme soluté est souvent réservé à la déshydratation des légumes.
38Il apparait ainsi nécessaire, industriellement, d'optimiser les conditions de traitement spécifiquement pour chaque produit. Les tableaux 3 et 4 fournissent à ce sujet quelques exemples représentatifs.
2.3. Application de la déshydratation osmotique
39La DO est un procédé relativement lent. Il est donc important de trouver des méthodes qui augmentent le transfert de masse sans affecter la qualité du produit. Ainsi, un traitement permettant d'augmenter la perméabilité des membranes cellulaires et de faciliter la libération de l'eau pendant la DO est obligatoire. Parmi les prétraitements utilisés, on peut citer les méthodes thermiques de blanchiment et de congélation (Kowalska et al., 2008). D'autres procédés consistent à remplacer un traitement unique (ici, la DO) par la combinaison de plusieurs techniques de conservation modérées, respectueuses du produit et pouvant accélérer les transferts. Ces techniques peuvent être l'application du vide, les hautes pressions hydrostatiques, ultrasons, irradiation, centrifugation, champs électrique pulsé, etc.
40Pré-traitement thermique
41Blanchiment. Le blanchiment est un traitement thermique, réalisé par immersion du produit dans un bain d'eau chaude, par passage dans une atmosphère de vapeur ou par chauffage ohmique. Sa durée est de quelques minutes, dans une gamme de 85 °C à 100 °C. Il permet de détruire les enzymes susceptibles d'altérer les légumes ou les fruits avant leur traitement ultérieur (dans notre cas, c'est la déshydratation). Ce procédé prévient ainsi un certain nombre d'altérations organoleptiques telles que des modifications de flaveurs et de couleurs (dégradation de la chlorophylle, brunissement des pommes, etc.). Il limite également certaines pertes nutritionnelles comme la destruction des vitamines et permet l'élimination de l'air et des gaz occlus dans les tissus végétaux facilitant la réhydratation (Dermesonlouoglou et al., 2008).
42Vis-à-vis de la DO, le blanchiment facilite le transfert des matières dissoutes, comme il l'a été rapporté pour les tranches de pomme et de tomate précédemment blanchies à la vapeur (Dermesonlouoglou et al., 2008 ; Kowalska et al., 2008). En revanche, le blanchiment est opéré à des températures trop élevées pour les constituants cellulaires, causant un risque accru d'altération qualitative et de pertes par dissolution.
43Congélation. L'eau est le principal composant de la majorité des aliments congelés du commerce. Une part notable de cette eau est liée à divers degrés : dans des complexes colloïdaux macromoléculaires, dans des structures gélifiées ou fibreuses à l'intérieur des cellules et dans les hydrates. Lors de la congélation, la nucléation de la glace et la croissance des cristaux apportent de nombreuses modifications au produit (Talens et al., 2003). Les composantes cellulaires solubles peuvent atteindre la saturation et précipiter, détruisant ainsi la turgescence des tissus ; des modifications de pH peuvent affecter les complexes colloïdaux ; des changements très marqués de pression osmotique peuvent rompre les membranes semi-perméables, ce qui facilite le transfert de masse au cours de la déshydratation osmotique (Dermesonlouoglou et al., 2008 ; Floury et al., 2008 ; Kowalska et al., 2008 ; Bchir et al., in press). La vitesse de congélation et la température finale de conservation sont des points critiques pour le maintien des propriétés sensorielles, fonctionnelles ou biologiques après la congélation. Une congélation très lente peut conduire à un exsudat excessif à la décongélation, alors qu'une congélation très rapide permet de préserver la texture de certains produits (Talens et al., 2003).
44Méthodes combinées à la DO
45Imprégnation sous vide. Le procédé de DO pour les produits végétaux est généralement mis en œuvre à pression atmosphérique (Raoult-Wack, 1994). Toutefois, l'application d'une dépression stationnaire augmente la vitesse de déshydratation (Corrêa et al., 2010). La présence de gaz occlus dans les espaces intercellulaires de la structure poreuse du produit traité apparait comme la cause principale de la modification des cinétiques de transferts de matières (Fito, 1994 ; Wu et al., 2009). Pendant la DO sous vide, le gaz est expulsé du tissu tandis que l'écoulement capillaire augmente. L'augmentation de la vitesse du transfert d'eau est principalement attribuée à l'action combinée du vide et de l'écoulement capillaire, qui dépend lui-même du volume de gaz occlus dans le tissu. Par conséquent, l'accélération des transferts de matière en DO sous vide est d'autant plus marquée que la porosité du produit est plus importante (Corrêa et al., 2010). Cependant, sous vide pulsé, c'est l'imprégnation qui est favorisée. En effet, lorsque le produit revient à pression atmosphérique, la solution concentrée pénètre massivement dans les pores du produit alimentaire, ce qui a pour conséquence ultérieure d'augmenter la surface de contact entre le produit et la solution et d'accélérer ainsi les transferts de matières (Fito, 1994). Corrêa et al. (2010) ont obtenu par cette technique une perte d'eau plus élevée que dans le cas d'une DO ordinaire, en utilisant le vide seulement pendant 15 min. La technologie du sous vide partiel cyclique trouve tout son potentiel lorsque l'on souhaite formuler le produit à l'aide d'additifs. Ainsi, la texture des fruits peut être améliorée par immersion sous vide dans une solution contenant de la pectine-méthylestérase ou différentes solutions salines, par exemple à base de chlorure de calcium ou de nitrate de calcium (Javeri et al., 1991).
46La DO sous vide permettrait d'obtenir des produits de qualité organoleptique et physicochimique supérieure à celle des produits traités par DO à pression atmosphérique. De plus, cette alternative réduit les couts énergétiques globaux (Fito, 1994).
47Haute pression hydrostatique. Les traitements à haute pression permettent une stabilisation microbiologique significative des aliments, tout en préservant les qualités organoleptiques et nutritionnelles de manière plus importante que les traitements thermiques. Certaines études (Taiwo et al., 2002 ; Rastogi et al., 2004) ont mis en évidence le fait que le prétraitement à haute pression crée un compactage de la structure cellulaire accompagné d'une libération de composants cellulaires. Ce phénomène a pour conséquence la formation d'un gel par liaison d'ions divalents avec la pectine estérifiée qui limite le coefficient de diffusion des solides. À haute pression (jusqu'à 600 Mpa), les membranes cellulaires sont réversiblement perméabilisées. Ce phénomène est imputable aux transitions de phase des bicouches lipidiques de la membrane cellulaire. Cet effet est recherché pour l'élaboration rapide des fruits sucrés tout en préservant l'aspect, les qualités organoleptiques et nutritionnelles du produit frais.
48Cependant, la technologie haute pression reste couteuse, du fait des contraintes de fabrication des enceintes et par leur capacité limitée.
49Ultrasons. L'application d'ultrasons (onde à fréquence supérieur à 20 000 Hz) a déjà fait ses preuves dans l'augmentation du taux de transfert de masse pour la déshydratation osmotique de tissus poreux comme des cubes de pomme. Simal et al. (2001) ont obtenu par cette technique une perte d'eau de 27 % et un gain de solide de 23 % plus élevés que dans le cas d'une DO ordinaire. L'application d'ultrasons produit un phénomène de cavitation consistant en la formation dans le liquide de bulles de gaz qui engendrent, en éclatant, des fluctuations de pression (Fernandes et al., 2009). Cet effet facilite la diffusion pendant le processus osmotique et accélère le dégazage du produit, tout en préservant la saveur, la couleur et les composants nutritifs les plus sensibles à la chaleur (Simal et al., 2001). Cette technique permet aussi l'inactivation des enzymes et des bactéries en cassant leurs membranes cellulaires (Jambrak et al., 2010).
50Irradiation. La structure intérieure du tissu des produits agricoles peut être lysée par γ-irradiation. Il en résulte une plus grande perméabilité des cellules, d'où un transfert de masse amélioré pendant un séchage à l'air (Wang et al., 2000). Rastogi et al. (2004) ont rapporté que la combinaison de la γ-irradiation avec la DO peut résoudre le problème de la diminution des transferts de masse pendant un séchage convectif.
51Chlorure de sodium. Comme il a déjà été mentionné, le type d'agent osmotique utilisé et par conséquent, sa masse moléculaire, affecte fortement la cinétique d'extraction d'eau et de gain en soluté. D'après Simal et al. (2001), le chlorure de sodium est un excellent agent osmotique, en raison de sa faible masse moléculaire qui se reflète par sa grande mobilité pendant le transfert de masse.
52Dans le cas des solutions sucrées-salées (Tableau 5), des effets fortement antagonistes sur le gain en solutés ont été identifiés. L'imprégnation en sel est en particulier limitée par la présence de sucre. Cet effet « barrière » du sucre sur la pénétration du sel a été mis en évidence sur des produits végétaux (Lenart, 1996). Il serait dû à la formation, dans l'aliment, d'une couche périphérique fortement concentrée en sucre. En même temps, la présence de sucre diminuerait fortement le coefficient de diffusion du NaCl (Lenart, 1996). La présence de sel empêche par ailleurs dans certains cas la formation d'une croute superficielle (croutage du produit) causée par le sucre.
53Centrifugation. Cette technique peut être utilisée pour augmenter la perte en eau tout en retardant le gain en solide. Azuara et al. (1998) ont appliqué une force centrifuge de 64 g pendant la déshydratation osmotique à 30 °C de disques de pomme et de pomme de terre. Ils ont observé que ces conditions augmentent le transfert de masse (perte en eau) de 15 % tout en retardant considérablement (80 %) le gain en solide.
54Traitement par champ électrique pulsé. Le traitement par champ électrique pulsé, pour une intensité de champ électrique comprise entre 0,5 et 15 kV.cm-1, entraine une augmentation de la perméabilité des membranes végétales. Son action instantanée, sa courte durée d'application (moins d'une seconde) et la possibilité de traiter des aliments solides à basse température, rendent le champ électrique pulsé plus prometteur qu'un traitement thermique dans une perspective de diffusion ou d'extraction d'eau (séchage) ou de métabolites (Ade-Omowaye et al., 2003). Un autre avantage du champ électrique pulsé réside dans le fait qu'il n'augmente pratiquement pas la température du produit. Ade-Omowaye et al. (2003) ont montré que la cinétique de DO à 20 °C du paprika traité à 2,5 kV.cm-1 est comparable à celle d'une DO réalisée à 55 °C sur le même produit sans application de champ électrique.
55Stabilisation des produits déshydratés osmotiquement par des traitements physiques. Les produits issus du procédé de déshydratation osmotique sont classés parmi les produits à humidité intermédiaire (PAI), à taux d'humidité élevé (Garcia-Martinez et al., 2002). Aussi, le produit n'est pas encore microbiologiquement stabilisé et l'activité de l'eau peut y être élevée. Plusieurs traitements ont été proposés pour parfaire le processus : séchage, congélation, pasteurisation, friture, etc. Les plus communs sont le séchage par air (Ade-Omowaye et al., 2003) et la congélation (Agnelli et al., 2005).
56Séchage. Le séchage provoque un abaissement de l'activité de l'eau du produit, c'est-à-dire que l'eau reste peu disponible pour les micro-organismes et pour les réactions chimiques. On considère généralement qu'un produit est stable lorsque son activité de l'eau est inférieure ou égale à 0,65 (Thebud et al., 1982).
57L'utilisation du séchage dans les industries agro-alimentaires a de multiples objectifs : accroître la durée de conservation des produits, stabiliser les produits agricoles (maïs, luzerne, riz, lait, etc.) pour amortir le caractère saisonnier de certaines activités et transformer les produits par des réactions biochimiques ou biologiques (produits de salaison, touraillage de malt, etc.). Cependant, cette technique est couteuse en énergie : le séchage des produits végétaux nécessite environ 5 000 kJ.kg-1 d'eau évaporée (Mujumdar, 2006).
58La combinaison de la déshydratation osmotique avec le séchage permet d'améliorer la qualité des produits (Fernandes et al., 2006) et de réduire le cout énergétique global de l'élimination de l'eau. En effet, la pré-déshydratation diminue le temps de séchage et le besoin énergétique du séchage complémentaire (Fernandes et al., 2006). En effet, la DO n'exige qu'entre 100 et 2 400 kJ.kg-1 d'eau enlevée, selon les applications (Mujumdar, 2006). Après une période de mise en régime, la cinétique de séchage par l'air est caractérisée par une période à vitesse constante, correspondant à l'évaporation de l'eau de surface qui est constamment renouvelée par transport interne et qui se traduit par une variation linéaire de la teneur en eau en fonction du temps. Cette première période est suivie d'une ou plusieurs étapes à vitesses décroissantes, où les forces capillaires n'acheminent plus suffisamment d'eau en surface pour compenser l'évaporation (Ade-Omowaye et al., 2003). Pour les produits alimentaires et biologiques, le séchage est limité par la résistance des parois cellulaires, par la migration des solutés qui obstruent les pores et par le croutage de la surface (Wang et al., 2000 ; Ade-Omowaye et al., 2003).
59Congélation. La congélation des aliments est un excellent moyen de maintenir pendant longtemps, presque inchangées, leurs valeurs nutritionnelles. Cette préservation de la qualité s'explique tant par l'abaissement de la température qui ralentit les réactions biochimiques et inhibe les activités microbiennes que par la réduction de l'activité de l'eau du substrat (Floury et al., 2008).
60La possibilité de prétraiter les produits par une déshydratation partielle (voire par imprégnation) avant congélation semble prometteuse (Talens et al., 2003 ; Wu et al., 2009). Cette technique, dite de déshydro-congélation, permet la réduction de la quantité d'eau dans le produit afin de diminuer la quantité de cristaux formés, le temps de congélation et de décongélation. Il en résulte une meilleure conservation des propriétés du fruit. La déshydratation osmotique constitue de ce point de vue un prétraitement efficace (Talens et al., 2003 ; Dermesonlouoglou et al., 2008).
61Au point de vue énergétique, on notera que, sans déshydratation préalable, la congélation des fruits nécessite entre 250 et 340 kJ.kg-1 d'eau congelée et entre 150 et 320 kJ.kg-1 d'eau congelée pour les légumes (Mujumdar, 2006).
2.4. Équipements pour la DO
62Diverses configuration de mise en contact des phases ont été proposées et étudiées (Figure 1). En pratique, l'opération peut être réalisée en contacteur continu ou discontinu, avec ou sans agitation. Les contacteurs discontinus (batch) sont les plus utilisés. Certains auteurs proposent simplement une immersion forcée des morceaux dans le liquide (Marouzé et al., 2001). Cette solution est d'ailleurs utilisée dans la plupart des entreprises de semi-confisage de fruits. D'autres systèmes plus élaborés ont été proposés en vue d'une mise en œuvre du procédé en continu : fluidisation inverse (Raoult-Wack, 1994), brassage mécanique ou brassage mixte hydraulique/mécanique (Giroux et al., 1994).

2.5. Qualité des produits végétaux traités par DO
63La déshydratation osmotique permet le maintien des qualités nutritionnelles, voire l'amélioration des qualités organoleptiques de produits souvent fragiles, ainsi qu'une meilleure résistance à des traitements ultérieurs (séchage, stockage, etc.) (Albagnac et al., 2002). En effet, en tenant compte de la possibilité de transferts de masse dans les deux sens (gain de solutés et perte de solutés), la déshydratation osmotique permet la formulation de nouveaux produits (Albagnac et al., 2002). Selon Raoult-Wack (1994), la déshydratation osmotique permet de modifier les propriétés fonctionnelles des produits en les imprégnant des solutés souhaités. La DO augmente le rapport sucre/acide, améliore la texture et préserve la couleur pendant la déshydratation et le stockage (Raoult-Wack, 1994). Toutefois, il convient de noter que les apports en soluté, notamment en sucres, ne vont pas toujours dans le sens d'une amélioration des propriétés nutritionnelles.
64En évitant le contact avec l'oxygène de l'air, la DO limite les réactions d'oxydation, mais aussi les pertes de composés volatils par entrainement. Elle est efficace même à température modérée (souvent inférieure à 50 °C), ménageant ainsi les composés thermosensibles tels que les arômes, pigments et vitamines (Vial et al., 1990).
65L'effet de la DO sur les différents attributs de la qualité est détaillé ci-après.
66Saveur. Au cours de la DO, l'introduction de soluté modifie inévitablement le rapport acides/sucre, ce qui adoucit la saveur du produit final. Cependant, en séchage ou en DO, l'élimination d'eau ne doit pas se faire au détriment de la saveur (i.e. des arômes). En règle générale, tout facteur tendant à augmenter la viscosité de la solution osmotique diminue la diffusivité relative des arômes. Ainsi, il vaut mieux en DO diminuer la température et augmenter la concentration du produit en matières sèches pour conserver les arômes (Torreggiani et al., 2001).
67Couleur. La couleur est un attribut très important des aliments, car elle influence l'acceptabilité par le consommateur (40 % du critère d'acceptabilité) (Falade et al., 2007). Des couleurs anormales, suggérant la détérioration de la qualité ou du caractère comestible, sont des causes de rejet par le consommateur. Beaucoup de réactions peuvent affecter la couleur pendant le traitement thermique des fruits et de leurs dérivés. Les plus communes sont la dégradation des pigments (chlorophylle, β-carotène, etc.) et les caroténoïdes et la chlorophylle, et les réactions de brunissement telles que la réaction de Maillard des hexoses, et l'oxydation de l'acide ascorbique. Au cours de la DO, les solutés introduits réduisent les modifications de la couleur du produit, notamment en limitant la dégradation des pigments chlorophylliens et caroténoïdes. L'activité enzymatique de polyphenol-oxydase responsable du brunissement enzymatique est alors inhibée. La sensibilité des produits au brunissement non enzymatique est également limitée (Torreggiani et al., 2001).
68Texture. Le départ d'eau, ainsi que son remplacement par d'autres molécules, implique des contraintes mécaniques qui modifient la conformation du matériau. Ainsi, le produit se rétracte sous l'action des fortes densités de flux (Castello et al., 2009 ; Garcia-Segovia et al., 2010). D'autre part, au cours du processus de déshydratation, les polysaccharides (pectine, hémicelluloses, cellulose) qui constituent la membrane cellulaire sont partiellement solubilisés, modifiant ainsi la fermeté du produit (Nunes et al., 2008). Ces modifications sont quantifiables par l'analyse de la texture du produit ; ces mesures sont basées sur la résistance à la pénétration par une sonde (Torreggiani et al., 2001).
69Réhydratation. Les produits déshydratés sont souvent conçus pour être réhydratés ultérieurement. La capacité et la vitesse de réhydratation qui est souvent longue (plusieurs heures), sont décrites comme les principaux critères de la qualité des produits finis. La réhydratation des fruits et légumes a été bien étudiée (Taiwo et al., 2002 ; Rastogi et al., 2004). Une étude de la cinétique de réhydratation peut être effectuée pour mesurer l'ampleur nette des dommages subis par le produit pendant les étapes de transformation antérieures (Rastogi et al., 2004).
70La réhydratation est influencée par plusieurs facteurs, groupés en tant que facteurs intrinsèques (composition chimique du produit, traitement de pré-séchage, formulation de produit, techniques et conditions de séchage) et extrinsèques (composition du milieu d'immersion, température, conditions hydrodynamiques). Certains de ces facteurs induisent des changements de structure et de composition du tissu végétal, ce qui influence les propriétés de reconstitution lors de la réhydratation (Taiwo et al., 2002). Par exemple, plus la concentration en sucre est grande ou plus la période de la DO est longue avant séchage, meilleure est la réhydratation, le sucre empêchant probablement le rétrécissement du tissu végétal lors du séchage à l'air (Neumann, 1972). Dans l'étude sur le céleri sec, Neumann (1972) a rapporté que la réhydratation à des températures élevées diminue le temps exigé pour atteindre la capacité maximum de sorption d'eau et le contenu d'humidité finale.
3. Valorisation des fruits conservés en solutions sucrées
71Les fruits ont été depuis longtemps conservés par le sucre. La fabrication de produits déshydratés osmotiquement remonte à la haute antiquité. Aujourd'hui, la conservation des fruits par les sucres est devenue une industrie à part entière et est appliquée à une vaste gamme de produits, comme les fruits confits (Espiard, 2002), les compotes et purées (Espiard, 2002), la confiture (Albagnac et al., 2002 ; Espiard, 2002), les marmelades et pâtes de fruits (Albagnac et al., 2002 ; Espiard, 2002). On trouve sur le marché un nombre de produits apparentés ayant tous subi des transformations visant non seulement à obtenir des fruits stables à température ambiante (grâce à une réduction de leur activité d'eau), mais à aussi leur conférer une texture et une saveur spécifique (Albagnac et al., 2002).
4. Conclusion
72À travers cette étude bibliographique, nous espérons apporter des bases scientifiques et techniques pour l'étude de la conservation des produits végétaux par déshydratation osmotique. La maitrise de cette technique revêt une importance primordiale pour les industries alimentaires car elle permet un gain d'énergie et, moyennant la prise en compte de l'effet des apports en solutés par imprégnation, une préservation de la qualité nutritionnelle des produits traités. Ainsi, l'utilisation de la DO permet un meilleur contrôle et une maitrise de la qualité des produits finis. Il en découle un élargissement de la gamme des fruits traités, une diversification des caractéristiques des produits obtenus et le développement de produits nouveaux. En effet, cette technique permet de définir des voies de valorisation de plusieurs fruits et légumes. Prenons l'exemple des graines de grenade, fruit jusqu'ici consommé presque exclusivement frais, pendant la période de récolte. De récents travaux (Bchir et al., 2009 ; Bchir et al., in press) ont évalué l'aptitude des graines de grenade en DO, en fonction de la température et du choix des solutés. Ces travaux ouvrent la voie à de nouveaux modes de consommation, comme les graines confites, qui pourraient être introduites dans d'autres produits transformés. De la sorte, il devient possible d'exploiter bien mieux les excellentes propriétés nutritionnelles, biologiques et thérapeutiques de ce fruit.
73Soulignons enfin que l'introduction de la DO dans le processus de transformation des fruits permet en général une réduction du nombre d'étapes et/ou de durée totale du traitement, et de bénéficier de l'effet protecteur des solutés incorporés. La littérature souligne aussi que, d'une manière générale, la déshydratation osmotique doit être complétée par un traitement thermique, chimique, mécanique ou physique afin de parfaire la stabilisation du produit fini.
Bibliographie
Abud-Archila M. et al., 2008. Optimization of osmotic dehydration of yam bean (Pachyrhizus erosus) using an orthogonal experimental design. J. Food Eng., 84, 413-419.
Adamrounou L.T., Conway J. & Castaigne F., 1994. Influence de la déshydratation partielle par osmose sur la composition de tranches de pomme. Sci. Aliments, 14, 75-85.
Ade-Omowaye B.I.O., Rastogi N.K., Angersbach A. & Knorr D., 2003. Combined effects of pulsed electric field pre-treatment and partial osmotic dehydration on air drying behaviour of red bell pepper. J. Food Eng., 60, 89-98.
Agnelli M.E., Marani C.M. & Mascheroni R.H., 2005. Modelling of heat and mass transfer during (osmo) dehydrofreezing of fruits. J. Food Eng., 69, 415-424.
Albagnac P.G., Varoquaux J. & Montigaud C.I., coord., 2002. Technologies de transformation des fruits. Paris : Lavoisier-Tec & Doc.
Azuara E., Beristain C.I. & Gutiérrez G.F., 1998. A method for continuous kinetic evaluation of osmotic dehydration. Lebensm. Wiss. Technol., 31, 317-321.
Bchir B., Besbes S., Attia H. & Blecker C., 2009. Osmotic dehydration of pomegranate seeds: mass transfer kinetics and DSC characterisation. Int. J. Food Sci. Technol., 44, 2208-2217.
Bchir B., Besbes S., Attia H. & Blecker C. Osmotic dehydration of pomegranate seeds (Punica granatum L.): effect of freezing pre-treatment. J. Food Process Eng. (DOI: 10.1111/j.1745-4530.2010.00591.x) (in press).
Biswal R.N. & Le Maguer M., 1989. Mass transfer in plant material in contact with aqueous solution of ethanol and sodium chloride: equilibrium data. J. Food Process Eng., 11, 159-176.
Cao H. et al., 2006. Optimization of osmotic dehydration of kiwifruit. Drying Technol., 24, 89-94.
Castello M., Igual M., Fito P. & Chiralt A., 2009. Influence of osmotic dehydration on texture, respiration and microbial stability of apple slices (var. 'Granny Smith'). J. Food Eng., 91, 1-9.
Chenlo F., Moreira R., Fernandez-Herrero C. & Vazquez G., 2007. Osmotic dehydration of chestnut with sucrose: mass transfer processes and global kinetics modelling. J. Food Eng., 78, 765-774.
Cornillon P., 2000. Characterization of osmotic dehydrated apple by NMR and DSC. Lebensm. Wiss. Technol., 33, 261-267.
Corrêa J., Pereira L., Vieira G. & Hubinger M., 2010. Mass transfer kinetics of pulsed vacuum osmotic dehydration of guavas. J. Food Process Eng., 96, 498-504.
Corzo O. & Gomez E., 2003. Optimization of osmotic dehydration of cantaloupe using desired function methodology. J. Food Eng., 64, 213-219.
Crank J., 1975. The mathematics of diffusion. 2nd ed. Oxford, UK: Clarendon Press.
Dermesonlouoglou E.K., Pourgouri S. & Taoukis P.S., 2008. Kinetic study of the effect of the osmotic dehydration pre-treatment to the shelf life of frozen cucumber. Innovative Food Sci. Emerg. Technol., 9, 542-549.
Derossi A., De Pilli T., Severini C. & McCarthy M.J., 2008. Mass transfer during osmotic dehydration of apples. J. Food Eng., 86, 519-528.
Eren I. & Kaymak-Ertekin F., 2007. Optimization of osmotic dehydration of potato using response surface methodology. J. Food Eng., 79, 344-352.
Espiard E., 2002. Introduction à la transformation industrielle des fruits. Paris : Lavoisier-Tec & Doc.
Falade K., Igbeka J. & Ayanwuyi F., 2007. Kinetics of mass transfer and colour changes during osmotic dehydration of watermelon. J. Food Eng., 80, 979-985.
Fernandes F., Rodrigues S., Gaspareto O.C.P. & Oliveira E.L., 2006. Optimization of osmotic dehydration of papaya followed by air-drying. Food Res. Int., 39, 492-498.
Fernandes F., Gallao M.I. & Rodrigues S., 2009. Effect of osmosis and ultrasound on pineapple cell tissues structure during dehydration. J. Food Eng., 90, 186-190.
Ferrando M. & Spiess W., 2001. Cellular of plant tissue during the osmotic treatment with sucrose, maltose and trehalose solutions. J. Food Eng., 49, 115-127.
Ferrari C. & Hubinger M., 2008. Evaluation of the mechanical properties and diffusion coefficients of osmodehydrated melon cubes. Int. J. Food Sci. Technol., 43, 2065-2074.
Fito P., 1994. Modelling of vacuum osmotic dehydration of food. J. Food Eng., 22, 313-328.
Floury J., Le Bail A. & Pham Q.T., 2008. A three-dimensional numerical simulation of the osmotic dehydration of mango and effect of freezing on the mass transfer rates. J. Food Eng., 85, 1-11.
Garcia-Martinez E., Martinezmonzo J., Camacho M.M. & Martineznavarrete N., 2002. Characterisation of reused osmotic solution as ingredient in new product formulation. Food Res. Int., 35, 307-313.
Garcia-Segovia P., Mognetti C., André-Bello A. & Martinez-Monzo J., 2010. Osmotic dehydration of Aloe vera (Aloea barbadensis Miller). J. Food Eng., 97, 154-160.
Giraldo G., Talens P., Fito P. & Chiralt A., 2003. Influence of sucrose solution concentration on kinetics and yield during osmotic of mango. J. Food Eng., 58, 33-43.
Giroux F. & Marouzé C., 1994. Étude de dispositifs permettant l'agitation des produits dans les procédés de déshydratation/imprégnation par immersion. In : GFGP. Agitation et mélange en biotechnologies alimentaire et industrielle. Paris : Lavoisier-Tec & Doc, 29-34.
Hawkes J. & Flink J.M., 1978. Osmotic concentration of fruits slices prior to freeze dehydration. J. Food Process. Preserv., 2, 265-284.
Heng K., Guilbert S. & Cuq J.L., 1990. Osmotic dehydration of papaya: influence of process variables on the product quality. Sci. Aliments, 10, 831-848.
Islam M.N. & Flink J.M., 1982. Dehydration of potato. 2. Osmotic concentration and its effects on air drying behaviour. J. Food Technol., 17, 387-403.
Jambrak A. et al., 2010. Ultrasound effect on physical properties of corn starch. Carbohydr. Polym., 79, 91-100.
Javeri H., Toledo R. & Wicker L., 1991. Vacuum infusion of citrus pectinmethylesterase and calcium effects on firmness of peaches. J. Food Sci., 56, 739-742.
Jena S. & Das H., 2004. Modelling for moisture variation during osmo-concentration in apple and pineapple. J. Food Eng., 66, 425-432.
Jiokap Nono Y., Nuadjea G.B., Raoult Wack A.L. & Giroux F., 2001. Comportement de certains fruits tropicaux traités par déshydratation-imprégnation par immersion dans une solution de saccharose. Fruits, 56, 75-83.
Khoyi M. & Hesari J., 2007. Osmotic dehydration kinetics of apricot using sucrose solution. J. Food Eng., 78, 1355-1360.
Kowalska H., Lenart A. & Leszczyk D., 2008. The effect of blanching and freezing on osmotic dehydration of pumpkin. J. Food Eng., 86, 30-38.
Krokida M.K., Karathanos V.T. & Maroulis Z.B., 2000. Effect of osmotic dehydration on colour and sorption characteristics of apple and banana. Drying Technol., 18, 937-950.
LeMaguer H. & Sharma S., 1997. Design and selection of processing conditions of pilot scale contactor for continuous osmotic dehydration of carrots. J. Food Process Eng., 21, 75-88.
Lenart A., 1996. Osmo-convective drying of fruits and vegetables: technology and application. Drying Technol., 14, 391-413.
Lerica C.R., Pinnavaia T.G., Dalla Rosa M. & Bartolucci L., 1985. Osmotic dehydration of fruit: influence of osmotic agents on drying behaviour and product quality. J. Food Eng., 50, 1217-1226.
Madamba P. & Lopez R., 2002. Optimization of the osmotic dehydration of mango (Mangifera indica L.) slices. Drying Technol., 20, 1227-1242.
Marchal L., Allali H. & Vorobiev E., 2005. Blanchiment de fraise par chauffage ohmique : incidence sur la cinétique de déshydratation-imprégnation par immersion. Paris : Lavoisier.
Marouzé C., Giroux F., Collignan A. & Rivier M., 2001. Equipment design for osmotic treatments. J. Food Eng., 49, 207-221.
Mavroudis N.E., Dejmek P. & Sjoholm I., 2004. Osmotic treatment induced cell death and osmotic processing kinetics of apples with characterised raw material properties. J. Food Eng., 63, 47-56.
Mayor L., Pissarra J. & Sereno A., 2008. Microstructural changes during osmotic dehydration of parenchymatic pumpkin tissue. J. Food Eng., 85, 326-339.
Mujumdar A.S., 2006. Handbook of industrial drying. 3rd ed. New York, USA: Taylor and Francis Group, LLC, 688-700.
Neumann H.J., 1972. Dehydrated celery: effects of pre-drying treatment and rehydration procedures on reconstitution. J. Food Sci., 37, 437-441.
Nieto A.B., Salvatori D.M., Castro M.A. & Alzamora S.M., 2004. Structural changes in apple tissue during glucose and sucrose osmotic dehydration: shrinkage, porosity, density and microscopic features. J. Food Eng., 61, 269-278.
Nunes C. et al., 2008. Effect of candying on microstructure and texture of plums (Prunus domestica L.). Lebensm. Wiss. Technol., 41, 1776-1783.
Ohkuma C. et al., 2008. Glass transition properties of frozen and freeze-dried surimi products: effect of sugar and moisture on the glass transition temperature. Food Hydrocolloids, 22, 255-262.
Ozdemir M., Ozen B., Dock L. & Floros J., 2008. Optimization of osmotic dehydration of diced green peppers by response surface methodology. Food Sci. Technol., 41, 2044-2050.
Panades G. et al., 2008. Mass transfer mechanisms occurring in osmotic dehydration of guava. J. Food Eng., 87, 386-390.
Petchi M. & Manivasagan R., 2009. Optimization of osmotic dehydration of radish in salt solution using response surface methodology. Int. J. Food Eng., 5(3), DOI: 10.2202/1556-3758.1584.
Raoult-Wack A.L., 1994. Recent advances in the osmotic dehydration of foods. Food Sci. Technol., 5, 255-260.
Rastogi N.K. & Raghavarao K.S.M.S., 2004. Mass transfer during osmotic dehydration of pineapple: considering Fickian diffusion in cubical configuration. Lebensm. Wiss. Technol., 37, 43-47.
Riggs P.D., Kinchesh P., Braden M. & Patel P.M., 2001. Nuclear magnetic imaging of an osmotic water uptake and delivery process. Biomaterials, 22, 419-427.
Riva M. et al., 2005. Structure property relationships in osmo-air-dehydrated apricot cubes. Food Res. Int., 38, 533-542.
Saurel R., Raoult-Wack A.L. & Rios Guilbert S., 1995. Approches technologiques nouvelles de la déshydratation-imprégnation par immersion (DII). Ind. Aliment. Agric., 2, 7-13.
Shi J., Le Maguer M., Wang S. & Liptay A., 1998. Application of osmotic treatment in tomato processing effect of skin treatments on mass transfer in osmotic dehydration of tomatoes. Food Res. Int., 30, 669-674.
Simal S. et al., 2001. Water and salt diffusion during cheese ripening: effect of the external and internal resistances to mass transfer. J. Food Eng., 48, 269-275.
Singh C., Sharma H. & Sarkar B., 2008a. Optimization of process conditions during dehydration of fresh pineapple. J. Food Sci. Technol.-Mysore, 45, 312-316.
Singh B., Panesar P. & Nanda V., 2008b. Optimization of osmotic dehydration process of carrot cubes in sucrose solution. J. Food Process Eng., 31, 1-20.
Souza J. et al., 2007. Optimization of osmotic dehydration of tomatoes in a ternary system followed by air-drying. J. Food Eng., 83, 501-509.
Sunjka P. & Raghavan G., 2004. Assessment of pretreatment methods and osmotic dehydration for cranberries. Can. Biosyst. Eng., 46, 335-340.
Taiwo K.A., Angersbach A. & Knorr D., 2002. Influence of high intensity electric field pulses and osmotic dehydration on the rehydration characteristics of apple slices at different temperatures. J. Food Eng., 52, 185-192.
Talens P., Escriche I., Martinez-Navarrete N. & Chiralt A., 2003. Influence of osmotic dehydration and freezing on the volatile profile of kiwi fruit. Food Res. Int., 36, 635-642.
Thebud R. & Santarius K.A., 1982. Effects of high-temperature stress on various bio-membranes of leaf cells in situ and in vitro. Plant Physiol., 70, 200-205.
Tortoe C., Orchard J., Beezer A. & O'Neil M., 2007. Potential of calorimetry to study osmotic dehydration of food materials. J. Food Eng., 78, 933-940.
Torreggiani D. & Bertolo G., 2001. Osmotic pre-treatments in fruit processing: chemical, physical and structural effects. J. Food Eng., 49, 247-253.
Uddin M., Ainsworth P. & Ibanoglu S., 2004. Evaluation of mass exchange during osmotic dehydration of carrots using response surface methodology. J. Food Eng., 65, 473-477.
Vial C., Guilbert S. & Cuq J., 1990. Osmotic dehydration of kiwi-fruits: influence of process variables on the colour and ascorbic acid content. Sci. Aliments, 11, 63-84.
Vijayanand P., Chand N. & Epieson W., 1995. Optimization of osmotic dehydration of cauliflower. J. Food Process. Preserv., 19, 229-242.
Wang W.C. & Sastry S.K., 2000. Effects of thermal and electrothermal pretreatments on hot air drying rate of vegetable tissue. J. Food Process Eng., 23, 299-319.
Wu L. et al., 2009. Applicability of vacuum-dehydrofreezing technique for the long-term preservation of fresh-cut eggplant: effects of process conditions on the quality attributes of the samples. J. Food Process Eng., 91, 560-565.
Om dit artikel te citeren:
Over : Brahim Bchir
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Technologie des Industries agro-alimentaires. Passage des Déportés, 2. B- 5030 Gembloux (Belgique). E-mail : bchbrahim@yahoo.fr
Over : Souhail Besbes
Laboratory of Food Analyses. National Engineering School of Sfax. Route de Soukra, 3038. TN- Sfax (Tunisie).
Over : Jean-Michel Giet
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Technologie des Industries agro-alimentaires. Passage des Déportés, 2. B- 5030 Gembloux (Belgique).
Over : Hamadi Attia
Laboratory of Food Analyses. National Engineering School of Sfax. Route de Soukra, 3038. TN- Sfax (Tunisie).
Over : Christophe Blecker
Univ. Liège - Gembloux Agro-Bio Tech. Unité de Technologie des Industries agro-alimentaires. Passage des Déportés, 2. B- 5030 Gembloux (Belgique).






